名校
解题方法
1 . 反应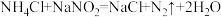 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是
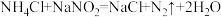 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是A. 的电子式为 的电子式为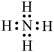 | B. 中 中 元素的化合价为+5 元素的化合价为+5 |
C.N2分子中存在 键 键 | D.H2O分子结构呈直线型 |
您最近半年使用:0次
解题方法
2 . 近日,科学家利用铁配合物催化氮气选择性转化成肼。铁配合物结构如图所示(Et为乙基:-CH2CH3)。

回答下列问题:
(1)基态 的价层电子排布式
的价层电子排布式___________ ,微粒半径Fe___________  。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)
(2) 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是___________ 。P原子的杂化类型是___________ 。
(3) 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是___________ 。
(4) 的VSEPR模型为
的VSEPR模型为___________ 。写出N2的一种等电子体___________ 。
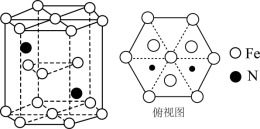
(5)某种磁性氮化铁的晶胞结构如图所示。已知: 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为___________ 。该晶体的密度为___________  (只列计算式)。
(只列计算式)。

回答下列问题:
(1)基态
 的价层电子排布式
的价层电子排布式 。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)(2)
 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是(3)
 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是(4)
 的VSEPR模型为
的VSEPR模型为(5)某种磁性氮化铁的晶胞结构如图所示。已知:
 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为 (只列计算式)。
(只列计算式)。
您最近半年使用:0次
3 . 下列各图中的大黑点代表原子序数从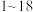 号元素的原子实(原子实是原子除最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键。下列各图表示的结构与化学式一定不相符的是
号元素的原子实(原子实是原子除最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键。下列各图表示的结构与化学式一定不相符的是
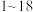 号元素的原子实(原子实是原子除最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键。下列各图表示的结构与化学式一定不相符的是
号元素的原子实(原子实是原子除最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键。下列各图表示的结构与化学式一定不相符的是| A | B | C | D |
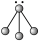 | 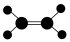 |  |  |
 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 结合VSEPR理论和杂化轨道理论,判断下列分子的中心原子杂化方式、空间构型。
| 分子 | 中心原子,写元素符号 | 价层电子对数 | 杂化轨道数 | 轨道杂化方式 | 孤电子对数 | 分子的空间构型 |
 | C | 4 | 4 |  | 0 | 正四面体 |
 | ||||||
 | ||||||
 |
您最近半年使用:0次
2024-03-31更新
|
315次组卷
|
2卷引用:北京市十一学校2023-2024学年高一下学期开学考化学试题
名校
5 . 回答下列问题。
(1) 中,
中, 的轨道杂化方式为
的轨道杂化方式为___________ ;列举与 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:___________ 、___________ (填化学式)。
(2)用价电子对互斥理论推断 分子中,
分子中, 原子的轨道杂化方式为
原子的轨道杂化方式为___________ , 分子中
分子中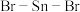 的键角
的键角___________  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(3)下列物质中具有旋光性的是___________(填标号)。
(1)
 中,
中, 的轨道杂化方式为
的轨道杂化方式为 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:(2)用价电子对互斥理论推断
 分子中,
分子中, 原子的轨道杂化方式为
原子的轨道杂化方式为 分子中
分子中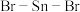 的键角
的键角 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。(3)下列物质中具有旋光性的是___________(填标号)。
A.乙醇( ) ) | B.1, 二氧丙烷( 二氧丙烷( ) ) |
C.乙酸( ) ) | D.乳酸(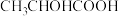 ) ) |
您最近半年使用:0次
名校
6 . H2S 和 SO2 反应生成 S 和 H2O。下列有关H2S、SO2、SO 、SO
、SO 的说法正确的是
的说法正确的是
 、SO
、SO 的说法正确的是
的说法正确的是| A.H2S 的沸点比H2O 的高 | B.SO2 与H2S 反应体现SO2 的还原性 |
C.SO 中S 原子轨道杂化类型为sp3 中S 原子轨道杂化类型为sp3 | D.SO 的空间构型为平面正方形 的空间构型为平面正方形 |
您最近半年使用:0次
7 . 下列“类比”结论正确的是
| A.C在足量O2中燃烧生成CO2,则S在足量O2中燃烧生成SO3 |
| B.NaCl与浓H2SO4共热可制HCl,则NaI与浓H2SO4共热也可制HI |
| C.H2O的分子构型为V形,则H2S的分子构型也为V形 |
| D.金属钠在空气中燃烧生成Na2O2,则金属锂在空气中燃烧也生成Li2O2 |
您最近半年使用:0次
名校
解题方法
8 . 下列化学用语或图示表达不正确 的是
A.基态Cl原子的价电子轨道表示式: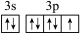 |
B.NaOH的电子式: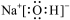 |
C.氨分子的VSEPR模型: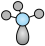 |
D. 结构示意图: 结构示意图: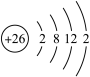 |
您最近半年使用:0次
解题方法
9 . 下列依据和结论对应正确的是
| 依据 | 结论 | |
| A | 一般来说,能层越高,电子的能量越高 | 电子按3p→3d→4s的顺序填充 |
| B | Si、P、S的最外层电子数依次增多 | Si、P、S的第一电离能依次增大 |
| C |  是直线型分子, 是直线型分子, 与 与 组成相似 组成相似 |  也是直线型分子 也是直线型分子 |
| D | 冰晶体中水分子间存在氢键,氢键具有方向性和饱和性 | 冰晶体中,水分子不能紧密堆积 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
10 . 下列说法不正确的是
A. 、 、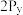 、 、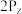 轨道相互垂直,但能量相等 轨道相互垂直,但能量相等 |
| B.最外层电子数为2的元素都分布在s区 |
C.“ ”中三原子不在一条直线上时,也能形成氢键 ”中三原子不在一条直线上时,也能形成氢键 |
D.价层电子对互斥模型中, 键电子对数不计入中心原子的价层电子对数 键电子对数不计入中心原子的价层电子对数 |
您最近半年使用:0次



