解题方法
1 . 有关NH3分子的结构分析正确的是
| A.中心原子孤电子对数为0,分子为平面三角形,键角为120° |
| B.中心原子孤电子对数为0,分子为三角锥形,键角为107° |
| C.中心原子孤电子对数为1,分子为三角锥形,键角为107° |
| D.中心原子孤电子对数为1,分子为平面三角形,键角为109°28′ |
您最近一年使用:0次
解题方法
2 . LiAlH4是有机合成中常用的还原剂,可在乙醚中制得:4LiH+AlCl3=LiAlH4+3LiCl。下列说法错误的是
| A.Li+半径大于H-半径 |
| B.[AlH4]-空间构型是正四面体 |
| C.LiAlH4中存在离子键、σ键、配位键 |
| D.Al2Cl6为AlCl3的双聚分子,氯原子提供给铝原子孤对电子 |
您最近一年使用:0次
2021-05-19更新
|
163次组卷
|
2卷引用:重庆市缙云联盟2021-2022学年高一10月质量检测化学试题
3 . 类比推理是化学中常用的思维方法,下列推理合理的是
| A.Fe与Cl2反应可生成FeCl3,推测Fe与I2反应生成FeI3 |
| B.CaO与Al2O3都可与酸反应生成对应的盐和水,推测两者都属于碱性氧化物 |
| C.SO2与CaCl2溶液不反应,推测SO2与Ca(NO3)2溶液也不反应 |
| D.CO2是直线型分子,推测CS2也是直线型分子 |
您最近一年使用:0次
2021-04-30更新
|
343次组卷
|
2卷引用:辽宁省大连市2022-2023学年高一3月月考化学试题
20-21高一下·浙江·阶段练习
解题方法
4 . 下列表示不正确的是
A.CO2的电子式: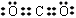 | B.NH3的空间结构:正三角形 |
C.水分子的球棍模型: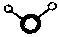 | D.Na+的结构示意图: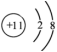 |
您最近一年使用:0次
5 . 图为周期表中短周期的一部分。若Y原子价电子排布为ns2np3,下列说法正确的是
| X | ||
| Y | Z | W |
| A.X和Z形成的化合物的空间构型一定为V形 |
| B.YW5分子中所有原子均满足8电子稳定结构 |
| C.X的最高正价和最低负价的绝对值之和为8 |
| D.X、Y、Z、W都可以与氢元素形成18电子结构物质 |
您最近一年使用:0次
名校
解题方法
6 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:___ 。
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:____ 。其正三价离子的未成对电子数为____
(3)写出3p轨道上有2个未成对电子的元素的符号:____ 。
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为___ 。
(5)基态原子的4s能级中只有1个电子的元素共有___ 种
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为___ ,属于____ 区元素;[Cu(NH3)4]SO4中所含的化学键有___ ,,[Cu(NH3)4]SO4的外界离子的空间构型为____ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:
(3)写出3p轨道上有2个未成对电子的元素的符号:
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
(5)基态原子的4s能级中只有1个电子的元素共有
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为
您最近一年使用:0次
名校
解题方法
7 . 下列分子或离子中,不含有孤对电子的是( )
| A.H2O | B.H3O+ | C.NH3 | D.NH |
您最近一年使用:0次
2020-11-20更新
|
475次组卷
|
12卷引用:高中化学人教版 选修三 第2章 分子结构与性质 价电子对互斥理论
高中化学人教版 选修三 第2章 分子结构与性质 价电子对互斥理论2015-2016学年贵州省思南中学高二下第一次月考化学试卷(已下线)同步君 选修3 第二章 第二节 第一课时 价电子互斥理论宁夏育才中学勤行校区2016-2017学年高二下学期第一次(3月)月考化学试题人教版2017-2018学年高二化学选修三同步训练:2.2 分子的立体构型(第1课时)广西蒙山县第一中学2017-2018学年高二下学期期末考试化学试题2020届高三化学二轮物质结构题型专攻——基态原子核外电子排布【选择基础专练】宁夏海原县第一中学2019-2020学年高二下学期第一次月考化学试题山东省淄博市般阳中学2020-2021学年高二上学期期中考试化学试题(已下线)作业09 配合物与超分子-2021年高二化学暑假作业(人教版2019)内蒙古赤峰市元宝山区第一中学2021-2022学年高二下学期4月月考化学试题浙江省海盐高级中学2021-2022学年高二下学期开学测试化学试题
名校
解题方法
8 . 按要求填空:
(1)质量数为37的氯原子符号为
(2)NH 的电子式
的电子式
(3)X射线衍射测定等发现,I3AsF6中存在I 离子。I
离子。I 离子的几何构型为
离子的几何构型为
(4)与O3分子互为等电子体的一种阴离子为
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-C1键的键能(242.7kJ/mol),原因是
您最近一年使用:0次
2020-08-23更新
|
297次组卷
|
2卷引用:天津市第四十三中学2020-2021学年高一下学期期末考试化学试题
9 . 过硝酸钠(NaNO4)能与水发生反应:NaNO4+H2O=NaNO3+H2O2,下列说法错误的是
| A.过硝酸钠中N表现+5价 |
B.根据VSEPR理论可知: 中心N原子孤电子对数为1 中心N原子孤电子对数为1 |
| C.过硝酸钠中含有“-O-O-”结构 |
| D.H2O2与H2O都属于极性分子 |
您最近一年使用:0次
2020-08-11更新
|
81次组卷
|
2卷引用:山东省乳山市银滩高级中学2022-2023学年高一4月月考化学试题
名校
解题方法
10 . 下列各组微粒的空间构型相同的是( )
①NH3和H2O ② 和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥
和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥ 和
和 ⑦BF3和Al2Cl6
⑦BF3和Al2Cl6
①NH3和H2O ②
 和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥
和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥ 和
和 ⑦BF3和Al2Cl6
⑦BF3和Al2Cl6| A.全部 | B.除④⑥⑦以外 | C.③④⑤⑥ | D.②⑤⑥ |
您最近一年使用:0次
2020-07-02更新
|
1051次组卷
|
31卷引用:湖北省武汉市五校联合体2019-2020学年高一下学期期末考试化学试题
湖北省武汉市五校联合体2019-2020学年高一下学期期末考试化学试题2014-2015福建省福州市八县高二下学期联考化学试卷2015-2016学年河南省孟津一中高二上学期期末化学试卷2015-2016学年山西省大同一中高二下3月月考化学试卷2015-2016学年江苏省启东中学高二下第二次月考化学试卷2014-2015学年陕西西北大学附中高二下期末化学试卷2016-2017学年山西省大同市第一中学高二3月月考化学试卷河南省南阳市第一中学2016-2017学年高二下学期第一次月考(3月)化学试题安徽省合肥市第一中学2016-2017学年高二下学期期中考试化学试题山西省大同市第一中学2016-2017学年高二5月月考化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测山西省阳泉市第二中学2018-2019学年高二下学期期中考试化学试题辽宁省凌源市第二高级中学2019-2020学年高二第四次网上测试化学试题河北省沧州市盐山县盐山中学2019-2020学年高二下学期开学考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题辽宁师范大学附属中学2019-2020学年高二下学期期末考试化学试题山西省朔州市怀仁县大地学校2019-2020学年高二下学期期末考试化学试题(已下线)模块同步卷11 综合检测卷(基础卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)福建省建瓯市芝华中学2020-2021学年高二下学期第一阶段考试化学试题福建省龙岩市长汀县三级达标校2020-2021学年高二下学期期中考试化学试题新疆新源县第二中学2019-2020学年高二下学期期末考试化学试题新疆昌吉教育共同体2020-2021学年高二下学期期末质量检测化学试题河北省石家庄市第一中学2020-2021学年高二下学期学情反馈(一)化学试题广西蒙山县第一中学2018-2019学年高二下学期第二次月考化学试题(已下线)考向37 分子结构与性质-备战2022年高考化学一轮复习考点微专题四川省西昌市2020-2021学年高二下学期期中检测化学试题贵州省凯里学院附属中学2021-2022学年高二下学期3月月考化学试题山西省太原市英才学校2021-2022学年高二下学期线上期中化学试题重庆市璧山来凤中学2022-2023学年高二下学期第一次月考化学试题陕西省西安市周至县第四中学2022-2023学年高二下学期期末考试化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题



