19. 元素周期表中的VA、ⅥA、ⅦA族非金属元素的单质及其化合物用途非常广泛。回答下列问题:
I.(1)基态锑(Sb)原子价电子排布式为
____。[H
2F]
+[SbF
6]
-(氟酸锑)是一种超强酸,存在[H
2F]
+,该离子的VSEPR模型为
______II.已知: 含氧酸酸性强弱与非羟基氧原子数有关,几种含氧酸的分子式如下表:
| 酸的名称 | 次磷酸 | 亚磷酸 | 硼酸 | 亚砷酸 |
| 分子式 | H3PO2 | H3PO3 | H3BO3 | H3AsO3 |
| 类别 | 一元中强酸 | 二元中强酸 | 一元弱酸 | 三元弱酸 |
回答下列问题:
(2)H
3PO
2酸性比H
3PO
3弱的原因为
___________________________________, H
3PO
2和过量的NaOH溶液反应的化学方程式是:
_____________________,
(3)H
3PO
3和H
3AsO
3分子式相似,但它们的酸性差别很大,H
3PO
3是二元中强酸,H
3AsO
3既有弱酸性又有弱碱性。由此可推出它们的结构简式分别为
__________________,
______________________。
(4)硼酸(H
3BO
3)和四氟硼酸铵(NH
4BF
4)都有着重要的化工用途。
①H
3BO
3和NH
4BF
4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
_____(填元素符号)。
②H
3BO
3本身不能电离出H
+,在水中易结合一个OH
﹣生成[B(OH)
4]
﹣,而体现弱酸性,则H
3BO
3的电离方程式为
_____________________。
③NH
4BF
4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在
_______(填序号):
A.离子键
B.σ键
C.π键
D.配位键
E.范德华力
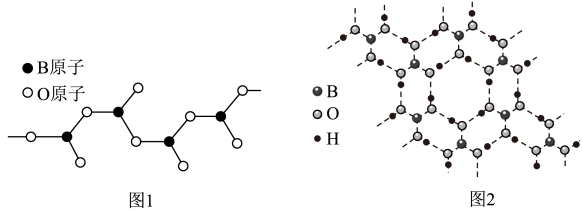
(5)图1表示多硼酸根离子的一种无限长的链式结构,其化学式可表示为
___________。
(6)硼酸晶体是片层结构,其中一层的结构如图2所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是
_________________________________。