解题方法
1 .  (直线形分子)、
(直线形分子)、 (平面三角形分子)、
(平面三角形分子)、 (正四面体型分子)都是非极性分子,
(正四面体型分子)都是非极性分子, (三角锥型分子)、
(三角锥型分子)、 (V形分子)、
(V形分子)、 (V形分子)都是极性分子。请分析什么样的
(V形分子)都是极性分子。请分析什么样的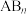 型分子为非极性分子
型分子为非极性分子_______ 。
 (直线形分子)、
(直线形分子)、 (平面三角形分子)、
(平面三角形分子)、 (正四面体型分子)都是非极性分子,
(正四面体型分子)都是非极性分子, (三角锥型分子)、
(三角锥型分子)、 (V形分子)、
(V形分子)、 (V形分子)都是极性分子。请分析什么样的
(V形分子)都是极性分子。请分析什么样的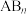 型分子为非极性分子
型分子为非极性分子
您最近一年使用:0次
2022-11-25更新
|
66次组卷
|
2卷引用:苏教2020版选择性必修2专题4第一单元 分子的空间结构课后习题
2 . 请用符号“>”“<”“=”填空:
(1)酸性:醋酸(CH3COOH)____ 丙酸(CH3CH2COOH)。
(2)键角:NH3____ SiH4。
(3)第一电离能:P____ S。
(4)电负性:S____ P。
(5)半径:Na+____ Al3+。
(1)酸性:醋酸(CH3COOH)
(2)键角:NH3
(3)第一电离能:P
(4)电负性:S
(5)半径:Na+
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
3 . 根据价层电子对互斥理论填空:
(1)OF2分子中,中心原子上的σ键电子对数为___________ ,孤电子对数为___________ ,价层电子对数为___________ ,中心原子的杂化方式为___________ 杂化,VSEPR模型为___________ ,分子的立体构型为___________ 。
(2)BF3分子中,中心原子上的σ键电子对数为___________ ,孤电子对数为___________ ,价层电子对数为___________ ,中心原子的杂化方式为___________ 杂化,VSEPR模型为___________ ,分子的立体构型为___________ 。
(1)OF2分子中,中心原子上的σ键电子对数为
(2)BF3分子中,中心原子上的σ键电子对数为
您最近一年使用:0次
解题方法
4 . 表中的中心原子A上没有孤电子对,运用价层电子对互斥模型,完成表中的空白:
 | 分子的空间结构 | 典型例子 |
 | ||
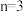 | ||
 |
您最近一年使用:0次
解题方法
5 . 分析乙烷、乙烯和乙炔的分子结构。其中的碳原子采取什么杂化轨道形成σ键_______ ?怎样理解乙烯中的双键和乙炔中的三键_______ ?乙炔加氢变成乙烯和乙烷,碳原子的杂化轨道发生什么变化_______ ?
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
6 . 磷酸根离子的空间构型为___________ ,其中P的价层电子对数为___________ 、杂化轨道类型为___________ 。
您最近一年使用:0次
2021-08-10更新
|
583次组卷
|
5卷引用:考点34 分子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点34 分子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考向37 分子结构与性质-备战2022年高考化学一轮复习考点微专题(已下线)考点47 分子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第一部分 二轮专题突破 专题20 原子结构、分子结构与性质的基础考查(选考)(已下线)02 常考题空2 立体构型及杂化类型的判断 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
解题方法
7 . 有以下物质:①HF;②Br2;③H2O;④N2;⑤C2H4;⑥C2H6;⑦H2;⑧H2O2;⑨HCHO
(1)只含有σ键的是___________ (填序号,下同);既含有σ键又含有π键的是___________ 。
(2)含有由两个原子的s轨道重叠形成σ键的物质是___________ 。
(3)写出以下分子或离子的空间构型:
NH3:___________ ,H2O:___________ ,SiH4:___________ ,BeCl2:___________ ,CO2:___________ 。
(1)只含有σ键的是
(2)含有由两个原子的s轨道重叠形成σ键的物质是
(3)写出以下分子或离子的空间构型:
NH3:
您最近一年使用:0次
2021-05-28更新
|
272次组卷
|
4卷引用:河北省石家庄卓越联盟2020-2021学年高二3月月考化学试题
河北省石家庄卓越联盟2020-2021学年高二3月月考化学试题(已下线)第2.2.1讲 分子结构的测定和多样性 价层电子对互斥模型-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)(已下线)第二章 分子结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)上海市华东师范大学附属东昌中学2023-2024学年高三上学期第四次测试化学试卷
名校
解题方法
8 . 原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:___ 。
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:____ 。其正三价离子的未成对电子数为____
(3)写出3p轨道上有2个未成对电子的元素的符号:____ 。
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为___ 。
(5)基态原子的4s能级中只有1个电子的元素共有___ 种
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为___ ,属于____ 区元素;[Cu(NH3)4]SO4中所含的化学键有___ ,,[Cu(NH3)4]SO4的外界离子的空间构型为____ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)写出原子序数最小的第Ⅷ族元素原子的核外的价电子排布图:
(3)写出3p轨道上有2个未成对电子的元素的符号:
(4)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
(5)基态原子的4s能级中只有1个电子的元素共有
(6)元素基态原子的M层全充满,N层有且只有一个未成对电子,其基态原子的电子排布式为
您最近一年使用:0次
解题方法
9 . 现有下列微粒:①CH4;②CH2=CH2;③CH≡CH;④NH3;⑤NH ;⑥BF3;⑦P4;⑧H2O;⑨H2O2.填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2.填写下列空白(填序号):
(1)空间结构为正四面体形的是____________________ .
(2)中心原子轨道为sp3杂化的是___________ ,为sp2杂化的是_________ ,为sp杂化的是______ .
(3)所有原子共平面(含共直线)的是________________ ,共直线的是_______________ .
(4)互为等电子体的一组是__________________ .
 ;⑥BF3;⑦P4;⑧H2O;⑨H2O2.填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2.填写下列空白(填序号):(1)空间结构为正四面体形的是
(2)中心原子轨道为sp3杂化的是
(3)所有原子共平面(含共直线)的是
(4)互为等电子体的一组是
您最近一年使用:0次
解题方法
10 . 请回答下列问题:
(1) 中含有化学键的类型为
中含有化学键的类型为_______ 。
(2) 由
由 和
和 构成,
构成, 的空间结构是
的空间结构是_______ ,根据化合物 判断,
判断, 、B、H的电负性由大到小的顺序为
、B、H的电负性由大到小的顺序为_______ 。
(1)
 中含有化学键的类型为
中含有化学键的类型为(2)
 由
由 和
和 构成,
构成, 的空间结构是
的空间结构是 判断,
判断, 、B、H的电负性由大到小的顺序为
、B、H的电负性由大到小的顺序为
您最近一年使用:0次



