1 . 铁及其化合物在生活中用途广泛,绿矾(FeSO4·7H2O)是一种常见的中草药成分,失水后可转为FeSO4·H2O,与FeS2可联合制备铁粉精(FexOy)和H2SO4。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为_________ 。
(2)比较 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:_________ 。
(3) 与
与 和
和 之间的作用力分别为
之间的作用力分别为_________ 。
ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。
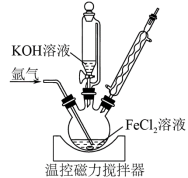
①三颈烧瓶发生反应的离子方程式为_________ 。
②检验反应是否进行完全的操作是_________ 。
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是_________ 。
②计算实验所得产品的产率_________ 。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为
(2)比较
 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:(3)
 与
与 和
和 之间的作用力分别为
之间的作用力分别为ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。

①三颈烧瓶发生反应的离子方程式为
②检验反应是否进行完全的操作是
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是
②计算实验所得产品的产率
您最近一年使用:0次
解题方法
2 . 下列分子或离子大的空间结构相同的是
| A.BeCl2和O3 | B.SO3和PCl3 | C. 和BH 和BH | D. 和 和 |
您最近一年使用:0次
3 . 下列各组物质性质的比较,结论正确的是
A.分子的极性: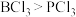 | B.沸点:邻羟基苯甲酸<对羟基苯甲酸 |
C.熔点: | D.硬度:C(金刚石)<SiC |
您最近一年使用:0次
名校
解题方法
4 . 某小组同学用图装置 略去加热仪器等
略去加热仪器等 制备
制备 。
。
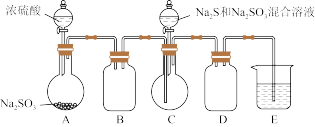
已知烧瓶 中发生反应如下:
中发生反应如下:
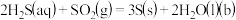

下列说法正确的是
 略去加热仪器等
略去加热仪器等 制备
制备 。
。
已知烧瓶
 中发生反应如下:
中发生反应如下:
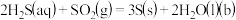

下列说法正确的是
A. 的稳定性比 的稳定性比 强 强 | B. 为 为 形分子 形分子 |
C. 与 与 的反应体现 的反应体现 的还原性 的还原性 | D. 、 、 的中心原子的轨道杂化类型为 的中心原子的轨道杂化类型为 |
您最近一年使用:0次
2022-09-10更新
|
169次组卷
|
3卷引用:江苏省南通市八校2022-2023学年高三上学期期初联考化学试题
5 . 下列说法正确的是
| A.HF、HCl、HBr的沸点依次增大 | B.H原子的1s电子云轮廓图为球形 |
| C.CH2Cl2分子中的碳原子为手性碳原子 | D.H2O分子的VSEPR模型是平面三角形 |
您最近一年使用:0次
名校
解题方法
6 . 下列粒子的空间构型不同于其他三个的是
A.气态 | B.气态 | C. | D. |
您最近一年使用:0次
2022-09-08更新
|
506次组卷
|
4卷引用:北京市第十一中学2022-2023学年高三上学期检测化学试题
名校
解题方法
7 . 下列说法正确的是
A. 的 的 模型为四面体形,属于极性分子 模型为四面体形,属于极性分子 |
B. 中σ键类型为“头碰头”形式形成的 中σ键类型为“头碰头”形式形成的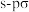 键和 键和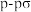 键 键 |
C. 的空间构型为正四面体形,键角是 的空间构型为正四面体形,键角是 |
D.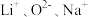 的离子半径依次增大 的离子半径依次增大 |
您最近一年使用:0次
2022-09-05更新
|
277次组卷
|
4卷引用:重庆市育才中学校2023届高三上学期开学测试化学试题
8 . 配合物 可用于蚀刻铜,蚀刻后的产物
可用于蚀刻铜,蚀刻后的产物 可在氧气中再生,再生反应为
可在氧气中再生,再生反应为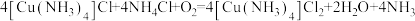 。下列说法正确的是
。下列说法正确的是
 可用于蚀刻铜,蚀刻后的产物
可用于蚀刻铜,蚀刻后的产物 可在氧气中再生,再生反应为
可在氧气中再生,再生反应为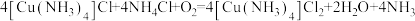 。下列说法正确的是
。下列说法正确的是A.基态Cu的电子排布式为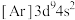 | B. 属于共价化合物 属于共价化合物 |
C. 的空间构型为三角锥形 的空间构型为三角锥形 | D. 中含 中含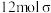 键 键 |
您最近一年使用:0次
名校
解题方法
9 . 常见的太阳能电池有硅太阳能电池、镓(Ga)砷(As)太阳能电池及铜铟镓硒薄膜太阳能电池等。下列有关它们的化合物的问题,请回答:
(1)基态Ga原子的电子排布式为_______ ;H2O的沸点高于 H2Se的沸点(-42℃),其原因是_______ 。
(2)Na3AsO4中阴离子的空间构型为_______ ,As 原子采取_______ 杂化。
(3)晶体Si、SiC都属于原子晶体,请写出它们的熔点从高到低的顺序排列_______ 。
(4)银与铜位于同一副族。氟化银具有氯化钠型结构,其中的阴离子采用面心立方最密堆积方式,氯化钠的晶胞结构如图所示。则 Ag+周围等距离且最近的F-在空间围成的几何构型为_______ ,已知氟化银的密度为 dg·cm-3,则氟化银晶胞的晶胞参数为_______ nm(不必简化)。

(1)基态Ga原子的电子排布式为
(2)Na3AsO4中阴离子的空间构型为
(3)晶体Si、SiC都属于原子晶体,请写出它们的熔点从高到低的顺序排列
(4)银与铜位于同一副族。氟化银具有氯化钠型结构,其中的阴离子采用面心立方最密堆积方式,氯化钠的晶胞结构如图所示。则 Ag+周围等距离且最近的F-在空间围成的几何构型为

您最近一年使用:0次
10 .  是一种重要的工业原料,常用作媒染剂等。已知
是一种重要的工业原料,常用作媒染剂等。已知 常温下是无色液体,在潮湿空气中易水解,熔点
常温下是无色液体,在潮湿空气中易水解,熔点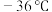 ,沸点
,沸点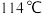 。工业上制备
。工业上制备 的工艺流程如图:
的工艺流程如图:
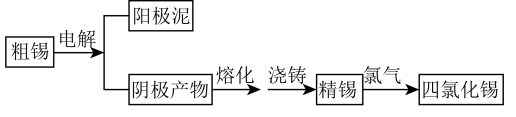
请回答下列问题;
(1)粗锡电解精炼时,常用硅氟酸 和硅氟酸亚锡
和硅氟酸亚锡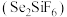 为电解液。已知
为电解液。已知 为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为
为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为___________ 。阴极的电极反应式为___________ ,根据价层电子对互斥理论和杂化轨道理论,判断 离子的空间构型是
离子的空间构型是___________ ,硅的杂化类型是___________ 。
(2)某同学模拟工业制法设计了由 与
与 反应制取
反应制取 的实验装置:
的实验装置:
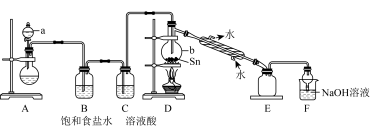
①a中浓盐酸与烧瓶内固体反应生成 ,则烧瓶内固体可以选用
,则烧瓶内固体可以选用___________ ,仪器b的名称为___________ 。
②装置D的主要缺点是___________ ,除此之外,整套装置还有的缺点是___________ 。
③制取 中可能会产生少量
中可能会产生少量 ,为测定产品中
,为测定产品中 的含量,可选用重铬酸钾标准液滴定,准确称取该样品
的含量,可选用重铬酸钾标准液滴定,准确称取该样品 放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成
放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成 溶液,取
溶液,取 于锥形瓶中,用
于锥形瓶中,用 重铬酸钾标准溶液滴定至终点,消耗标准液
重铬酸钾标准溶液滴定至终点,消耗标准液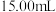 ,则产品中
,则产品中 的含量为
的含量为___________  (用含m的代数式表示),测定
(用含m的代数式表示),测定 含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是
含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是___________ (用离子方程式表示)。
 是一种重要的工业原料,常用作媒染剂等。已知
是一种重要的工业原料,常用作媒染剂等。已知 常温下是无色液体,在潮湿空气中易水解,熔点
常温下是无色液体,在潮湿空气中易水解,熔点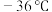 ,沸点
,沸点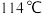 。工业上制备
。工业上制备 的工艺流程如图:
的工艺流程如图:
请回答下列问题;
(1)粗锡电解精炼时,常用硅氟酸
 和硅氟酸亚锡
和硅氟酸亚锡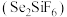 为电解液。已知
为电解液。已知 为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为
为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为 离子的空间构型是
离子的空间构型是(2)某同学模拟工业制法设计了由
 与
与 反应制取
反应制取 的实验装置:
的实验装置:
①a中浓盐酸与烧瓶内固体反应生成
 ,则烧瓶内固体可以选用
,则烧瓶内固体可以选用②装置D的主要缺点是
③制取
 中可能会产生少量
中可能会产生少量 ,为测定产品中
,为测定产品中 的含量,可选用重铬酸钾标准液滴定,准确称取该样品
的含量,可选用重铬酸钾标准液滴定,准确称取该样品 放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成
放于烧杯中,用少量浓盐酸溶解,加入过量的氯化铁溶液,再加水稀释,配制成 溶液,取
溶液,取 于锥形瓶中,用
于锥形瓶中,用 重铬酸钾标准溶液滴定至终点,消耗标准液
重铬酸钾标准溶液滴定至终点,消耗标准液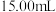 ,则产品中
,则产品中 的含量为
的含量为 (用含m的代数式表示),测定
(用含m的代数式表示),测定 含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是
含量会随在烧杯中配制时间的增加而逐渐增大,其原因可能是
您最近一年使用:0次



