23-24高二上·广东深圳·期末
名校
1 . 化合物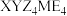 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为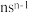 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是
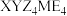 可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布,仅有Y和M同族,且Y的原子半径小于M。Y的基态原子价层p轨道半充满,X的基态原子价层电子排布式为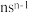 ,X与M同周期,E在地壳中含量最多。下列说法正确的是
,X与M同周期,E在地壳中含量最多。下列说法正确的是A.元素电负性: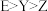 | B.简单氢化物沸点: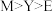 |
C.第一电离能: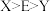 | D.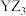 和 和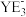 空间结构均为三角锥形 空间结构均为三角锥形 |
您最近一年使用:0次
名校
解题方法
2 . 用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是
A.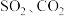 都是直线形的分子 都是直线形的分子 |
B. 键角为 键角为 , , 键角为 键角为 |
C. 都是三角锥形的分子 都是三角锥形的分子 |
D.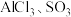 都是平面三角形的粒子 都是平面三角形的粒子 |
您最近一年使用:0次
名校
解题方法
3 . 下列粒子的VSEPR模型为四面体、且其空间结构为V形的是
| A.NO2 | B. | C.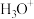 | D.H2O |
您最近一年使用:0次
2023-12-06更新
|
255次组卷
|
3卷引用:广东省东莞市第一中学2023-2024学年高二上学期期中考试化学试卷
名校
解题方法
4 . 有X、Y两种活性反应中间体微粒,均含有1个碳原子和3个氢原子,其球棍模型如图所示:
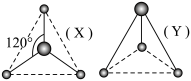
下列说法错误的是

下列说法错误的是
A.X的组成为CH | B.Y的组成为CH |
| C.X的价层电子对数为3 | D.Y中键角大于120° |
您最近一年使用:0次
2023-08-11更新
|
95次组卷
|
2卷引用:广东省江门市第一中学2023-2024学年高二上学期第一次段考化学试题
名校
解题方法
5 . 铜的单质及其化合物在工农业、国防、科技等领域具有广泛应用。回答下列问题:
(1)基态Cu+的价层电子排布式为_______ 。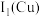
_______ (填“ ”或“
”或“ ”)
”)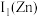 ,原因是
,原因是_______ 。
(2)研究发现,阳离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是_______ 。
(3)合成氨工业中,铜(I)氨溶液常用于除去原料气(N2和H2等)中少量的CO,发生的化学反应为: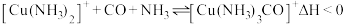 。
。
①NH3分子中N原子的杂化轨道类型是_______ ,NH3和[Cu(NH3)4]2+中H-N-H键角的大小:NH3_______ [Cu(NH3)4]2+ (填“ ”或“
”或“ ”)。
”)。
②铜(Ⅰ)氨液吸收CO适宜的生产条件是_______ (填序号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③[Cu(NH3)3CO]+配离子中配体是_______ 。
(4)CuCl2与乙二胺(H2NCH2CH2NH2)可形成配离子[Cu(En)2]2+ (En是乙二胺的简写),其结构简式如图所示:
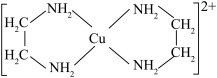
①H2NCH2CH2NH2 (乙二胺)和N(CH3)3(三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是_______ 。
②配合物[Cu(En)2]Cl2中不存在的作用力类型有_______ (填选项字母)。
A.配位键 B.极性键 C.离子键 D.非极性键 E.范德华力 F.金属键
(5)金属合金MgCux的结构可看作以Cu4四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。

①
_______ 。
②若Mg原子A的原子坐标为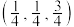 ,则C的原子坐标为
,则C的原子坐标为_______ 。
③晶胞参数为 ,则AB原子之间的距离为
,则AB原子之间的距离为_______ nm。
(1)基态Cu+的价层电子排布式为
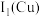
 ”或“
”或“ ”)
”)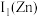 ,原因是
,原因是(2)研究发现,阳离子的颜色与未成对电子数有关。例如:Cu2+、Fe2+、Fe3+等。Cu+呈无色,其原因是
(3)合成氨工业中,铜(I)氨溶液常用于除去原料气(N2和H2等)中少量的CO,发生的化学反应为:
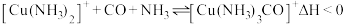 。
。①NH3分子中N原子的杂化轨道类型是
 ”或“
”或“ ”)。
”)。②铜(Ⅰ)氨液吸收CO适宜的生产条件是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
③[Cu(NH3)3CO]+配离子中配体是
(4)CuCl2与乙二胺(H2NCH2CH2NH2)可形成配离子[Cu(En)2]2+ (En是乙二胺的简写),其结构简式如图所示:

①H2NCH2CH2NH2 (乙二胺)和N(CH3)3(三甲胺)均属于胺,二者相对分子质量相近,但乙二胺的沸点比三甲胺的高得多,原因是
②配合物[Cu(En)2]Cl2中不存在的作用力类型有
A.配位键 B.极性键 C.离子键 D.非极性键 E.范德华力 F.金属键
(5)金属合金MgCux的结构可看作以Cu4四面体(相互共用顶点)替换立方金刚石结构中的碳原子,形成三维骨架,在晶胞空隙处,有序地放置Mg原子(四面体的4个顶点代表Cu原子,圆球代表Mg原子),结构如图所示。

①

②若Mg原子A的原子坐标为
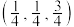 ,则C的原子坐标为
,则C的原子坐标为③晶胞参数为
 ,则AB原子之间的距离为
,则AB原子之间的距离为
您最近一年使用:0次
6 . 卤化物在生产、生活和科研中应用广泛。请回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为___________ 。
(2)四氟乙烯( )分子中,
)分子中, 键与
键与 键的数目比为
键的数目比为___________ ,C的杂化轨道类型为___________ 。“塑料王”——聚四氟乙烯,其化学稳定性高于聚乙烯,从化学键的角度解释原因___________ 。
(3) 主要用于火箭工程液体助燃剂,其分子的空间构型为
主要用于火箭工程液体助燃剂,其分子的空间构型为___________ ,该分子为___________ (填“极性”或“非极性”)分子。
(4)三种卤化物 、
、 、
、 的熔点由高到低的顺序是
的熔点由高到低的顺序是___________ 。
(5) 在
在 的催化下,可与
的催化下,可与 反应得到
反应得到 。比较酸性强弱:
。比较酸性强弱:
___________  填“>”或“<”)。
填“>”或“<”)。
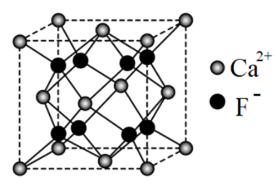
(6)萤石是自然界中常见的含氟矿物,其主要成分晶体的一种立方晶胞结构如图所示。该晶胞的化学式应为___________ 。若该立方晶胞的密度为 ,氟化钙的摩尔质量为
,氟化钙的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞边长为
,则晶胞边长为___________ 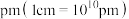 。
。
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为(2)四氟乙烯(
 )分子中,
)分子中, 键与
键与 键的数目比为
键的数目比为(3)
 主要用于火箭工程液体助燃剂,其分子的空间构型为
主要用于火箭工程液体助燃剂,其分子的空间构型为(4)三种卤化物
 、
、 、
、 的熔点由高到低的顺序是
的熔点由高到低的顺序是(5)
 在
在 的催化下,可与
的催化下,可与 反应得到
反应得到 。比较酸性强弱:
。比较酸性强弱:
 填“>”或“<”)。
填“>”或“<”)。(6)萤石是自然界中常见的含氟矿物,其主要成分晶体的一种立方晶胞结构如图所示。该晶胞的化学式应为
 ,氟化钙的摩尔质量为
,氟化钙的摩尔质量为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞边长为
,则晶胞边长为 。
。
您最近一年使用:0次
7 . 亚铁氰化钾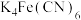 俗名黄血盐,在烧制青花瓷时用于绘画。制备方法为:
俗名黄血盐,在烧制青花瓷时用于绘画。制备方法为: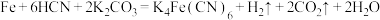 。设
。设 为阿伏伽德罗常数,下列说法正确的是
为阿伏伽德罗常数,下列说法正确的是
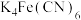 俗名黄血盐,在烧制青花瓷时用于绘画。制备方法为:
俗名黄血盐,在烧制青花瓷时用于绘画。制备方法为: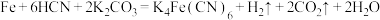 。设
。设 为阿伏伽德罗常数,下列说法正确的是
为阿伏伽德罗常数,下列说法正确的是A.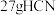 分子中含有 分子中含有 键数目为 键数目为 |
B. 中阴离子的空间结构为三角锥形 中阴离子的空间结构为三角锥形 |
C.配合物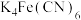 的中心离子配位数为6 的中心离子配位数为6 |
D. 的VSEPR模型为直线形 的VSEPR模型为直线形 |
您最近一年使用:0次
8 . 下列化学用语或图示表达正确的是
A.氨基的电子式: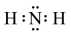 | B. 的VSEPR模型: 的VSEPR模型: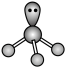 |
C.苯的实验式: | D.1—丙醇的结构简式: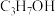 |
您最近一年使用:0次
名校
解题方法
9 . 三溴化砷(AsBr3)常应用于医药和化学分析领域。下列说法正确的是
| A.该分子含非极性共价键 | B.中心原子采取sp3杂化 |
| C.键角等于120° | D.空间结构为平面三角形 |
您最近一年使用:0次
10 . 根据价层电子对互斥模型,判断下列分子或离子的空间构型为三角锥形的是
| A.H2O | B. | C.BF3 | D.PCl3 |
您最近一年使用:0次



