名校
解题方法
1 . 溶剂是影响化学反应的重要因素之一,当反应在无溶剂条件下进行时,具有操作简单、反应时间短、无溶剂浪费且遵循绿色化学的原理等独特优点。因此,无溶剂不对称催化已成为合成化学中的重要课题。化合物H是一种手性有机催化剂,可无溶剂催化如下迈克尔加成反应(Michael addition reaction): 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
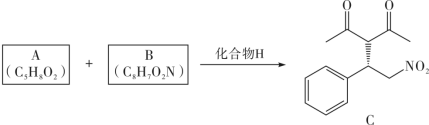
(1)A的化学名称为___________ ;B为反式结构,其结构简式为___________ 。
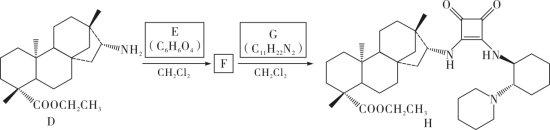
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式___________ ,该反应类型为___________ 。
(3)G的同分异构体中,含有碳、氮环状骨架为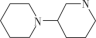 的共有
的共有___________ 种(不含立体异构)。
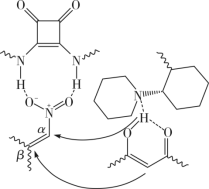
(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(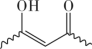 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示, 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的___________ (填标号)。
a.离子键 b.共价键 c.配位键 d.氢键___________ 。
(5)如果要合成H的类似物H′(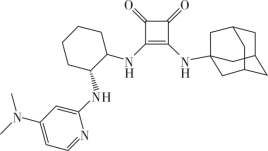 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式___________ 。以甲苯为溶剂,H′可催化A与B的迈克尔加成反应,产物主要是___________ (填“C”“C的手性异构体”或“C及其手性异构体各占50%”),判断理由是___________ 。
化合物H的合成路线如下( 、
、 分别表示由纸面向内、向外伸展的共价键):
分别表示由纸面向内、向外伸展的共价键):
 、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体
、R(大)、R′(小)顺时针排列的面称为Re-face(下图左),逆时针排列的面称为Si-face(下图右),—R″进攻不同面β-碳的产物互为手性异构体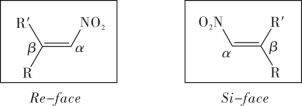
(1)A的化学名称为
(2)已知E的核磁共振氢谱只有一个吸收峰。写出D(用
 简化表示)与E反应的化学方程式
简化表示)与E反应的化学方程式(3)G的同分异构体中,含有碳、氮环状骨架为
 的共有
的共有(4)推测H催化A和B反应的部分机理可能为:A异构化为烯醇(
 ),再和B与催化剂H结合(如图所示,
),再和B与催化剂H结合(如图所示, 表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的
表示链的延长)。反应物与催化剂H结合的作用力主要是下列中的a.离子键 b.共价键 c.配位键 d.氢键
(5)如果要合成H的类似物H′(
 ),参照上述合成路线,写出相应的G′的结构简式
),参照上述合成路线,写出相应的G′的结构简式
您最近一年使用:0次
名校
解题方法
2 . 下列分子或离子的空间结构和中心原子的杂化方式均正确的是
A. 平面三角形 平面三角形  杂化 杂化 | B. 平面三角形 平面三角形  杂化 杂化 |
C. V形 V形  杂化 杂化 | D. 三角锥形 三角锥形  杂化 杂化 |
您最近一年使用:0次
2024-04-21更新
|
243次组卷
|
7卷引用:天津市静海区四校2022-2023学年高二下学期3月阶段性检测化学试题
天津市静海区四校2022-2023学年高二下学期3月阶段性检测化学试题(已下线)期中模拟预测卷02(测试范围:选择性必修2+选择性必修3第1章)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)天津市第三中学2022-2023学年高二下学期期中质量检测化学试题四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题陕西省渭南市华州区咸林中学2023-2024学年高二下学期第一次月考化学试题浙江省舟山中学2023-2024学年高二下学期4月月考化学试题福建省南安市侨光中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
3 . 实验室可由Ca(OH)2与NH4Cl反应制备NH3,同时生成CaCl2和H2O。下列说法正确的是
A.NH4Cl的电子式为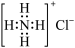 | B.H2O的空间构型为直线形 |
| C.CaCl2中只含有离子键 | D.键角大小: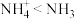 |
您最近一年使用:0次
解题方法
4 . 下列化学用语表达正确的是
A.基态 离子的价电子排布图为 离子的价电子排布图为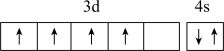 |
B.N,N-二甲基苯甲酰胺的结构简式: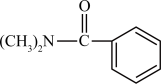 |
C.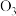 分子的球棍模型: 分子的球棍模型: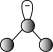 |
D. 的电子式: 的电子式: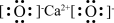 |
您最近一年使用:0次
2024-03-29更新
|
968次组卷
|
4卷引用:湖北省2024届高三十一校第二次联考化学试题
湖北省2024届高三十一校第二次联考化学试题2024届湖北省十一校高三下学期第二次联考化学试卷 (已下线)题型2 有关化学用语的正误判断(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)化学(新七省高考“15+4”)-2024年高考押题预测卷
名校
解题方法
5 . 实验室中常用NaOH对NO、NO2的尾气进行吸收,反应方程式NO+NO2+2NaOH=2NaNO2+H2O,下列说法错误的是
| A.NaNO2中既有共价键也有离子键 |
B.氮原子的价层电子轨道表示式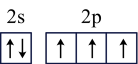 |
| C.水的VSEPR模型为四面体形 |
| D.NO、NO2均为酸性氧化物 |
您最近一年使用:0次
解题方法
6 . 从微粒结构角度分析,下列说法正确的是
A.三氧化硫有单分子气体和三聚分子固体(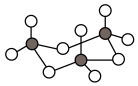 )两种存在形式,两种形式中S原子的杂化轨道类型相同 )两种存在形式,两种形式中S原子的杂化轨道类型相同 |
B. 中Al原子采用 中Al原子采用 杂化, 杂化, 离子的空间构型为平面正方形 离子的空间构型为平面正方形 |
C.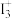 的空间结构为V形,中心原子的杂化方式为 的空间结构为V形,中心原子的杂化方式为 |
D. ( (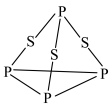 )中S和P原子最外层均满足8电子稳定结构 )中S和P原子最外层均满足8电子稳定结构 |
您最近一年使用:0次
2024-03-14更新
|
80次组卷
|
2卷引用:海南省海口中学2023-2024学年高二上学期12月月考化学试题
解题方法
7 . 金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛在周期表中的位置________ ,Ti2+电子占据的最高能层的电子排布式为_________ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是___________ ,第一电离能介于Al、P之间的第三周期元素为___________ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为___________ ,B原子的杂化方式是___________ ,其中的BH 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有___________ (填序号)
①σ键②π键③氢键④配位键⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为___________ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
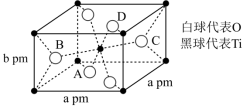
(1)钛在周期表中的位置
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为
 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有①σ键②π键③氢键④配位键⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近一年使用:0次
8 . 根据要求填空:
(1)红宝石是刚玉的一种,主要成分为氧化铝,因含微量杂质元素铬(Cr)而呈红色。基态铬原子的价层电子排布式为___________ 。
(2)铜催化烯烃确化反应时会产生 ,键角:
,键角:
___________ 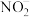 (填“<”或“=”或“>”)
(填“<”或“=”或“>”)
(3)①乙酸;②丙酸;③二氯乙酸的酸性由强到弱的顺序为___________ (填序号)。
(4)有机物吡啶(C5H5N),结构简式为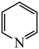 ,其中N的杂化方式为
,其中N的杂化方式为___________ ,吡啶在水中的溶解度远大于在苯中的溶解度,可能原因是:
①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②___________ 。
(1)红宝石是刚玉的一种,主要成分为氧化铝,因含微量杂质元素铬(Cr)而呈红色。基态铬原子的价层电子排布式为
(2)铜催化烯烃确化反应时会产生
 ,键角:
,键角:
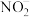 (填“<”或“=”或“>”)
(填“<”或“=”或“>”)(3)①乙酸;②丙酸;③二氯乙酸的酸性由强到弱的顺序为
(4)有机物吡啶(C5H5N),结构简式为
 ,其中N的杂化方式为
,其中N的杂化方式为①吡啶和水均为极性分子,相似相溶,而苯为非极性分子;
②
您最近一年使用:0次
名校
9 . 类推是化学学习和研究中常用的思维方法。下列类推正确的是
A. 为直线形分子,则 为直线形分子,则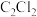 也为直线形分子 也为直线形分子 |
| B.N原子之间可以形成N=N,则P原子之间也可形成P=P |
C. 分子的空间结构为V形,则 分子的空间结构为V形,则 的VSEPR模型也是V形 的VSEPR模型也是V形 |
D.基态V的价层电子排布式为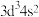 ,基态Cr的价层电子排布式为 ,基态Cr的价层电子排布式为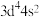 |
您最近一年使用:0次
2024-03-02更新
|
276次组卷
|
2卷引用:辽宁省朝阳市建平县实验中学2023-2024学年高二上学期期末化学试题
名校
解题方法
10 . 根据价层电子对互斥模型,判断下列分子或离子的空间结构正确的是
| 编号 | 分子式 | 价层电子对互斥模型 | 分子或离子的空间结构 |
| ① | AsCl3 | 四面体形 | 三角锥形 |
| ② | HCHO | 平面三角形 | 三角锥形 |
| ③ | NF3 | 四面体形 | 平面三角形 |
| ④ |  | 正四面体形 | 正四面体形 |
| A.①② | B.①④ | C.②④ | D.②③ |
您最近一年使用:0次
2024-02-29更新
|
351次组卷
|
4卷引用:新疆阿克苏市实验中学2022-2023学年高二下学期第二次月考化学试题



