1 . 樱黄素(乙)具有抗过敏、抗炎、抗肿瘤和保护心脑血管等多方面生物活性。以金雀异黄酮(甲)为原料,经碘甲烷甲基化合成樱黄素的反应如下,下列说法正确的是

| A.甲、乙所含官能团种类不相同 |
B.乙分子中所有原子杂化类型均为 |
C.一定条件下,甲与足量的 加成产物的分子中有8个手性碳原子 加成产物的分子中有8个手性碳原子 |
D.甲、乙既能与 溶液反应,又能与 溶液反应,又能与 溶液反应 溶液反应 |
您最近一年使用:0次
2 . 淀粉-聚丙烯酸钠高吸水性树脂具有强大的吸水和保水能力,也是可生物降解的绿色材料。一种合成聚丙烯酸钠的路线如下图所示,下列有关说法不正确的是
CH3CH2COOH CH3CHBrCOOH
CH3CHBrCOOH CH2=CHCOONa
CH2=CHCOONa

| A.高吸水性树脂结构中有强亲水基团 |
B.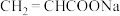 中C原子杂化轨道类型有2种 中C原子杂化轨道类型有2种 |
| C.反应①、③分别为取代反应、加聚反应 |
| D.反应②的条件为NaOH的乙醇溶液、加热 |
您最近一年使用:0次
解题方法
3 . 我国科学家研究发现,常温常压下,铁基离子液体 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有___________ 。在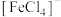 中,配体为
中,配体为___________ ,配位数为___________ 。
(2)在一定条件下 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为___________ , 的电子式为
的电子式为___________ 。
(3) 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。
①科学家通过最常用的___________ 实验测定了物质X的晶体结构,其晶胞如图b所示(未表示 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。___________ 。
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为___________ 。
④已知物质X的摩尔质量为 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为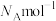 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为___________ nm,晶体的密度为___________  。
。
 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。
 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有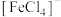 中,配体为
中,配体为(2)在一定条件下
 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为 的电子式为
的电子式为(3)
 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。①科学家通过最常用的
 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为
④已知物质X的摩尔质量为
 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为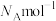 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为 。
。
您最近一年使用:0次
4 . 2022年诺贝尔化学奖授予了点击化学领域的三位科学家。一价铜催化的叠氮化物-炔烃环加成反应可谓点击化学中的第一个经典之作,其中 代表烃基,含氮五元环为平面结构,催化剂
代表烃基,含氮五元环为平面结构,催化剂 的结构属立方晶系,晶胞如图所示,下列说法正确的是
的结构属立方晶系,晶胞如图所示,下列说法正确的是

 代表烃基,含氮五元环为平面结构,催化剂
代表烃基,含氮五元环为平面结构,催化剂 的结构属立方晶系,晶胞如图所示,下列说法正确的是
的结构属立方晶系,晶胞如图所示,下列说法正确的是
A.基态 的价电子排布图为 的价电子排布图为 |
B.五元环中 和 和 原子轨道的杂化类型相同 原子轨道的杂化类型相同 |
C. 的第一电离能从大到小的顺序是 的第一电离能从大到小的顺序是 |
D.若晶胞参数为 ,则距离最近的两个 ,则距离最近的两个 之间的距离为 之间的距离为 |
您最近一年使用:0次
名校
解题方法
5 . 一种可吸附甲醇的材料,其化学式为 ,部分晶体结构如图所示,其中
,部分晶体结构如图所示,其中 为平面结构。下列说法不正确的是
为平面结构。下列说法不正确的是
 ,部分晶体结构如图所示,其中
,部分晶体结构如图所示,其中 为平面结构。下列说法不正确的是
为平面结构。下列说法不正确的是
| A.该晶体为离子晶体 | B.元素的电负性: |
C.基态原子未成对电子数: | D.晶体中所有C原子轨道的杂化类型相同 |
您最近一年使用:0次
6 . 苏轼的《格物粗谈》有如下记载:“红柿摘下末熟,每篮用木瓜三枚放入,得气即发,并无涩味。”文中的“气”实指一种常见的烃,关于该烃分子的说法错误的是
A.碳原子均采取 杂化 杂化 | B.所有原子在同一平面上 |
| C.能使酸性高锰酸钾溶液褪色 | D.结构简式为: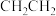 |
您最近一年使用:0次
2023-07-15更新
|
109次组卷
|
4卷引用:山西省应县第四中学校2022-2023学年高二下学期7月期末考试化学试题
山西省应县第四中学校2022-2023学年高二下学期7月期末考试化学试题吉林省普通高中友好学校联合体2022-2023学年高二下学期第三十六届基础年段期末联考化学试题黑龙江省哈尔滨市宾县第二中学2023-2024学年高二上学期期末考试化学试题 (已下线)猜想05 烃 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
解题方法
7 . 山梨糖醇主要用作甜味剂,甜度约为蔗糖的一半,热值与蔗糖相近。山梨糖醇的结构如图,下列有关说法错误的是


A. 山梨糖醇与足量Na反应产生 山梨糖醇与足量Na反应产生 | B.山梨糖醇中C原子的杂化方式均为 |
| C.山梨糖醇中所有原子在同一平面上 | D.山梨糖醇能催化氧化成含酮羰基的物质 |
您最近一年使用:0次
名校
解题方法
8 . 中科院大连化学物理研究所科学家用Ni-BaH3/Al2O3、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《Nature Energy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸中C原子的杂化方式为___________ ,晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
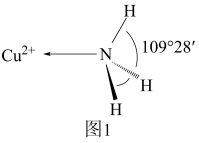
(3)NH3分子中的键角为107°,但在 中NH3分子的键角如图1所示,导致这种变化的原因是
中NH3分子的键角如图1所示,导致这种变化的原因是___________ 。
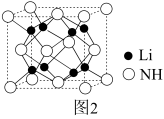
(4)亚氨基锂(Li2NH)是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图2所示,若晶胞参数为dpm,密度为ρg/cm3,则阿伏加德罗常数
___________  (列出表达式)。
(列出表达式)。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸中C原子的杂化方式为
(3)NH3分子中的键角为107°,但在
 中NH3分子的键角如图1所示,导致这种变化的原因是
中NH3分子的键角如图1所示,导致这种变化的原因是
(4)亚氨基锂(Li2NH)是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图2所示,若晶胞参数为dpm,密度为ρg/cm3,则阿伏加德罗常数

 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
2023-07-07更新
|
84次组卷
|
3卷引用:山西省怀仁市第一中学校2022-2023学年高二下学期期末考试理综化学试题
9 . 氨基吡啶与铜等金属离子所形成的配合物具备良好的磁学性质,某氨基吡啶衍生物铜配合物X的结构简式如图所示。
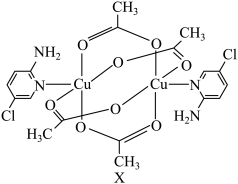
(1)基态氯原子的价层电子排布图为______ ;下列不同状态的氮原子中,能量最高的是______ (填字母)。
A. B.
B.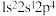 C.
C.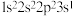 D.
D.
(2)C、N、O元素原子的电负性由大到小的顺序为______ 。
(3)X中 的配位数是
的配位数是______ ;铜元素有不同价态氧化物,高温下稳定性
______ CuO(填“大于”或“小于”),从离子的电子层结构角度分析,主要原因是______ 。
(4)X中N原子的杂化方式为______ 。
(5)下列关于X的说法中不正确的是______(填字母)。

(1)基态氯原子的价层电子排布图为
A.
 B.
B.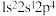 C.
C.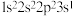 D.
D.
(2)C、N、O元素原子的电负性由大到小的顺序为
(3)X中
 的配位数是
的配位数是
(4)X中N原子的杂化方式为
(5)下列关于X的说法中不正确的是______(填字母)。
A.存在大π键 |
| B.存在氢键、配位键等化学键 |
| C.碳、氧原子间形成的σ键和π键个数比为2∶1 |
| D.铜属于d区元素 |
您最近一年使用:0次
2023-07-06更新
|
80次组卷
|
2卷引用:山西省怀仁市第十一中学校2022-2023学年高二下学期7月期末化学试题
10 . 苯乙炔常用作医药中间体和有机合成试剂。下列关于苯乙炔说法正确的是


| A.分子中有14个σ键,5个π键 | B.所有碳原子均为 杂化 杂化 |
| C.分子中所有碳碳键的键能均相等 | D.该分子加聚后可以做导电塑料 |
您最近一年使用:0次
2023-07-06更新
|
83次组卷
|
2卷引用:山西省怀仁市第十一中学校2022-2023学年高二下学期7月期末化学试题



