1 . 淀粉-聚丙烯酸钠高吸水性树脂具有强大的吸水和保水能力,也是可生物降解的绿色材料。一种合成聚丙烯酸钠的路线如下图所示,下列有关说法不正确的是
CH3CH2COOH CH3CHBrCOOH
CH3CHBrCOOH CH2=CHCOONa
CH2=CHCOONa

| A.高吸水性树脂结构中有强亲水基团 |
B.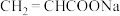 中C原子杂化轨道类型有2种 中C原子杂化轨道类型有2种 |
| C.反应①、③分别为取代反应、加聚反应 |
| D.反应②的条件为NaOH的乙醇溶液、加热 |
您最近一年使用:0次
解题方法
2 . 我国科学家研究发现,常温常压下,铁基离子液体 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有___________ 。在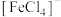 中,配体为
中,配体为___________ ,配位数为___________ 。
(2)在一定条件下 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为___________ , 的电子式为
的电子式为___________ 。
(3) 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。
①科学家通过最常用的___________ 实验测定了物质X的晶体结构,其晶胞如图b所示(未表示 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。___________ 。
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为___________ 。
④已知物质X的摩尔质量为 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为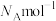 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为___________ nm,晶体的密度为___________  。
。
 在工业尾气中
在工业尾气中 、
、 等的脱除方面具有良好的性能。
等的脱除方面具有良好的性能。 结构如图所示。
结构如图所示。
 中C原子的杂化轨道类型有
中C原子的杂化轨道类型有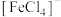 中,配体为
中,配体为(2)在一定条件下
 还可以转化为较稳定的
还可以转化为较稳定的
 中σ键与π键的个数比为
中σ键与π键的个数比为 的电子式为
的电子式为(3)
 与
与 反应生成具有特征蓝色的物质X,这是实验室中检验
反应生成具有特征蓝色的物质X,这是实验室中检验 的常用方法。
的常用方法。①科学家通过最常用的
 ),图a表示晶胞的
),图a表示晶胞的 结构(未表示K+)。
结构(未表示K+)。
③若A处粒子的坐标参数为(0,0,0),B处粒子为(1,1,1),则C处粒子的坐标为
④已知物质X的摩尔质量为
 ,晶胞中
,晶胞中 与
与 的最小距离为dnm,阿伏加德罗常数为
的最小距离为dnm,阿伏加德罗常数为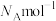 。则该晶胞中两个
。则该晶胞中两个 之间的最短距离为
之间的最短距离为 。
。
您最近一年使用:0次
解题方法
3 . 山梨糖醇主要用作甜味剂,甜度约为蔗糖的一半,热值与蔗糖相近。山梨糖醇的结构如图,下列有关说法错误的是


A. 山梨糖醇与足量Na反应产生 山梨糖醇与足量Na反应产生 | B.山梨糖醇中C原子的杂化方式均为 |
| C.山梨糖醇中所有原子在同一平面上 | D.山梨糖醇能催化氧化成含酮羰基的物质 |
您最近一年使用:0次
4 . 氨基吡啶与铜等金属离子所形成的配合物具备良好的磁学性质,某氨基吡啶衍生物铜配合物X的结构简式如图所示。
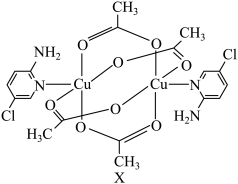
(1)基态氯原子的价层电子排布图为______ ;下列不同状态的氮原子中,能量最高的是______ (填字母)。
A. B.
B.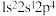 C.
C.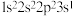 D.
D.
(2)C、N、O元素原子的电负性由大到小的顺序为______ 。
(3)X中 的配位数是
的配位数是______ ;铜元素有不同价态氧化物,高温下稳定性
______ CuO(填“大于”或“小于”),从离子的电子层结构角度分析,主要原因是______ 。
(4)X中N原子的杂化方式为______ 。
(5)下列关于X的说法中不正确的是______(填字母)。

(1)基态氯原子的价层电子排布图为
A.
 B.
B.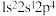 C.
C.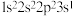 D.
D.
(2)C、N、O元素原子的电负性由大到小的顺序为
(3)X中
 的配位数是
的配位数是
(4)X中N原子的杂化方式为
(5)下列关于X的说法中不正确的是______(填字母)。
A.存在大π键 |
| B.存在氢键、配位键等化学键 |
| C.碳、氧原子间形成的σ键和π键个数比为2∶1 |
| D.铜属于d区元素 |
您最近一年使用:0次
2023-07-06更新
|
80次组卷
|
2卷引用:山西省怀仁市第十一中学校2022-2023学年高二下学期7月期末化学试题
5 . 苯乙炔常用作医药中间体和有机合成试剂。下列关于苯乙炔说法正确的是


| A.分子中有14个σ键,5个π键 | B.所有碳原子均为 杂化 杂化 |
| C.分子中所有碳碳键的键能均相等 | D.该分子加聚后可以做导电塑料 |
您最近一年使用:0次
2023-07-06更新
|
82次组卷
|
2卷引用:山西省怀仁市第十一中学校2022-2023学年高二下学期7月期末化学试题
解题方法
6 . 氧化镓是一种新型超宽窄带半导体材料,由于自身的优异性能,在紫外探测、高频功率器件等领域吸引了越来越多的关注和研究,中国科技部将其列入“十四五研发计划”,让第四代半导体获得更广泛的关注。回答下列问题:
(1)基态 原子最外层电子排布式为
原子最外层电子排布式为_______ 。
(2)①氧化镓的熔点为1740℃,氧化钙的熔点为2613℃,但有的离子晶体如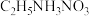 (硝酸乙基铵)的熔点只有12℃。
(硝酸乙基铵)的熔点只有12℃。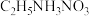 中N原子的杂化轨道类型是
中N原子的杂化轨道类型是_______ , 离子的空间结构为
离子的空间结构为_______ ,该物质中所含化学键类型:_______ (填字母)。
A.金属键 B.离子键 C.共价键 D.范德华力 E.σ键
②第一电离能:Al_______ Mg(填“>”或“<”),其原因是_______ 。
(3)锑化物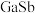 是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为
是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为 ,设Ga和Sb的原子半径分别为
,设Ga和Sb的原子半径分别为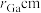 和
和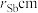 ,则原子的空间占有率为
,则原子的空间占有率为_______  (列出计算表达式,
(列出计算表达式,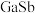 的摩尔质量为
的摩尔质量为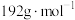 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。

(1)基态
 原子最外层电子排布式为
原子最外层电子排布式为(2)①氧化镓的熔点为1740℃,氧化钙的熔点为2613℃,但有的离子晶体如
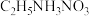 (硝酸乙基铵)的熔点只有12℃。
(硝酸乙基铵)的熔点只有12℃。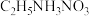 中N原子的杂化轨道类型是
中N原子的杂化轨道类型是 离子的空间结构为
离子的空间结构为A.金属键 B.离子键 C.共价键 D.范德华力 E.σ键
②第一电离能:Al
(3)锑化物
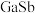 是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为
是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为 ,设Ga和Sb的原子半径分别为
,设Ga和Sb的原子半径分别为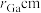 和
和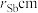 ,则原子的空间占有率为
,则原子的空间占有率为 (列出计算表达式,
(列出计算表达式,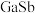 的摩尔质量为
的摩尔质量为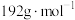 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解题方法
7 . 铜及其化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1)[Cu(NH3)2]Ac溶液可以吸收合成氨中对催化剂有毒害的CO气体[醋酸根(CH3COO-)简写成Ac-],反应的化学方程式为:[Cu(NH3)2]Ac+CO+NH3 [Cu(NH3)3CO]Ac。
[Cu(NH3)3CO]Ac。
①基态Cu+的核外电子排布式为_____ 。
②CH3COO-中C原子的杂化轨道类型为_____ 。
③[Cu(NH3)2]Ac中所含非金属元素的电负性由大到小的顺序是_____ (用元素符号表示)。
④[Cu(NH3)2]+中N原子形成的H—N—H键角_____ (填“大于”“小于”或“等于”)气态NH3中的键角,原因是_____ 。
⑤1个[Cu(NH3)3CO]+中含有的共价键数为_____ 。
(2)Cu—Mn—Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:
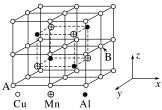
①合金的化学式为_____ 。
②若A原子的坐标参数为(0,1,0),则B原子的坐标参数为_____ 。
③已知该合金晶体的密度为ρg·cm-3,则最近的两个Al原子间的距离为_____ nm(阿伏加德罗常数的值用NA表示)。
(1)[Cu(NH3)2]Ac溶液可以吸收合成氨中对催化剂有毒害的CO气体[醋酸根(CH3COO-)简写成Ac-],反应的化学方程式为:[Cu(NH3)2]Ac+CO+NH3
 [Cu(NH3)3CO]Ac。
[Cu(NH3)3CO]Ac。①基态Cu+的核外电子排布式为
②CH3COO-中C原子的杂化轨道类型为
③[Cu(NH3)2]Ac中所含非金属元素的电负性由大到小的顺序是
④[Cu(NH3)2]+中N原子形成的H—N—H键角
⑤1个[Cu(NH3)3CO]+中含有的共价键数为
(2)Cu—Mn—Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:

①合金的化学式为
②若A原子的坐标参数为(0,1,0),则B原子的坐标参数为
③已知该合金晶体的密度为ρg·cm-3,则最近的两个Al原子间的距离为
您最近一年使用:0次



