名校
1 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为___________ ;As的第一电离能比Se的第一电离能大的原因为___________ 。
(2) 中心原子的杂化类型是:
中心原子的杂化类型是:___________ , 的立体构型是
的立体构型是___________ 。
(3) 属于
属于___________ (填“极性”或“非极性”)分子;比较 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:___________ 。
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___________ ;若该晶胞密度为ρg⋅cm ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为___________ 。
(1)基态硒原子的价层电子排布式为
(2)
 中心原子的杂化类型是:
中心原子的杂化类型是: 的立体构型是
的立体构型是(3)
 属于
属于 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为
 ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为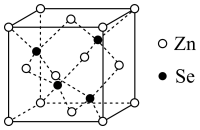
您最近一年使用:0次
2024-05-03更新
|
388次组卷
|
2卷引用:广东省茂名市高州中学2023-2024学年高二下学期期中考试化学试题
名校
解题方法
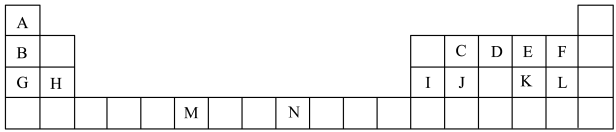
2 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)表中元素,电负性最强的是___________ (填元素符号),J的元素名称为___________ 。N基态原子核外能级上有___________ 未成对电子。
(2)D元素原子的价电子排布图为___________ ,核外有___________ 种不同运动状态的电子。
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是___________ (填“极性”或“非极性”)分子。
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是___________ (填字母)。
(1)表中元素,电负性最强的是
(2)D元素原子的价电子排布图为
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
a.  b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)COCl2分子中所有原子均满足8电子稳定结构,COCl2分子中σ键和π键的个数比为____ ,中心原子的杂化方式为____ 。
(2)AlH 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为____ ;列举与AlH 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:____ 、____ (填化学式)。
(3)用价层电子对互斥模型推断SnBr2分子中,Sn原子的轨道杂化方式为____ ,SnBr2分子中Br—Sn—Br的键角____ 120°(填“>”“<”或“=”)。
(1)COCl2分子中所有原子均满足8电子稳定结构,COCl2分子中σ键和π键的个数比为
(2)AlH
 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:(3)用价层电子对互斥模型推断SnBr2分子中,Sn原子的轨道杂化方式为
您最近一年使用:0次
2022-04-05更新
|
168次组卷
|
2卷引用:广东省茂名化州市第三中学2021-2022学年高二下学期3月月考化学试题
名校
4 . 硫和钙的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)钙元素的焰色反应呈砖红色,其中红色对应的辐射波长为_____ (填字母)nm。
A.435 B.500 C.580 D.605 E.700
(2)元素S和Ca中,第一电离能较大的是_____ (填元素符号),其基态原子核外电子排布式为__________________ 。
(3)通过X射线衍射实验发现,石膏(CaSO4• 2H2O)中存在SO42-离子。SO42-离子的几何构型为_________________ ,中心原子的杂化形式为_________________ 。
(4) 基态Ca原子中,核外电子占据最高能层的符号是______ ,占据该能层电子的电子云轮廓图形状为_______________ 。钙元素和锰元素属于同一周期,且核外最外层电子构型相同,但金属钙的熔点、沸点等都比金属锰低,原因是_____________________________ 。
(5)过氧化钙晶体的晶胞结构如图所示,已知该晶胞的密度是ρ g • cm-3,则晶胞结构中最近的两个Ca2+间的距离为_______________________________ nm (列算式即可,用NA表示阿伏伽德罗常数的数值),与Ca2+紧邻O22-的个数为______ 。

(1)钙元素的焰色反应呈砖红色,其中红色对应的辐射波长为
A.435 B.500 C.580 D.605 E.700
(2)元素S和Ca中,第一电离能较大的是
(3)通过X射线衍射实验发现,石膏(CaSO4• 2H2O)中存在SO42-离子。SO42-离子的几何构型为
(4) 基态Ca原子中,核外电子占据最高能层的符号是
(5)过氧化钙晶体的晶胞结构如图所示,已知该晶胞的密度是ρ g • cm-3,则晶胞结构中最近的两个Ca2+间的距离为

您最近一年使用:0次
2017-09-15更新
|
411次组卷
|
4卷引用:广东省茂名市2018届高三五大联盟学校9月份联考化学试题



