名校
1 . 顺铂[Pt(NH3)2Cl2]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是1,1-环丁二羧酸二氨合铂(II)的简称,属于第二代铂族抗癌药物,结构如图所示,其毒副作用低于顺铂。下列说法正确的是


| A.碳铂分子中所有碳原子在同一平面上 |
| B.碳铂分子中非金属元素的电负性大小:N>O>C>H |
| C.碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子数目之比为2:1 |
| D.1mol1,1-环丁二羧酸含有σ键的数目为12NA |
您最近一年使用:0次
名校
2 . NA为阿伏加德罗常数的值。下列说法正确的是


| A.46 g CH3CH2OH中采用sp3杂化的原子总数为2NA |
| B.0.1 mol SF6 (如图所示)分子中含有共价键的数目为1. 6NA |
| C.56 g铁与1 mol氯气充分反应,转移的电子数为2NA |
| D.标准状况下,11.2 L SO3溶于1 L水所形成的溶液中,含有的H+数为NA |
您最近一年使用:0次
2022-06-03更新
|
107次组卷
|
2卷引用:吉林省白山市抚松县第一中学2021-2022学年高二下学期第二次月考化学试题
名校
3 . 某超分子的结构如图所示,下列有关超分子的描述不正确 的是
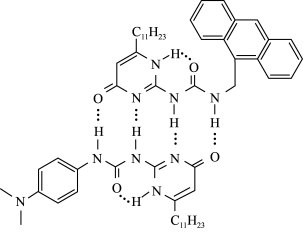

| A.图示中的超分子是两个不同的分子通过氢键形成的分子聚集体 |
| B.超分子的特征是分子识别和分子自组装 |
| C.超分子是指分子量特别大的分子 |
| D.图示中的超分子中的N原子采取sp2、sp3杂化 |
您最近一年使用:0次
2022-04-29更新
|
242次组卷
|
4卷引用:吉林省白山市抚松县第一中学2021-2022学年高二下学期第二次月考化学试题
名校
解题方法
4 . 钛及其化合物作用重要,尤其氧化钛、四氧化钛、钛酸钡等应用更广。回答下列问题:
(1)基态钛原子的价层电子排布式为_______ 。
(2) 二氧化钛是世界上最白的物质,1g二氧化钛可以把450多平方厘米的面积涂得雪白,是调制白油漆的最好颜料。基态Ti4+中核外电子占据的原子轨道数为_____ 个。
(3)四氯化钛是种有趣的液体,在潮湿空气中水解生成白色的二氧化钛水凝胶,军事上利用四氯化钛的这种“怪脾气”制造烟雾剂。写出四氯化钛水解的化学方程式_______ 。
(4)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。LiBH4由Li+和BH 构成,其中BH
构成,其中BH 的空间构型为
的空间构型为_______ ;B原子的杂化轨道类型为_______ 。
(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下:
锰元素位于第_______ 周期_______ 族_______ 区;比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,对此你的解释是_______ 。
(1)基态钛原子的价层电子排布式为
(2) 二氧化钛是世界上最白的物质,1g二氧化钛可以把450多平方厘米的面积涂得雪白,是调制白油漆的最好颜料。基态Ti4+中核外电子占据的原子轨道数为
(3)四氯化钛是种有趣的液体,在潮湿空气中水解生成白色的二氧化钛水凝胶,军事上利用四氯化钛的这种“怪脾气”制造烟雾剂。写出四氯化钛水解的化学方程式
(4)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。LiBH4由Li+和BH
 构成,其中BH
构成,其中BH 的空间构型为
的空间构型为(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下:
元素 | Mn | Fe | |
电离能/kJ∙mol−1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
您最近一年使用:0次
2022-01-17更新
|
306次组卷
|
3卷引用:吉林省抚松县第一中学2021-2022学年高二下学期开学考试化学试题
吉林省抚松县第一中学2021-2022学年高二下学期开学考试化学试题湖南省怀化市2021-2022学年高二上学期期末考试化学试题(已下线)期末押题卷02-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)
21-22高二·全国·课时练习
名校
5 . 下列说法中正确的是
| A.NCl3分子呈三角锥形,这是氮原子采取sp2杂化的结果 |
| B.sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的4个sp3杂化轨道 |
| C.中心原子采取sp3杂化的分子,其空间结构可能是四面体形或三角锥形或V形 |
| D.AB3型的分子空间结构必为平面三角形 |
您最近一年使用:0次
2021-12-25更新
|
643次组卷
|
4卷引用:吉林省抚松县第一中学2021-2022学年高二下学期开学考试化学试题
吉林省抚松县第一中学2021-2022学年高二下学期开学考试化学试题(已下线)2.2.2 杂化轨道理论-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)吉林省长春外国语学校2021-2022学年高二上学期期末考试化学试题(已下线)2.2.2 杂化轨道理论简介-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)
名校
解题方法
6 . 碳(C)、铜(Cu)、锡(Sn)及其化合物有许多用途。回答下列问题。
(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为_______ 。
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,P、S的第二电离能(I2)的大小关系为I2(P)___ I2(S)(填“>”、“<”或“=”),原因是_ 。PH3分子的热稳定性比NH3______ (填“强”或“弱”)。
(3)1mol苯中含 键的数目为
键的数目为______ 。CH3CH2COOH中C的杂化方式有______ ;
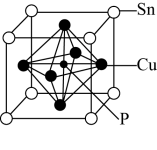
(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为anm,该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为__________ nm,该晶体密度为______ g cm-3(用含NA的代数式表示)。
cm-3(用含NA的代数式表示)。

(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,P、S的第二电离能(I2)的大小关系为I2(P)
(3)1mol苯中含
 键的数目为
键的数目为(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为anm,该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为
 cm-3(用含NA的代数式表示)。
cm-3(用含NA的代数式表示)。
您最近一年使用:0次
2021-04-14更新
|
210次组卷
|
3卷引用:吉林省白山市抚松县第一中学2021-2022学年高二下学期第二次月考化学试题
名校
7 . 分子或离子中的大π键可表示为 ,其中x表示参与形成大π键原子总数,y表示π电子数,已知π电子数=价电子总数-(σ电子对数+孤电子对数)×2。SO2和SO3的结构如图所示:
,其中x表示参与形成大π键原子总数,y表示π电子数,已知π电子数=价电子总数-(σ电子对数+孤电子对数)×2。SO2和SO3的结构如图所示:
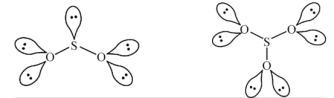
下列关于SO2和SO3的有关说法正确的是
 ,其中x表示参与形成大π键原子总数,y表示π电子数,已知π电子数=价电子总数-(σ电子对数+孤电子对数)×2。SO2和SO3的结构如图所示:
,其中x表示参与形成大π键原子总数,y表示π电子数,已知π电子数=价电子总数-(σ电子对数+孤电子对数)×2。SO2和SO3的结构如图所示:
下列关于SO2和SO3的有关说法正确的是
| A.SO2的π电子数为6 | B.SO3的大π键可表示为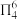 |
C.SO3中心原子为 杂化方式 杂化方式 | D.SO2与SO3空间构型相同 |
您最近一年使用:0次
2021-01-05更新
|
299次组卷
|
4卷引用:吉林省白山市抚松县第一中学2021-2022学年高二下学期第二次月考化学试题



