名校
1 . 东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1) 与
与 中更稳定的是
中更稳定的是______ (填化学式),原因为______ 。
(2)Ni与Co位于同一族,取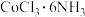 (黄色)、
(黄色)、 (紫红色)、
(紫红色)、 (绿色)和
(绿色)和 (紫色)四种化合物各1mol分别溶于水,分别加入足量的硝酸银溶液,立即产生氯化银,沉淀的量分别为3mol、2mol、1mol和1mol。
(紫色)四种化合物各1mol分别溶于水,分别加入足量的硝酸银溶液,立即产生氯化银,沉淀的量分别为3mol、2mol、1mol和1mol。
①根据实验事实用配合物的形式写出 的化学式:
的化学式:______ 。
②后两种物质的组成相同而颜色不同,写出其在水中的电离方程式:______ 。
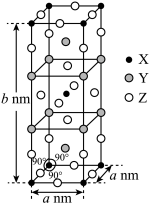
(3)一种含Ni元素的化合物的晶胞Q的结构如图。
______ 。
②设Q的最简式的摩尔质量为Mg⋅mol ,
, 为阿伏加德罗常数的值,则该晶体的密度的计算式为
为阿伏加德罗常数的值,则该晶体的密度的计算式为______ g·cm 。
。
(4)一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中的化合物,其晶胞结构如图所示。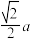 (其中a为晶胞参数)的Ni原子有
(其中a为晶胞参数)的Ni原子有______ 个。
②过渡金属与CO形成羰基配合物时,每个CO分子向中心原子提供2个电子,最终使中心原子的电子总数与同周期的稀有气体原子的原子序数相同,称为有效原子序数规则。根据此规则,镍与CO形成的羰基配合物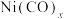 中,
中,
______ ,0.5mol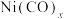 中含有
中含有______ molσ键。
(1)
 与
与 中更稳定的是
中更稳定的是(2)Ni与Co位于同一族,取
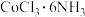 (黄色)、
(黄色)、 (紫红色)、
(紫红色)、 (绿色)和
(绿色)和 (紫色)四种化合物各1mol分别溶于水,分别加入足量的硝酸银溶液,立即产生氯化银,沉淀的量分别为3mol、2mol、1mol和1mol。
(紫色)四种化合物各1mol分别溶于水,分别加入足量的硝酸银溶液,立即产生氯化银,沉淀的量分别为3mol、2mol、1mol和1mol。①根据实验事实用配合物的形式写出
 的化学式:
的化学式:②后两种物质的组成相同而颜色不同,写出其在水中的电离方程式:
(3)一种含Ni元素的化合物的晶胞Q的结构如图。

②设Q的最简式的摩尔质量为Mg⋅mol
 ,
, 为阿伏加德罗常数的值,则该晶体的密度的计算式为
为阿伏加德罗常数的值,则该晶体的密度的计算式为 。
。(4)一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中的化合物,其晶胞结构如图所示。
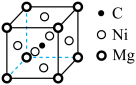
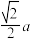 (其中a为晶胞参数)的Ni原子有
(其中a为晶胞参数)的Ni原子有②过渡金属与CO形成羰基配合物时,每个CO分子向中心原子提供2个电子,最终使中心原子的电子总数与同周期的稀有气体原子的原子序数相同,称为有效原子序数规则。根据此规则,镍与CO形成的羰基配合物
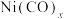 中,
中,
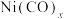 中含有
中含有
您最近一年使用:0次
2024-03-29更新
|
124次组卷
|
4卷引用:河北省保定市清苑中学等校2023-2024学年高二下学期3月月考化学试题
2 . 绿色化学的核心是原子经济化学反应。采用高选择的配位催化过程是实现原子经济学反应的重要手段之一、如烯烃的氢甲酰化生产醛等工业的配位催化过程是绿色化学工业的代表。用RhCl( Pph3)3(A)作催化剂实现下面反应: (B) →
(B) →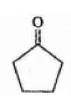 (G),其可能的机理如图:
(G),其可能的机理如图:
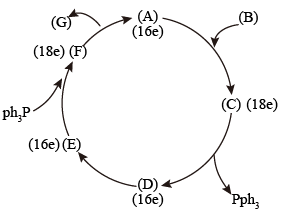
(C)中Rh的氧化态比(A)中Rh的氧化态大2
(1)试指出(A)、(C)、(D)、(E)、(F)中Rh的氧化态。___________
(2)试指出(A)、(C)、(D)、(E)、(F)中Rh原子的杂化类型。___________
(3)试画出与杂化类型相一致的(A)、(C)、(D)、(E)、(F)的结构式。___________
(4)指出(C)和(E)显颇磁性还是抗磁性,给出理由。___________
 (B) →
(B) → (G),其可能的机理如图:
(G),其可能的机理如图:
(C)中Rh的氧化态比(A)中Rh的氧化态大2
(1)试指出(A)、(C)、(D)、(E)、(F)中Rh的氧化态。
(2)试指出(A)、(C)、(D)、(E)、(F)中Rh原子的杂化类型。
(3)试画出与杂化类型相一致的(A)、(C)、(D)、(E)、(F)的结构式。
(4)指出(C)和(E)显颇磁性还是抗磁性,给出理由。
您最近一年使用:0次
3 . 金属M的三氯化物MCl3水溶液中加入锌汞齐后可得还原性溶液A,若将该溶液加入到醋酸钠的饱和溶液中可以得到难溶的红色晶体B。已知MCl3中Cl含量为67.16%,光谱分析表明,B分子呈中心对称,其中M原子的配位数为6(即M原子周围有6个原子与之成键),M原子含量27.64%,碳原子仅存在于醋酸根离子中,碳原子含量25.54%。试问:
(1)金属M的原子量为_______ 。
(2)红色晶体B中M原子和碳原子的个数比为_______ 。
(3)红色晶体B中和M原子配位的除了醋酸根离子还有_______ 。
(4)红色晶体B的分子式为_______ 。
(5)画出红色晶体B的结构图_______ 。
(1)金属M的原子量为
(2)红色晶体B中M原子和碳原子的个数比为
(3)红色晶体B中和M原子配位的除了醋酸根离子还有
(4)红色晶体B的分子式为
(5)画出红色晶体B的结构图
您最近一年使用:0次
4 . 羟基亚乙基二磷酸(HEDPA,结构式如下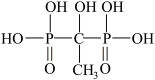 ,可简写为H4L)可在较宽的pH范围内与金属离子或原子形成稳定的配合物,是一种常用的配体,主要用作工业循环冷却水的缓蚀阻垢剂和无氰电镀的络合剂,与188Re所形成的188Re-HEDPA可用于治疗转移性骨癌。HEDPA和Mn2+可在一定的pH值和Mn2+/HEDPA配比下形成配合物A,将该配合物加热,在250°C以上样品失重25.80%,脱水结束后对残余物之进行元素分析,配合物A的元素含量为:Mn(15.74%)、C(6.88%)、H(4.62%)、O(55.01%)、P(17.77%)。
,可简写为H4L)可在较宽的pH范围内与金属离子或原子形成稳定的配合物,是一种常用的配体,主要用作工业循环冷却水的缓蚀阻垢剂和无氰电镀的络合剂,与188Re所形成的188Re-HEDPA可用于治疗转移性骨癌。HEDPA和Mn2+可在一定的pH值和Mn2+/HEDPA配比下形成配合物A,将该配合物加热,在250°C以上样品失重25.80%,脱水结束后对残余物之进行元素分析,配合物A的元素含量为:Mn(15.74%)、C(6.88%)、H(4.62%)、O(55.01%)、P(17.77%)。
(1)根据元素分析数据,推证配合物A的分子式为____ 。
(2)画出该配合物的结构示意图,并在图上注明HEDPA中哪些原子可为配位原子?(用*表示)____ 。
(3)实验测得配合物A的磁矩为6.12μ0,配合物未成对电子数为___ ,中心原子的杂化轨道类型是____ 。
(4)如何将合成A的条件作修改,可得到多核配合物___ ,写出2种该多核配合物的分子式__ 。
(5)已知配合物[Mn(H2O)6]2+的d-d跃迁在400nm-550nm范围内有弱的吸收,配合物呈肉粉色,在水溶液中形成配合物后,中心离子的晶体场分裂能将发生怎样的变化____ 。观察配合物的颜色明显加深,为什么?___ 。
 ,可简写为H4L)可在较宽的pH范围内与金属离子或原子形成稳定的配合物,是一种常用的配体,主要用作工业循环冷却水的缓蚀阻垢剂和无氰电镀的络合剂,与188Re所形成的188Re-HEDPA可用于治疗转移性骨癌。HEDPA和Mn2+可在一定的pH值和Mn2+/HEDPA配比下形成配合物A,将该配合物加热,在250°C以上样品失重25.80%,脱水结束后对残余物之进行元素分析,配合物A的元素含量为:Mn(15.74%)、C(6.88%)、H(4.62%)、O(55.01%)、P(17.77%)。
,可简写为H4L)可在较宽的pH范围内与金属离子或原子形成稳定的配合物,是一种常用的配体,主要用作工业循环冷却水的缓蚀阻垢剂和无氰电镀的络合剂,与188Re所形成的188Re-HEDPA可用于治疗转移性骨癌。HEDPA和Mn2+可在一定的pH值和Mn2+/HEDPA配比下形成配合物A,将该配合物加热,在250°C以上样品失重25.80%,脱水结束后对残余物之进行元素分析,配合物A的元素含量为:Mn(15.74%)、C(6.88%)、H(4.62%)、O(55.01%)、P(17.77%)。(1)根据元素分析数据,推证配合物A的分子式为
(2)画出该配合物的结构示意图,并在图上注明HEDPA中哪些原子可为配位原子?(用*表示)
(3)实验测得配合物A的磁矩为6.12μ0,配合物未成对电子数为
(4)如何将合成A的条件作修改,可得到多核配合物
(5)已知配合物[Mn(H2O)6]2+的d-d跃迁在400nm-550nm范围内有弱的吸收,配合物呈肉粉色,在水溶液中形成配合物后,中心离子的晶体场分裂能将发生怎样的变化
您最近一年使用:0次
解题方法
5 . 化合物 A是近十年开始采用的锅炉水添加剂。A的相对分子质量90.10,可形成无色晶体,能除去锅炉水中溶解氧,并可使锅炉壁钝化。
(1)A是用碳酸二甲酯和一水合肼在70°C下合成的,收率80%。 画出A的结构式___________ 。
(2)写出合成A的反应方程式___________ 。
(3)低于135°C时,A直接与溶解氧反应,生成三种产物。写出化学方程式___________ 。
(4) 高于135°C时,A先发生水解,水解产物再与氧反应。写出化学方程式___________ 。
(5)化合物A能使锅炉壁钝化是基于它能将氧化铁转化为致密的四氧化三铁。写出化学方程式___________ 。
(6)化合物A与许多金属离子形成八面体配合物,例如[Mn(A)3]2+。 结构分析证实该配合物中的A和游离态的A相比,分子中原本等长的两个键不再等长。画出这种配合物的结构简图(氢原子不需画出),讨论异构现象___________ 。
(1)A是用碳酸二甲酯和一水合肼在70°C下合成的,收率80%。 画出A的结构式
(2)写出合成A的反应方程式
(3)低于135°C时,A直接与溶解氧反应,生成三种产物。写出化学方程式
(4) 高于135°C时,A先发生水解,水解产物再与氧反应。写出化学方程式
(5)化合物A能使锅炉壁钝化是基于它能将氧化铁转化为致密的四氧化三铁。写出化学方程式
(6)化合物A与许多金属离子形成八面体配合物,例如[Mn(A)3]2+。 结构分析证实该配合物中的A和游离态的A相比,分子中原本等长的两个键不再等长。画出这种配合物的结构简图(氢原子不需画出),讨论异构现象
您最近一年使用:0次
名校
6 . 胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列有关胆矾的说法正确的是

下列有关胆矾的说法正确的是
| A.Cu2+的价电子排布式为3d84s1 |
| B.所有氧原子都采取sp3杂化 |
| C.氧原子参与形成离子键、配位键和氢键三种化学键 |
| D.胆矾中的水在不同温度下会分步失去 |
您最近一年使用:0次
2019-04-29更新
|
1100次组卷
|
4卷引用:【校级联考】福建省福州市八县(市)一中2018-2019学年高二下学期期中联考化学试题
解题方法
7 . 超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。___________ ;核外未成对电子数是___________ 个。
(2)该超分子中存在的化学键类型有___________ 。
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是___________ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因___________ 。
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是___________ 。
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。___________ 。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是M g·mol-1,阿伏伽德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为___________ pm。

(2)该超分子中存在的化学键类型有
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。

您最近一年使用:0次
2019-04-23更新
|
5685次组卷
|
3卷引用:陕西省西安市选课分科摸底考2023-2024学年高二下学期4月月考化学试题
8 . 过渡金属的某些氧化物能在常温下催化氧化空气中的一氧化碳和甲醛,如铜锰氧化物(CuMn2O4)等。
(1)铜元素位于第4周期第ⅠB族。基态Cu+的核外电子排布式为___________ 。SO 的空间构型为
的空间构型为___________ 。
(2)HCHO中含有的σ键和π键数目之比为___________ 。
(3)火山喷出的岩浆中含有多种硫化物,冷却时ZnS比HgS先析出,原因是___________ 。
(4)CuCl的盐酸溶液能吸收CO形成配合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O],其结构如图所示。

下列说法不正确的是___________
(5)请判断键角NF3___________ NH3,其原因是___________ 。
(6)Cu3N形成的晶体结构如图所示。则与同一个N3-相连的Cu+有___________ 个,Cu+的半径为a pm,N3-的半径为b pm,则Cu3N的密度为___________ g/cm3.
(1)铜元素位于第4周期第ⅠB族。基态Cu+的核外电子排布式为
 的空间构型为
的空间构型为(2)HCHO中含有的σ键和π键数目之比为
(3)火山喷出的岩浆中含有多种硫化物,冷却时ZnS比HgS先析出,原因是
(4)CuCl的盐酸溶液能吸收CO形成配合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O],其结构如图所示。

下列说法不正确的是
| A.该配合物质只含有离子键和配位键 | B.该配合物中Cl原子的杂化类型为sp3 |
| C.该配合物只有CO和H2O作为配体 | D.CO与N2的价电子总数相同,其结构为 |
(6)Cu3N形成的晶体结构如图所示。则与同一个N3-相连的Cu+有
您最近一年使用:0次
9-10高二下·河南郑州·期末
名校
9 . 水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为______________________________ ;
(2)写出与H2O分子互为等电子体的微粒_________________________ (填2种)。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是______________
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_________ (请用相应的编号填写)

(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能” 是_________ kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配离子。请写出生成此配离子的离子方程式:__________________________________________________________ 。
(1)水分子中氧原子在基态时核外电子排布式为
(2)写出与H2O分子互为等电子体的微粒
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
| A.氧原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
| C.微粒的化学性质发生了改变 | D.微粒中的键角发生了改变 |
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是

(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能” 是
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配离子。请写出生成此配离子的离子方程式:
您最近一年使用:0次
2014-01-09更新
|
580次组卷
|
7卷引用:2010年郑州市智林学校高二下学期期末考试化学试题
(已下线)2010年郑州市智林学校高二下学期期末考试化学试题(已下线)2010-2011学年山西省吕梁市高二下学期期中考试化学试卷(已下线)2013-2014学年四川省绵阳中学高二上学期第三次月考化学试卷【全国百强校】内蒙古集宁一中(东校区)2017-2018学年高二下学期期中考试化学试题【市级联考】新疆维吾尔自治区乌鲁木齐市2018-2019学年高二下学期期末考试化学试题(已下线)2015届安徽省滁州中学高三九月份化学月考试卷江西省井冈山市宁冈中学2021-2022学年高三下学期开学考试化学试题



