1 . 短周期元素可形成许多结构和性质不同的化合物,回答下列问题:

(1) 是一种甲基化试剂,能发生水解反应
是一种甲基化试剂,能发生水解反应 ;
; 的水解产物为
的水解产物为_____ (填化学式)。
(2) 是共价化合物,可以形成二聚体和多聚体
是共价化合物,可以形成二聚体和多聚体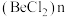 ,二聚体中
,二聚体中 的杂化方式为
的杂化方式为 ,二聚体的结构式为
,二聚体的结构式为_____ 。
(3) 分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成
分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成 的方向上时斥力最大,判断
的方向上时斥力最大,判断 应采用结构
应采用结构_____ (填“a”或“b”)。
(4) 在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了
在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了_____ (填化学式),比较它与 的稳定性并说明理由
的稳定性并说明理由_____ 。
(5)在超高压下,金属钠和氦可形成化合物。结构中的钠离子按简单立方排布,形成 立方体空隙如图,电子对
立方体空隙如图,电子对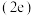 和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对
和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对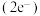 在该晶胞中的所有分数坐标除了
在该晶胞中的所有分数坐标除了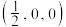 、
、 ,还有
,还有_____ ;若晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞的边长
,晶胞的边长
_____  (用含
(用含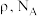 的代数式表示)。
的代数式表示)。


(1)
 是一种甲基化试剂,能发生水解反应
是一种甲基化试剂,能发生水解反应 ;
; 的水解产物为
的水解产物为(2)
 是共价化合物,可以形成二聚体和多聚体
是共价化合物,可以形成二聚体和多聚体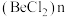 ,二聚体中
,二聚体中 的杂化方式为
的杂化方式为 ,二聚体的结构式为
,二聚体的结构式为(3)
 分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成
分子的电子对空间构型为三角双锥,排布方式有两种,结构如图。根据价层电子对互斥理论中:“孤电子对一成键电子对”分布在互成 的方向上时斥力最大,判断
的方向上时斥力最大,判断 应采用结构
应采用结构(4)
 在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了
在水溶液中显蓝色,加入过量的氨水后变为深蓝色,原因是生成了 的稳定性并说明理由
的稳定性并说明理由(5)在超高压下,金属钠和氦可形成化合物。结构中的钠离子按简单立方排布,形成
 立方体空隙如图,电子对
立方体空隙如图,电子对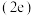 和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对
和氦原子交替分布填充在立方体的中心。若将氦原子放在晶胞顶点,则电子对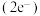 在该晶胞中的所有分数坐标除了
在该晶胞中的所有分数坐标除了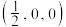 、
、 ,还有
,还有 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,晶胞的边长
,晶胞的边长
 (用含
(用含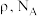 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2 . 络合平衡遵循化学平衡移动原理。已知:①Ag++NH3 [Ag(NH3)]+ K1
[Ag(NH3)]+ K1
②[Ag(NH3)]++NH3 [Ag(NH3)2]2+ K2(K2>K1)。
[Ag(NH3)2]2+ K2(K2>K1)。
向饱和AgCl溶液中滴加氨水,lgX[X= 或
或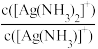 与lgc(NH3)关系如图所示:
与lgc(NH3)关系如图所示:
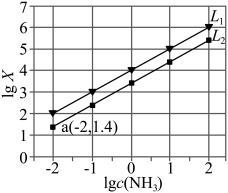
下列说法错误的是
 [Ag(NH3)]+ K1
[Ag(NH3)]+ K1②[Ag(NH3)]++NH3
 [Ag(NH3)2]2+ K2(K2>K1)。
[Ag(NH3)2]2+ K2(K2>K1)。向饱和AgCl溶液中滴加氨水,lgX[X=
 或
或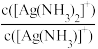 与lgc(NH3)关系如图所示:
与lgc(NH3)关系如图所示:
下列说法错误的是
| A.直线L2代表反应①中离子浓度关系 |
| B.络合平衡常数K2=1.0×104 |
| C.在上述混合液中加入足量盐酸,无明显现象 |
D.Ag++2NH3 [Ag(NH3)2]+的平衡常数K =107.4 [Ag(NH3)2]+的平衡常数K =107.4 |
您最近一年使用:0次
3 . 下列化合物是抗磁性的是
A.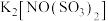 | B. | C. | D.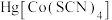 |
您最近一年使用:0次
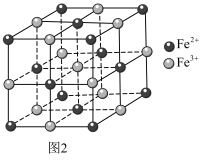
4 . 普鲁士蓝的化学式为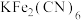 ,其结构如图1(可能位于中心的
,其结构如图1(可能位于中心的 未标出)或图2(
未标出)或图2( 、
、 未标出)所示。
未标出)所示。
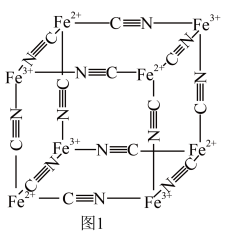
请回答:
(1)基态Fe价电子轨道表示式为_______ 。
(2)已知铁的电离能数据如下:
则,铁的第四电离能( )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:_______ 。
(3)关于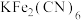 晶体下列说法不正确的是_______(填序号)。
晶体下列说法不正确的是_______(填序号)。
(4)可溶性氰化物(如KCN)有剧毒,但普鲁士蓝却无毒,请从结构角度解释普鲁士蓝无毒的原因是_______ 。
(5)图2晶胞中 的个数为
的个数为_______ ,设普鲁士蓝的最简式的式量为Mr,晶体密度为 ,则相邻
,则相邻 之间的最短距离为
之间的最短距离为_______ nm。(列出计算式, 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
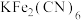 ,其结构如图1(可能位于中心的
,其结构如图1(可能位于中心的 未标出)或图2(
未标出)或图2( 、
、 未标出)所示。
未标出)所示。
请回答:
(1)基态Fe价电子轨道表示式为
(2)已知铁的电离能数据如下:
电离能/( ) ) |  |  |  |  | …… |
| Fe | 759 | 1561 | 2597 | 5290 | …… |
 )大于第三电离能(
)大于第三电离能( )的可能原因是:
)的可能原因是:(3)关于
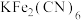 晶体下列说法不正确的是_______(填序号)。
晶体下列说法不正确的是_______(填序号)。| A.存在的化学键有σ键、π键、配位键、离子键等 |
B.Fe、N、C的电负性由大到小的顺序: |
C.晶体中 的键能>KCN中 的键能>KCN中 的键能 的键能 |
D.晶胞中 、 、 原子均参与形成配位键,其配位数之比为6:6 原子均参与形成配位键,其配位数之比为6:6 |
(5)图2晶胞中
 的个数为
的个数为 ,则相邻
,则相邻 之间的最短距离为
之间的最短距离为 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近一年使用:0次
2023-05-06更新
|
699次组卷
|
4卷引用:浙江省温州市2023届高三下学期5月第三次模拟适应性考试化学试题
浙江省温州市2023届高三下学期5月第三次模拟适应性考试化学试题(已下线)【2023】【高三下】【模拟考】【温州三模】【高中化学】【李鼎收集】浙江省名校协作体2023-2024学年高三上学期开学适应性考试化学试题(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)
5 . 固体化合物 由4种元素组成,某学习小组开展如图探究实验:
由4种元素组成,某学习小组开展如图探究实验:
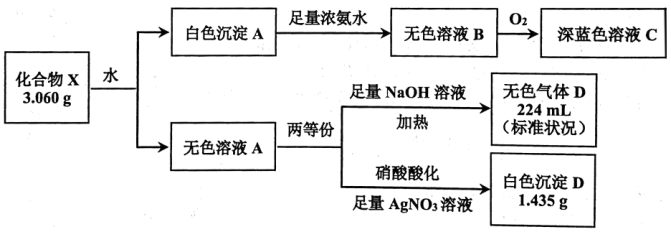
已知:白色沉淀 仅含两种元素。溶液
仅含两种元素。溶液 和溶液
和溶液 中阳离子由相同元素组成,且完全转化时,消耗标准状况下
中阳离子由相同元素组成,且完全转化时,消耗标准状况下 ,同时消耗
,同时消耗 。
。
请回答:
(1)无色气体 的电子式是
的电子式是_______ 。
(2)化合物 中的金属元素是
中的金属元素是_______ (填写元素符号),化学式是_______ 。
(3)写出无色溶液 转化为深蓝色溶液
转化为深蓝色溶液 的离子方程式
的离子方程式_______ 。
(4)白色沉淀 加水煮沸得到绿色溶液(溶质的元素组成与沉淀
加水煮沸得到绿色溶液(溶质的元素组成与沉淀 相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。
相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。
①写出上述反应的化学方程式_______ 。
②设计实验方案证明红色固体是混合物_______ 。
 由4种元素组成,某学习小组开展如图探究实验:
由4种元素组成,某学习小组开展如图探究实验:
已知:白色沉淀
 仅含两种元素。溶液
仅含两种元素。溶液 和溶液
和溶液 中阳离子由相同元素组成,且完全转化时,消耗标准状况下
中阳离子由相同元素组成,且完全转化时,消耗标准状况下 ,同时消耗
,同时消耗 。
。请回答:
(1)无色气体
 的电子式是
的电子式是(2)化合物
 中的金属元素是
中的金属元素是(3)写出无色溶液
 转化为深蓝色溶液
转化为深蓝色溶液 的离子方程式
的离子方程式(4)白色沉淀
 加水煮沸得到绿色溶液(溶质的元素组成与沉淀
加水煮沸得到绿色溶液(溶质的元素组成与沉淀 相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。
相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。①写出上述反应的化学方程式
②设计实验方案证明红色固体是混合物
您最近一年使用:0次
2021-09-02更新
|
897次组卷
|
2卷引用:浙江省“七彩阳光”2022届新高考研究联盟返校考试化学试题
解题方法
6 . 钢中加入微量钒可起到脱氧和脱氮的作用,改善钢的性能。测定钢中钒含量的步骤如下:钢试样用硫磷混合酸分解,钒以四价形式存在。再用KMnO4将其氧化为五价,过量的KMnO4用NaNO2除去,过量的NaNO2用尿素除去。五价钒与N-苯甲酰-N-苯基羟胺在3.5 mol/L~5 mol/L盐酸介质中以1:2形成紫红色单核电中性配合物,比色测定。
回答如下问题:
(1)高价钒在酸性溶液中通常以含氧阳离子的形式存在。写出钒与浓硫酸作用的反应方程式_________ 。
(2)以反应方程式表示上述测定过程中KMnO4、NaNO2和尿素的作用_________ 。
(3)写出紫红色配合物的结构式_________ 。
回答如下问题:
(1)高价钒在酸性溶液中通常以含氧阳离子的形式存在。写出钒与浓硫酸作用的反应方程式
(2)以反应方程式表示上述测定过程中KMnO4、NaNO2和尿素的作用
(3)写出紫红色配合物的结构式
您最近一年使用:0次
解题方法
7 . 咔咯(corrole)及其配合物作为人工合成的大环配体之一,咔咯的合成及其与金属离子的配位化学备受关注。利用咔咯作为反应配体,可实现过渡金属离子的非常规氧化态,制备功能材料,探索新型催化剂,等等。下图(a)给出三(五氟苯基)咔咯分子(A)的示意图,简写为H3(tpfc)。它与金属离子结合时四个氮原子均参与配位。室温下,空气中,Cr(CO)6和A在甲苯中回流得到深红色晶体B(反应1),B显顺磁性,有效磁矩为1.72μB,其中金属离子的配位几何为四方锥;在惰性气氛保护下,B与三苯基膦(PPh3)和三苯基氧膦(OPPh3)按1:1:1在甲苯中反应得到绿色晶体C(反应2);在氩气保护下,CrCl2和A在吡啶(简写为py)中反应,得到深绿色晶体D(反应3),D中金属离子为八面体配位,配位原子均为氮原子。在一定的条件下,B、C和D之间可以发生转化(下图b),这一过程被认为有可能用于O2的活化或消除。
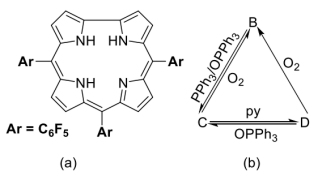
(1)A中的咔咯环是否有芳香性______ ?与之对应的π电子数是______ 。
(2)写出B、C、D的化学式(要求:配体用简写符号表示):
B______ 、C______ 、D______ 。
(3)写出B、C、D中金属离子的价电子组态(均用dn方式表示)。
B______ 、C______ 、D______ 。
(4)写出制备B、C、D的反应方程式(要求:配体用简写符号,系数为最简整数比)。
B______ 、C______ 、D______ 。
(5)利用电化学处理,B可以得电子转化为B-,也可以失去电子转化为B+。与预期的磁性相反,B+依然显示顺磁性。进一步光谱分析发现,与咔咯环配体相关的吸收峰位置发生了显著变化。推测金属离子的价电子组态______ (用dn方式表示),指出磁性与光谱变化的原因______ 。

(1)A中的咔咯环是否有芳香性
(2)写出B、C、D的化学式(要求:配体用简写符号表示):
B
(3)写出B、C、D中金属离子的价电子组态(均用dn方式表示)。
B
(4)写出制备B、C、D的反应方程式(要求:配体用简写符号,系数为最简整数比)。
B
(5)利用电化学处理,B可以得电子转化为B-,也可以失去电子转化为B+。与预期的磁性相反,B+依然显示顺磁性。进一步光谱分析发现,与咔咯环配体相关的吸收峰位置发生了显著变化。推测金属离子的价电子组态
您最近一年使用:0次
解题方法
8 . (1)德国马克斯普朗克聚合物研究所的Klaus Mullen研究小组制备了一种六取代的苯,其拥有中性分子中目前已知的最大偶极矩(14.1Debye),已经超过了离子化合物的偶极矩如溴化钾(10.5Debye)。该分子含氮 、氢
、氢 ,摩尔质量在
,摩尔质量在 左右。画出其结构简式
左右。画出其结构简式____ 。
(2)化合物甲由四种元素组成,甲隔绝空气爆炸产生乙、丙、丁的数量关系如下图:

丙和丁是相对分子质量相同的常见气体,其中丁是空气的主要成分之一。给出甲的化学式____ 。
(3)含铬配合物X由四种元素组成,元素分析结果如下:含氯 、含氧
、含氧 、含氢
、含氢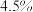 。将
。将 溶于
溶于 水中,加入过量
水中,加入过量 使其溶解;再在溶液中加入过量硝酸银至沉淀完全,收集沉淀、将沉淀干燥,得
使其溶解;再在溶液中加入过量硝酸银至沉淀完全,收集沉淀、将沉淀干燥,得 产物,1.066gA在干燥空气中缓慢加热至100°C时有0.144g水。
产物,1.066gA在干燥空气中缓慢加热至100°C时有0.144g水。
①给出配合物X的化学式(写明内界和外界)____ 。
②画出配合物X中阳离子的几何异构体____ 。
 、氢
、氢 ,摩尔质量在
,摩尔质量在 左右。画出其结构简式
左右。画出其结构简式(2)化合物甲由四种元素组成,甲隔绝空气爆炸产生乙、丙、丁的数量关系如下图:

丙和丁是相对分子质量相同的常见气体,其中丁是空气的主要成分之一。给出甲的化学式
(3)含铬配合物X由四种元素组成,元素分析结果如下:含氯
 、含氧
、含氧 、含氢
、含氢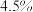 。将
。将 溶于
溶于 水中,加入过量
水中,加入过量 使其溶解;再在溶液中加入过量硝酸银至沉淀完全,收集沉淀、将沉淀干燥,得
使其溶解;再在溶液中加入过量硝酸银至沉淀完全,收集沉淀、将沉淀干燥,得 产物,1.066gA在干燥空气中缓慢加热至100°C时有0.144g水。
产物,1.066gA在干燥空气中缓慢加热至100°C时有0.144g水。①给出配合物X的化学式(写明内界和外界)
②画出配合物X中阳离子的几何异构体
您最近一年使用:0次
9 . 氮、磷、砷、铁、钛等元素及其化合物在现代农业、科技和国防建设中有着许多独特的用途。
I.如LiFePO4是新型锂离子电池的电极材料,可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。
(1)Fe2+核外电子排布式为___________ ,NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是___________ (填元素符号)。
(2)苯胺(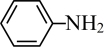 )和NH4H2PO4中的N原子杂化方式分别为
)和NH4H2PO4中的N原子杂化方式分别为___________ 。
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是___________ 。
II.(4)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiC136H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________ 。
(5)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。
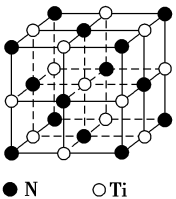
①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则与该Ti原子最邻近的Ti的数目为___________ 。Ti 原子与跟它次邻近的N原子之间的距离为___________ 。
②已知在氮化钛晶体中Ti原子的半径为apm,N原子的半径为bpm,它们在晶体中是紧密接触的,则在氮化钛晶体中原子的空间利用率为___________ 。(用a、b表示)
III.(6)从磷钇矿中可提取稀土元素钇(Y),某磷钇矿的晶胞如图所示,该磷钇矿的化学式为___________ 。
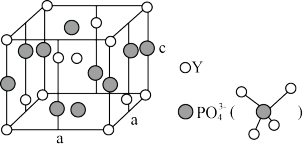
(7)已知晶胞参数为anm和cnm,阿伏加德罗常数的值为NA,则该磷钇矿的ρ为___________ 。g·cm-3 (列出计算式,用a、c表示)
I.如LiFePO4是新型锂离子电池的电极材料,可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。
(1)Fe2+核外电子排布式为
(2)苯胺(
 )和NH4H2PO4中的N原子杂化方式分别为
)和NH4H2PO4中的N原子杂化方式分别为(3)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是
II.(4)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiC136H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为
(5)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。

①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则与该Ti原子最邻近的Ti的数目为
②已知在氮化钛晶体中Ti原子的半径为apm,N原子的半径为bpm,它们在晶体中是紧密接触的,则在氮化钛晶体中原子的空间利用率为
III.(6)从磷钇矿中可提取稀土元素钇(Y),某磷钇矿的晶胞如图所示,该磷钇矿的化学式为

(7)已知晶胞参数为anm和cnm,阿伏加德罗常数的值为NA,则该磷钇矿的ρ为
您最近一年使用:0次
解题方法
10 . 超分子化学已逐渐扩展到化学的各个分支,还扩展到生命科学和物理学等领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。___________ ;核外未成对电子数是___________ 个。
(2)该超分子中存在的化学键类型有___________ 。
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是___________ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有___________ 。
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因___________ 。
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是___________ 。
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。___________ 。已知该晶体的密度是ρg·cm-3,Mo的摩尔质量是M g·mol-1,阿伏伽德罗常数是NA,晶体中距离最近的Mo原子核之间的距离为___________ pm。

(2)该超分子中存在的化学键类型有
A σ键Bπ键C离子键D氢键
(3)该超分子中配体CO提供孤电子对的原子是
(4)从电负性角度解释CF3COOH的酸性强于CH3COOH的原因
(5)C60与金刚石互为同素异形体,从结构与性质之间的关系解释C60的熔点远低于金刚石的原因是
(6)已知:某晶胞中各原子的相对位置可用如图所示的原子坐标表示,其中所有顶点原子坐标均为(0,0,0)。

您最近一年使用:0次
2019-04-23更新
|
5686次组卷
|
3卷引用:【省级联考】云南省2019届高三下学期第二次复习统一检测理科综合化学试题



