名校
解题方法
1 . 分类是学化学的重要方法,下列分类正确的是
A.醇类: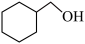 和 和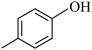 | B.电子云轮廓图为球形:2s、2p、3s |
| C.共价晶体:锗、硅和金刚石 | D.配合物: 和 和 |
您最近一年使用:0次
2 . 卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有________ ,其中能量较高的是________ 。(填标号)
A. B.
B. C.
C.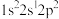 D.
D.
(2)基态Br原子的核外电子排布式为________ 。
(3) 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是________ ,中心离子的配位数为________ 。
(4)Kr是第四周期的稀有气体元素,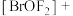 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为________ 。
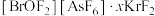 晶体中的微粒间作用力有
晶体中的微粒间作用力有________ (填标号)。
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在 形式,画出
形式,画出 的链状结构
的链状结构________ 。
(6)四氟乙烯 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为________ 和________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因________ 。
(1)氟原子激发态的电子排布式有
A.
 B.
B. C.
C.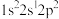 D.
D.
(2)基态Br原子的核外电子排布式为
(3)
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(4)Kr是第四周期的稀有气体元素,
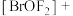 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为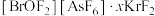 晶体中的微粒间作用力有
晶体中的微粒间作用力有a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在
 形式,画出
形式,画出 的链状结构
的链状结构(6)四氟乙烯
 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为
您最近一年使用:0次
名校
解题方法
3 . 配合物在生产、生活中应用广泛。例如, (铁氰化钾)用于检验
(铁氰化钾)用于检验 ,
, 用于检验
用于检验 。回答下列问题:
。回答下列问题:
(1)基态 的价层电子排布式为
的价层电子排布式为___________ ,向某未知溶液中滴加适量 溶液,若
溶液,若___________ (填实验现象),则说明溶液中含有 。
。
(2) 中配位原子是
中配位原子是___________ (填元素符号)。
(3)已知:络合平衡反应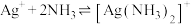 ,其平衡常数又称配离子稳定常数,
,其平衡常数又称配离子稳定常数,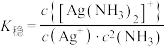 。常温下,
。常温下,
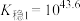 ;
;
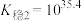 。
。
由此推知稳定性:
___________  (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是___________ 。
(4)分裂能( )定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能(
)定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能( ):
):
___________  (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是___________ 。
 (铁氰化钾)用于检验
(铁氰化钾)用于检验 ,
, 用于检验
用于检验 。回答下列问题:
。回答下列问题:(1)基态
 的价层电子排布式为
的价层电子排布式为 溶液,若
溶液,若 。
。(2)
 中配位原子是
中配位原子是(3)已知:络合平衡反应
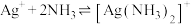 ,其平衡常数又称配离子稳定常数,
,其平衡常数又称配离子稳定常数,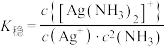 。常温下,
。常温下,
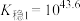 ;
;
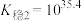 。
。由此推知稳定性:

 (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是(4)分裂能(
 )定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能(
)定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能( ):
):
 (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是
您最近一年使用:0次
名校
解题方法
4 . 化学与人类生产、生活息息相关。下列叙述错误的是
| A.18—冠—6分子可识别K+,因此可增大KI在苯中的溶解度 |
| B.向硫酸四氨合铜溶液中加入乙醇会析出深蓝色晶体,因为乙醇的极性比水小 |
| C.壁虎能在天花板上爬行,是因为它的细毛与墙体之间有范德华力 |
| D.“杯酚”可分离C60和C70,体现了超分子的“自组装”特性 |
您最近一年使用:0次
5 . NA表示阿伏加德罗常数的值,配合物Na2[Fe(CN)5(NO)]可用于离子检验。下列说法不正确的是
| A.该配合物中存在离子键、配位键、极性键、非极性键 |
| B.配离子为[Fe(CN)5(NO)]2-,中心离子为Fe3+,配位数为6,配位原子为C和N |
| C.1mol该配合物中σ键数目为6NA |
| D.该配合物为离子化合物,易电离,1mol配合物电离共得到3NA个阴、阳离子 |
您最近一年使用:0次
6 . 已知:铜离子的配位数通常为4, 和
和 均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是
均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是
 和
和 均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是
均为深蓝色,某小组同学设计以下方案研究铜的配合物。下列说法错误的是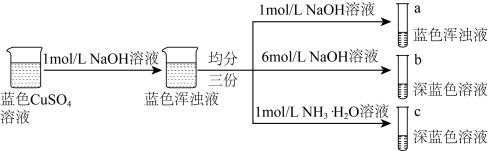
A.b、c溶液中 相同 相同 |
B.b中得到配合物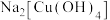 ,其配体为 ,其配体为 |
C.由实验可知, 的配位能力比 的配位能力比 弱 弱 |
D.a、b、c三种溶液中加入 溶液均会产生白色沉淀 溶液均会产生白色沉淀 |
您最近一年使用:0次
名校
7 . 反应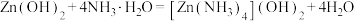 中的有关物质的说法不正确的是
中的有关物质的说法不正确的是
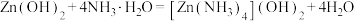 中的有关物质的说法不正确的是
中的有关物质的说法不正确的是A.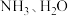 固态时均属于分子晶体 固态时均属于分子晶体 |
B.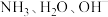 均为 均为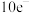 微粒 微粒 |
C. 分子中的键角 分子中的键角 比 比 中的键角 中的键角 大 大 |
D. 中存在离子键、配位键、极性键 中存在离子键、配位键、极性键 |
您最近一年使用:0次
名校
解题方法
8 . 蓝铜矿的主要成分为2CuCO3·Ca(OH)2,将它与焦炭一起加热可以生成Cu、CO2和H2O。下列说法正确的是
| A.Cu是第四周期第ⅦB族元素 |
| B.0.1mol[Cu(H2O)4]2+中所含配位键的物质的量为0.8mol |
| C.电负性:O>C>H |
| D.将0.1L0.1mol/L[Cu(NH3)4](OH)2加入足量的MgCl2溶液中,理论上可得到0.2molMg(OH)2 |
您最近一年使用:0次
9 . Ⅰ.经研究表明,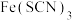 是配合物,
是配合物, 与
与 不仅能以1:3的个数比配合,还可以其他个数比配合。
不仅能以1:3的个数比配合,还可以其他个数比配合。
(1) 中所有原子都达到
中所有原子都达到 稳定结构,请画出
稳定结构,请画出 的结构式
的结构式______ ,若其中主要是 与
与 以个数比1:1配合所得离子,显血红色,该离子的离子符号是
以个数比1:1配合所得离子,显血红色,该离子的离子符号是______ 。
(2)若 与
与 以个数比1:5配合,则
以个数比1:5配合,则 与KSCN在水溶液中发生反应的化学方程式可以表示为
与KSCN在水溶液中发生反应的化学方程式可以表示为______ 。
(3)Fe还能与CO形成配合物 ,该配合物中的配位原子是
,该配合物中的配位原子是______ (写元素符号)。
(4) 溶液可吸收NO生成配合物
溶液可吸收NO生成配合物 ,减少环境污染。下列说法正确的是 。
,减少环境污染。下列说法正确的是 。
Ⅱ.铜的单质及其化合物应用广泛:研究表明新冠病毒在铜表面存活时间最短,仅为4小时,铜被称为细菌病毒的“杀手”;硫酸铜可用于制农药波尔多液。
(5)向硫酸铜溶液中逐滴加入氨水,形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,请画出深蓝色离子的结构。______ ;再加入乙醇后,析出深蓝色的晶体,请写出深蓝色晶体的化学式:______ 。
(6)金属铜与氨水或过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液发生反应得到深蓝色溶液,写出离子方程式:______ 。
(7) 结构示意图如下,
结构示意图如下, 中存在的相互作用有
中存在的相互作用有______ (填序号)。
(8)青霉胺可用于医学上误食铜盐的解毒,解毒原理: 形成环状配合物,其结构如图所示,该配合物无毒、易溶于水,可经尿液排出。下列说法错误的是 。
形成环状配合物,其结构如图所示,该配合物无毒、易溶于水,可经尿液排出。下列说法错误的是 。
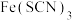 是配合物,
是配合物, 与
与 不仅能以1:3的个数比配合,还可以其他个数比配合。
不仅能以1:3的个数比配合,还可以其他个数比配合。(1)
 中所有原子都达到
中所有原子都达到 稳定结构,请画出
稳定结构,请画出 的结构式
的结构式 与
与 以个数比1:1配合所得离子,显血红色,该离子的离子符号是
以个数比1:1配合所得离子,显血红色,该离子的离子符号是(2)若
 与
与 以个数比1:5配合,则
以个数比1:5配合,则 与KSCN在水溶液中发生反应的化学方程式可以表示为
与KSCN在水溶液中发生反应的化学方程式可以表示为(3)Fe还能与CO形成配合物
 ,该配合物中的配位原子是
,该配合物中的配位原子是(4)
 溶液可吸收NO生成配合物
溶液可吸收NO生成配合物 ,减少环境污染。下列说法正确的是 。
,减少环境污染。下列说法正确的是 。| A.该配合物中所含非金属元素均位于元素周期表的p区 |
B. 提供孤电子对用于形成配位键 提供孤电子对用于形成配位键 |
| C.该配合物中阴离子空间结构为正四面体形 |
D.配离子为 ,中心离子的配位数为5 ,中心离子的配位数为5 |
Ⅱ.铜的单质及其化合物应用广泛:研究表明新冠病毒在铜表面存活时间最短,仅为4小时,铜被称为细菌病毒的“杀手”;硫酸铜可用于制农药波尔多液。
(5)向硫酸铜溶液中逐滴加入氨水,形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,请画出深蓝色离子的结构。
(6)金属铜与氨水或过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液发生反应得到深蓝色溶液,写出离子方程式:
(7)
 结构示意图如下,
结构示意图如下, 中存在的相互作用有
中存在的相互作用有
(8)青霉胺可用于医学上误食铜盐的解毒,解毒原理:
 形成环状配合物,其结构如图所示,该配合物无毒、易溶于水,可经尿液排出。下列说法错误的是 。
形成环状配合物,其结构如图所示,该配合物无毒、易溶于水,可经尿液排出。下列说法错误的是 。
A.共价键键角的大小关系为 |
B.电负性大小关系为 |
| C.该配合物易溶于水的主要原因是其与水可形成分子间氢键 |
D.与铜离子形成配位键强弱的大小关系为 |
您最近一年使用:0次
10 . 实验室以废铜屑(含少量Fe、不溶性杂质)为原料制取 晶体和
晶体和 晶体,其实验流程如下:
晶体,其实验流程如下:
(1)基态Cu原子核外电子排布式为______ 。
(2) 中,中心离子为
中,中心离子为_____ ,其配位数为_____ ,配体是_____ 。
(3) 中,存在的化学键有
中,存在的化学键有______ (填字母)。
a.离子键 b.非极性共价键 c.极性共价键 d.配位键 e.氢键
(4)“氧化”时,在如图所示的装置中进行。从长导管中通入氧气的作用是_______ 。保持试剂的用量不变,实验中提高反应速率的操作有______ (写一种)。该步骤首先加入一定量 的
的 溶液,再调节浓
溶液,再调节浓 的用量至
的用量至 为2.0左右时,铜粉和浓
为2.0左右时,铜粉和浓 完全反应,主要反应的化学方程式为
完全反应,主要反应的化学方程式为_______ 。硝酸过量对产品的影响为______ 。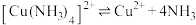 ;
; 、
、 难溶于乙醇。结合下图,
难溶于乙醇。结合下图, 在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的
在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的 溶液制备
溶液制备 晶体的实验方案补充完整:将
晶体的实验方案补充完整:将 溶液加入
溶液加入______ ,所得沉淀先用乙醇—水混合液洗涤,向最后的洗涤滤液中滴加_______ (填试剂)无沉淀生成,再将晶体用无水乙醇洗涤,放入真空干燥箱中干燥。
 晶体和
晶体和 晶体,其实验流程如下:
晶体,其实验流程如下: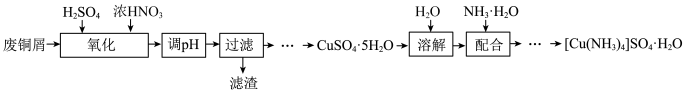
(1)基态Cu原子核外电子排布式为
(2)
 中,中心离子为
中,中心离子为(3)
 中,存在的化学键有
中,存在的化学键有a.离子键 b.非极性共价键 c.极性共价键 d.配位键 e.氢键
(4)“氧化”时,在如图所示的装置中进行。从长导管中通入氧气的作用是
 的
的 溶液,再调节浓
溶液,再调节浓 的用量至
的用量至 为2.0左右时,铜粉和浓
为2.0左右时,铜粉和浓 完全反应,主要反应的化学方程式为
完全反应,主要反应的化学方程式为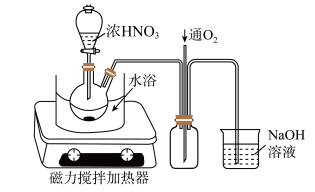
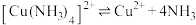 ;
; 、
、 难溶于乙醇。结合下图,
难溶于乙醇。结合下图, 在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的
在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的 溶液制备
溶液制备 晶体的实验方案补充完整:将
晶体的实验方案补充完整:将 溶液加入
溶液加入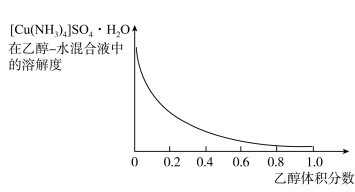
您最近一年使用:0次



