名校
解题方法
1 . 某学习小组为探究化合物 [化学式为
[化学式为 ]的性质,设计并完成如下实验:
]的性质,设计并完成如下实验:
I.取少量固体 ,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。
,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。
Ⅱ.取 固体
固体 ,按如图装置进行实验(夹持装置略,装置
,按如图装置进行实验(夹持装置略,装置 和
和 中为常见药品):
中为常见药品):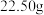 残渣
残渣 ,装置c增重
,装置c增重 ;
;
Ⅲ.将Ⅱ中的残渣B加入到水中,部分溶解,离心分离出 红色固体
红色固体 (单一成分),向溶解液中继续加水至
(单一成分),向溶解液中继续加水至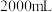 得到溶液
得到溶液 ;
;
IV.测定溶液 的
的 ,再取
,再取 溶液
溶液 加入足量的稀硫酸,得到
加入足量的稀硫酸,得到 白色沉淀
白色沉淀 。
。
V.将红色固体 溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液
溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液 。
。
回答下列问题:
(1)步骤Ⅱ中:
①装置 用石英管,而不用普通玻璃管的原因是
用石英管,而不用普通玻璃管的原因是___________ ,装置 中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置
中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置 中盛放药品的方法是
中盛放药品的方法是___________ ;装置 的作用是
的作用是___________ 。
②停止加热后的实验操作是___________ 。
(2)步骤Ⅲ中向溶解液继续加水至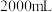 得到溶液
得到溶液 时,一定未用到下列仪器中的
时,一定未用到下列仪器中的___________ (填名称)。 的
的 的实验操作是
的实验操作是___________ ;溶液 是
是___________ (填“单一溶质”或“混合溶质”),理由是___________ 。
(4)步骤V中红色固体 溶于稀硝酸发生反应的离子方程式是
溶于稀硝酸发生反应的离子方程式是___________ 。
(5) 中的z:w=
中的z:w=___________ 。
 [化学式为
[化学式为 ]的性质,设计并完成如下实验:
]的性质,设计并完成如下实验:I.取少量固体
 ,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。
,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。Ⅱ.取
 固体
固体 ,按如图装置进行实验(夹持装置略,装置
,按如图装置进行实验(夹持装置略,装置 和
和 中为常见药品):
中为常见药品):
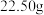 残渣
残渣 ,装置c增重
,装置c增重 ;
;Ⅲ.将Ⅱ中的残渣B加入到水中,部分溶解,离心分离出
 红色固体
红色固体 (单一成分),向溶解液中继续加水至
(单一成分),向溶解液中继续加水至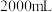 得到溶液
得到溶液 ;
;IV.测定溶液
 的
的 ,再取
,再取 溶液
溶液 加入足量的稀硫酸,得到
加入足量的稀硫酸,得到 白色沉淀
白色沉淀 。
。V.将红色固体
 溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液
溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液 。
。回答下列问题:
(1)步骤Ⅱ中:
①装置
 用石英管,而不用普通玻璃管的原因是
用石英管,而不用普通玻璃管的原因是 中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置
中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置 中盛放药品的方法是
中盛放药品的方法是 的作用是
的作用是②停止加热后的实验操作是
(2)步骤Ⅲ中向溶解液继续加水至
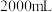 得到溶液
得到溶液 时,一定未用到下列仪器中的
时,一定未用到下列仪器中的
 的
的 的实验操作是
的实验操作是 是
是(4)步骤V中红色固体
 溶于稀硝酸发生反应的离子方程式是
溶于稀硝酸发生反应的离子方程式是(5)
 中的z:w=
中的z:w=
您最近一年使用:0次
解题方法
2 . 探究配制不同金属离子—氨配体溶液的差异性,实验操作及现象如下:
资料:①饱和氨水的浓度约为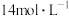
② 为浅青色沉淀
为浅青色沉淀
③ 溶液为红色,在活性炭催化下转化为橙黄色的
溶液为红色,在活性炭催化下转化为橙黄色的 溶液
溶液
(1)实验i-a中生成蓝色沉淀的离子方程式为___________ 。
(2)有研究认为蓝色沉淀中还有 成分,其可以溶于稀酸。检验蓝色沉淀中不止含
成分,其可以溶于稀酸。检验蓝色沉淀中不止含 的实验操作为:将蓝色沉淀过滤,充分洗涤后,
的实验操作为:将蓝色沉淀过滤,充分洗涤后,___________ 。(填后续操作和现象)
(3)对比实验i-a和实验i-b,从平衡移动角度,结合化学用语解释 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因___________ 。
(4)对比实验i-a和实验i-c中再加入过量氨水前的反应,推测 对
对 生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。
生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。___________ ,c=___________ 。
②实验现象是___________ 。
(5)从平衡移动角度,结合化学用语,解释 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因___________ 。
(6)针对实验ii未能成功配制 溶液,结合以上分析,提出改进方案:
溶液,结合以上分析,提出改进方案:
①在实验ii-a的基础上继续加入___________ ,即可成功配制。
②验证配制成功的操作及实验现象是:取①的上层红色清液,加入少许活性炭振荡试管,溶液转为橙黄色,反应的离子方程式为:___________ 。
(7)综合以上分析,配制不同金属离子—氨配体溶液的难易程度存在差异性,推测可能与以下因素有关:配位数、___________ 。
| 实验序号 | 操作 | 现象 | |
实验i: 的配制 的配制 | 实验i-a | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的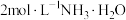 | 产生蓝色沉淀,加入 后沉淀少部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 后沉淀少部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 |
| 实验i-b | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的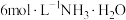 | 产生蓝色沉淀,加入 后沉淀大部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 后沉淀大部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 | |
| 实验i-c | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的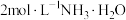 | 产生蓝色沉淀,加入 后沉淀完全溶解,得到澄清的深蓝色溶液。 后沉淀完全溶解,得到澄清的深蓝色溶液。 | |
实验ii: 的配制 的配制 | 实验ii-a | 在试管内混合 溶液和过量 溶液和过量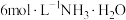 | 得到浅青色沉淀,沉淀未见明显溶解。 |
| 实验ii-b | 在试管内混合 溶液和过量 溶液和过量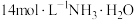 | 得到浅青色沉淀,沉淀未见明显溶解。 | |
实验iii: 的配制 的配制 | 实验iii | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的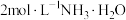 | 产生白色沉淀,加入 后沉淀完全溶解,得到无色溶液。 后沉淀完全溶解,得到无色溶液。 |
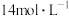
②
 为浅青色沉淀
为浅青色沉淀③
 溶液为红色,在活性炭催化下转化为橙黄色的
溶液为红色,在活性炭催化下转化为橙黄色的 溶液
溶液(1)实验i-a中生成蓝色沉淀的离子方程式为
(2)有研究认为蓝色沉淀中还有
 成分,其可以溶于稀酸。检验蓝色沉淀中不止含
成分,其可以溶于稀酸。检验蓝色沉淀中不止含 的实验操作为:将蓝色沉淀过滤,充分洗涤后,
的实验操作为:将蓝色沉淀过滤,充分洗涤后,(3)对比实验i-a和实验i-b,从平衡移动角度,结合化学用语解释
 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因(4)对比实验i-a和实验i-c中再加入过量氨水前的反应,推测
 对
对 生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。
生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。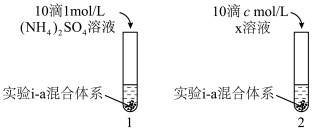
②实验现象是
(5)从平衡移动角度,结合化学用语,解释
 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因(6)针对实验ii未能成功配制
 溶液,结合以上分析,提出改进方案:
溶液,结合以上分析,提出改进方案:①在实验ii-a的基础上继续加入
②验证配制成功的操作及实验现象是:取①的上层红色清液,加入少许活性炭振荡试管,溶液转为橙黄色,反应的离子方程式为:
(7)综合以上分析,配制不同金属离子—氨配体溶液的难易程度存在差异性,推测可能与以下因素有关:配位数、
您最近一年使用:0次
3 . 某含氰废水中氰主要以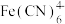 和少量
和少量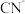 形式存在,对该废水进行除氰处理的步骤如下。
形式存在,对该废水进行除氰处理的步骤如下。
Ⅰ.取一定量处理好的铁屑和活性炭混合物(按照一定的体积比混合);
Ⅱ.加入一定体积的含氰废水,调节 值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液
值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液 ,总氰去除率接近
,总氰去除率接近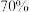 ;
;
Ⅲ.调节滤液 的
的 ,加入一定量的
,加入一定量的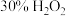 溶液,反应一段时间后过滤,得滤液
溶液,反应一段时间后过滤,得滤液 ,总氰去除率可达
,总氰去除率可达 以上;
以上;
Ⅳ.向滤液 中加入
中加入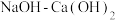 调节
调节 至
至 ,混凝沉淀,经过滤,总氰去除率接近
,混凝沉淀,经过滤,总氰去除率接近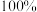 ,得到符合排放标准的废水。
,得到符合排放标准的废水。
(1)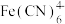 的中心离子是
的中心离子是_______ 。
(2)Ⅰ中,处理过程需用稀硫酸除去铁屑表面的氧化铁,反应的离子方程式是_______ 。
(3)步骤Ⅱ中,生成沉淀的主要成分是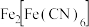 。
。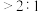 时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是:
时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是: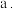 活性炭的吸附性减弱;
活性炭的吸附性减弱;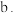
_______ 。
②反应过程中,会有部分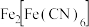 转化为
转化为 ,补全反应的离子方程式
,补全反应的离子方程式_______ 。
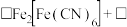 _______
_______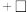 _______
_______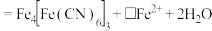
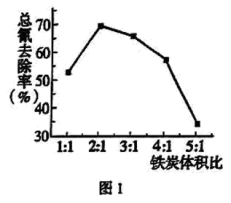
(4)步骤Ⅲ中,其他条件不变,研究 不同对滤液
不同对滤液 中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液
中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液 的
的 为4左右。
为4左右。 可将
可将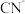 氧化为
氧化为 和
和 ,反应的离子方程式是
,反应的离子方程式是_______ 。
②当 时,随
时,随 增大,总氰去除率下降,可能的原因是
增大,总氰去除率下降,可能的原因是_______ 。
(5)在步骤Ⅳ中产生了胶体,使水中的氰经聚沉而除去。证明有胶体产生的方法是_______ 。
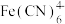 和少量
和少量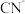 形式存在,对该废水进行除氰处理的步骤如下。
形式存在,对该废水进行除氰处理的步骤如下。Ⅰ.取一定量处理好的铁屑和活性炭混合物(按照一定的体积比混合);
Ⅱ.加入一定体积的含氰废水,调节
 值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液
值为3.5,控制曝气(即通入空气)时间,静置,反应一段时间后过滤,得滤液 ,总氰去除率接近
,总氰去除率接近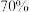 ;
;Ⅲ.调节滤液
 的
的 ,加入一定量的
,加入一定量的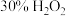 溶液,反应一段时间后过滤,得滤液
溶液,反应一段时间后过滤,得滤液 ,总氰去除率可达
,总氰去除率可达 以上;
以上;Ⅳ.向滤液
 中加入
中加入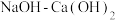 调节
调节 至
至 ,混凝沉淀,经过滤,总氰去除率接近
,混凝沉淀,经过滤,总氰去除率接近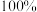 ,得到符合排放标准的废水。
,得到符合排放标准的废水。(1)
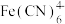 的中心离子是
的中心离子是(2)Ⅰ中,处理过程需用稀硫酸除去铁屑表面的氧化铁,反应的离子方程式是
(3)步骤Ⅱ中,生成沉淀的主要成分是
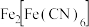 。
。
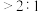 时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是:
时,随着铁炭体积比增加,相同时间内总氰去除率降低,原因是: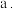 活性炭的吸附性减弱;
活性炭的吸附性减弱;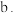
②反应过程中,会有部分
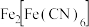 转化为
转化为 ,补全反应的离子方程式
,补全反应的离子方程式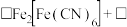 _______
_______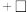 _______
_______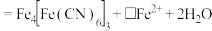
(4)步骤Ⅲ中,其他条件不变,研究
 不同对滤液
不同对滤液 中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液
中总氰去除效果的影响,结果如图2所示,依据实验结果确定应调节滤液 的
的 为4左右。
为4左右。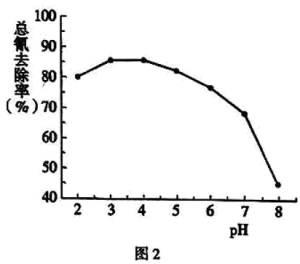
 可将
可将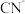 氧化为
氧化为 和
和 ,反应的离子方程式是
,反应的离子方程式是②当
 时,随
时,随 增大,总氰去除率下降,可能的原因是
增大,总氰去除率下降,可能的原因是(5)在步骤Ⅳ中产生了胶体,使水中的氰经聚沉而除去。证明有胶体产生的方法是
您最近一年使用:0次
4 . 由下列实验事实得出的结论中错误的是
| 选项 | 实验目的 | 实验事实 | 结论 |
| A | 验证牺牲阳极的阴极保护法 | 将锌片与铁片用导线相连,插入酸化的3%NaCl溶液,一段时间后在铁电极区滴入2滴K3[Fe(CN)6]溶液,出现蓝色沉淀 | 铁不一定被腐蚀 |
| B | 麦芽糖水解产物的检验 | 麦芽糖与稀硫酸共热后,加NaOH溶液调至碱性再加入新制Cu(OH)2并加热,有砖红色沉淀生成 | 麦芽糖水解生成葡萄糖 |
| C | 探究Mg和水反应 | 取一小段镁条,用砂纸除去表面氧化膜,放入试管中,加入2mL水,并滴入2滴酚酞溶液,无明显现象;再加热试管至液体沸腾,溶液变红 | Mg可以与热水反应 |
| D | 制备一水合硫酸四氨合铜 | 向[Cu(NH3)4]SO4溶液中加入无水乙醇,并用玻璃棒摩擦试管壁,有深蓝色晶体析出 | 乙醇极性小,降低了[Cu(NH3)4]SO4的溶解度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 配合物在生产、生活中应用广泛。例如, (铁氰化钾)用于检验
(铁氰化钾)用于检验 ,
, 用于检验
用于检验 。回答下列问题:
。回答下列问题:
(1)基态 的价层电子排布式为
的价层电子排布式为___________ ,向某未知溶液中滴加适量 溶液,若
溶液,若___________ (填实验现象),则说明溶液中含有 。
。
(2) 中配位原子是
中配位原子是___________ (填元素符号)。
(3)已知:络合平衡反应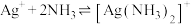 ,其平衡常数又称配离子稳定常数,
,其平衡常数又称配离子稳定常数,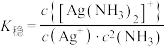 。常温下,
。常温下,
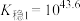 ;
;
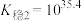 。
。
由此推知稳定性:
___________  (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是___________ 。
(4)分裂能( )定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能(
)定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能( ):
):
___________  (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是___________ 。
 (铁氰化钾)用于检验
(铁氰化钾)用于检验 ,
, 用于检验
用于检验 。回答下列问题:
。回答下列问题:(1)基态
 的价层电子排布式为
的价层电子排布式为 溶液,若
溶液,若 。
。(2)
 中配位原子是
中配位原子是(3)已知:络合平衡反应
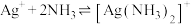 ,其平衡常数又称配离子稳定常数,
,其平衡常数又称配离子稳定常数,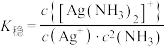 。常温下,
。常温下,
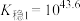 ;
;
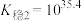 。
。由此推知稳定性:

 (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是(4)分裂能(
 )定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能(
)定义:1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,分裂能大小与配体、中心原子(或离子)有关。分裂能( ):
):
 (填“
(填“ ”“
”“ ”或“
”或“ ”),判断依据是
”),判断依据是
您最近一年使用:0次
名校
解题方法
6 . 某小组同学向 溶液中匀速滴加氨水,实验数据及现象记录如下:
溶液中匀速滴加氨水,实验数据及现象记录如下:
经检测,蓝绿色沉淀为 。下列说法正确的是
。下列说法正确的是
 溶液中匀速滴加氨水,实验数据及现象记录如下:
溶液中匀速滴加氨水,实验数据及现象记录如下:时间/s | 0~20 | 20~94 | 94~144 | 144~430 |
pH | 从5.2升高至5.9 | 从5.9升高至6.8 | 从6.8升高至9.5 | 从9.5升高至11.2 |
现象 | 无明显现象 | 产生蓝绿色沉淀,并逐渐增多 | 无明显变化 | 蓝绿色沉淀溶解,溶液变为深蓝色 |
 。下列说法正确的是
。下列说法正确的是A.0s时, 是因为 是因为 |
B.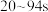 ,主要反应的离子方程式为 ,主要反应的离子方程式为 |
| C.从94s到144s,混合液中水的电离程度增大 |
D.从144s到430s,pH升高与 转化为 转化为 的反应有关 的反应有关 |
您最近一年使用:0次
7日内更新
|
145次组卷
|
2卷引用:北京市海淀区2023-2024学年高三下学期期末练习(二模)化学试题
7 . 实验装置为实验提供必要条件和测量手段。如图装置不能达到实验目的的是
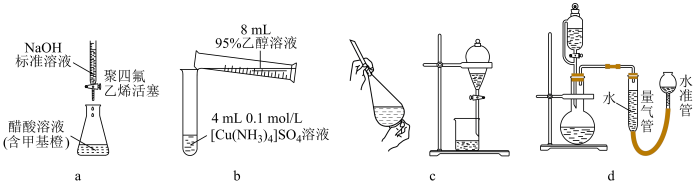
| A.图a测定醋酸溶液的浓度 |
| B.图b制备[Cu(NH3)4]SO4•H2O晶体 |
| C.图c用NaOH溶液除去溴苯中的溴单质 |
| D.图d测定一定质量的Na2O2和Na2O混合物中Na2O2的含量 |
您最近一年使用:0次
7日内更新
|
426次组卷
|
2卷引用:辽宁省重点高中协作校2024届高三下学期第二次模拟考试化学试题
8 . 下列关于物质的结构与性质或应用的描述中错误的是
| A.葡萄糖可用于玻璃等材料表面化学覆银,因为葡萄糖具有还原性 |
B.AgCl溶于氨水,是由于AgCl与 反应生成了可溶性配合物 反应生成了可溶性配合物 |
C. 比 比 的热稳定性强,因为氨分子间存在氢键 的热稳定性强,因为氨分子间存在氢键 |
D.利用 除去HCl气体中混有的 除去HCl气体中混有的 ,可从 ,可从 和 和 都是非极性分子的角度解释 都是非极性分子的角度解释 |
您最近一年使用:0次
9 . 砷化镓是一种高性能半导体材料,被广泛应用于光电子器件等领域。砷化镓立方晶胞(晶胞参数为 )如图1。下列说法正确的是
)如图1。下列说法正确的是
 )如图1。下列说法正确的是
)如图1。下列说法正确的是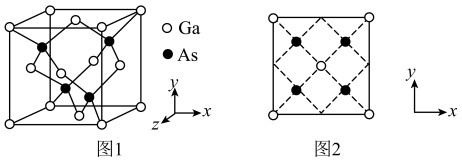
A. 的配位数为2 的配位数为2 | B.该晶胞沿z轴方向的平面投影如图2 |
| C.晶体中配位键占共价键总数的25% | D.晶胞中砷原子与镓原子间的最短距离为 |
您最近一年使用:0次
7日内更新
|
446次组卷
|
4卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
解题方法
10 . 化学与人类生产、生活息息相关。下列叙述错误的是
| A.18—冠—6分子可识别K+,因此可增大KI在苯中的溶解度 |
| B.向硫酸四氨合铜溶液中加入乙醇会析出深蓝色晶体,因为乙醇的极性比水小 |
| C.壁虎能在天花板上爬行,是因为它的细毛与墙体之间有范德华力 |
| D.“杯酚”可分离C60和C70,体现了超分子的“自组装”特性 |
您最近一年使用:0次



