名校
解题方法
1 . 甲醇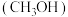 是一种用途广泛的基础有机原料和优质燃料。
是一种用途广泛的基础有机原料和优质燃料。
(1)甲醇可以在铜做催化剂的条件下直接氧化成甲醛 。
。
①基态 原子的价层电子的轨道表示式为
原子的价层电子的轨道表示式为_______ 。
②甲醛中碳原子的杂化方式为_______ 杂化,其组成元素的电负性由小到大 的顺序为_______ 。
(2)在一定条件下,甲醇可转化为乙酸甲酯 ,一个乙酸甲酯分子中
,一个乙酸甲酯分子中 键和
键和 键个数之比为
键个数之比为_______ 。
(3)由 制备的
制备的 可用于检验醛基。
可用于检验醛基。 中配位原子为
中配位原子为_______ , 的空间构型为
的空间构型为_______ 。
(4)图中银晶胞的边长为 ,该晶胞中
,该晶胞中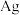 的配位数为
的配位数为_______ ;该晶胞密度为_______ 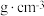 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
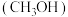 是一种用途广泛的基础有机原料和优质燃料。
是一种用途广泛的基础有机原料和优质燃料。(1)甲醇可以在铜做催化剂的条件下直接氧化成甲醛
 。
。①基态
 原子的价层电子的轨道表示式为
原子的价层电子的轨道表示式为②甲醛中碳原子的杂化方式为
(2)在一定条件下,甲醇可转化为乙酸甲酯
 ,一个乙酸甲酯分子中
,一个乙酸甲酯分子中 键和
键和 键个数之比为
键个数之比为(3)由
 制备的
制备的 可用于检验醛基。
可用于检验醛基。 中配位原子为
中配位原子为 的空间构型为
的空间构型为(4)图中银晶胞的边长为
 ,该晶胞中
,该晶胞中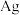 的配位数为
的配位数为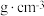 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
7日内更新
|
293次组卷
|
5卷引用:四川省成都市锦江区嘉祥外国语高级中学2023-2024学年高三下学期第二次诊断性考试化学试题
名校
解题方法
2 . 配合物在化学实验中有重要的作用,可以作为催化剂、反应中间体、反应物等参与反应,从而改变反应速率和反应路径
(1)基态Ti原子的价层电子轨道表示式为_____ 。
(2)区分晶态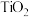 和非晶态
和非晶态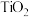 最可靠的科学方法是
最可靠的科学方法是_____ ,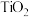 与光气
与光气 反应可用于制取四氯化钛,
反应可用于制取四氯化钛, 的空间构型为
的空间构型为_____ 。
(3)一种由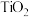 形成的一种配合物丁二酮缩邻氨基酚钛,是高性能的聚烯烃催化剂,其结构如图。
形成的一种配合物丁二酮缩邻氨基酚钛,是高性能的聚烯烃催化剂,其结构如图。_____ ,其中碳原子的杂化方式为_____ 。
②该配合物中心离子是_____ ,配位数为_____ 。
(4)已知配合物的稳定性: ,其原因是
,其原因是_____ 。
(5)一种由Mg和Fe组成的储氢材料的结构属立方晶系,晶胞参数为 ,晶胞如图所示(氢未标出)。
,晶胞如图所示(氢未标出)。 ,B点原子的分数坐标为
,B点原子的分数坐标为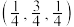 ,则C点原子的分数坐标为
,则C点原子的分数坐标为_____ 。
②该结构中,H原子以正八面体的配位模式有序分布在Fe的周围,H原子与Fe原子之间的最短距离等于晶胞参数的 ,晶胞密度为
,晶胞密度为_____  (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
(1)基态Ti原子的价层电子轨道表示式为
(2)区分晶态
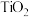 和非晶态
和非晶态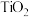 最可靠的科学方法是
最可靠的科学方法是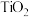 与光气
与光气 反应可用于制取四氯化钛,
反应可用于制取四氯化钛, 的空间构型为
的空间构型为(3)一种由
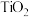 形成的一种配合物丁二酮缩邻氨基酚钛,是高性能的聚烯烃催化剂,其结构如图。
形成的一种配合物丁二酮缩邻氨基酚钛,是高性能的聚烯烃催化剂,其结构如图。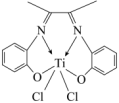
②该配合物中心离子是
(4)已知配合物的稳定性:
 ,其原因是
,其原因是(5)一种由Mg和Fe组成的储氢材料的结构属立方晶系,晶胞参数为
 ,晶胞如图所示(氢未标出)。
,晶胞如图所示(氢未标出)。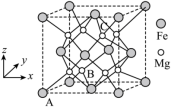
 ,B点原子的分数坐标为
,B点原子的分数坐标为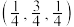 ,则C点原子的分数坐标为
,则C点原子的分数坐标为②该结构中,H原子以正八面体的配位模式有序分布在Fe的周围,H原子与Fe原子之间的最短距离等于晶胞参数的
 ,晶胞密度为
,晶胞密度为 (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
3 . 上海有机化学研究所施世良课题组以Ni(cod)2为催化剂实现了叔醇的手性合成。
(1)Ni在元素周期表中的位置是___________ ,写出其基态原子的最外层电子排布图:___________ 。
(2)Ni(cod)2是指双-(1,5-环辛二烯)镍,其结构如图所示。___________ 种。
②Ni(cod)2分子内存在的作用力有___________ (填序号)。
a.配位键 b.金属键 c.极性键 d.非极性键 e.氢键
(3)葡萄糖(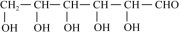 )分子中,手性碳原子个数为
)分子中,手性碳原子个数为 ___________ 。
(4)红银矿NiAs晶体结构如图所示:___________ 。
②两个As原子的原子分数坐标依次为( ,
, ,
, )和
)和___________ 。
③已知晶体密度为pg·cm-3,X射线光谱测算出的晶胞参数为a=b=m pm、c=n pm,则阿伏加德罗常数NA可表示为___________ mol-1(用含m、n和p的代数式表示)。
(1)Ni在元素周期表中的位置是
(2)Ni(cod)2是指双-(1,5-环辛二烯)镍,其结构如图所示。
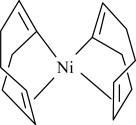
②Ni(cod)2分子内存在的作用力有
a.配位键 b.金属键 c.极性键 d.非极性键 e.氢键
(3)葡萄糖(
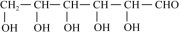 )分子中,手性碳原子个数为
)分子中,手性碳原子个数为 (4)红银矿NiAs晶体结构如图所示:
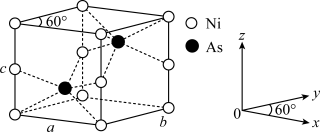
②两个As原子的原子分数坐标依次为(
 ,
, ,
, )和
)和③已知晶体密度为pg·cm-3,X射线光谱测算出的晶胞参数为a=b=m pm、c=n pm,则阿伏加德罗常数NA可表示为
您最近一年使用:0次
4 . 已知 可形成配离子
可形成配离子 、
、 、
、 。在试管中进行下列实验:
。在试管中进行下列实验:
 可形成配离子
可形成配离子 、
、 、
、 。在试管中进行下列实验:
。在试管中进行下列实验:
A.上述三种配离子中 的配位数不完全相同 的配位数不完全相同 |
B. 和 和 中配位原子均为N 中配位原子均为N |
C.溶度积常数: |
D.稳定性: |
您最近一年使用:0次
名校
解题方法
5 . W、X、Y、Z为元素周期表中的前四周期元素,原子的最外层电子数之和为12。W与X同周期相邻,X的基态原子价层电子排布为 ;Y与Z同周期,
;Y与Z同周期, 的
的 轨道半充满;四种元素可形成化合物
轨道半充满;四种元素可形成化合物 。回答下列问题:
。回答下列问题:
(1)W的三种单质分别是共价晶体、分子晶体、混合型晶体,则三种单质分别是___________ 、___________ 、___________ 。
(2)单质 化学性质很稳定,其原因是
化学性质很稳定,其原因是___________ 。 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
(3)阴离子 的结构如图所示,五个X原子位于同一平面,则X原子均采用
的结构如图所示,五个X原子位于同一平面,则X原子均采用___________ 杂化,每个X原子未参与杂化的___________ 轨道垂直于五元环平面,相互平行重叠形成大 键,
键, 中的
中的 键总数为
键总数为___________ 个,形成大 键的电子共有
键的电子共有___________ 个。 的化学式为
的化学式为___________ ,它在水中可以电离出配离子 。该配离子的中心离子是
。该配离子的中心离子是___________ ,配位数是___________ 。
(5) 有剧毒,但
有剧毒,但 却允许用作食盐的抗结剂,其最大使用量为
却允许用作食盐的抗结剂,其最大使用量为 (以配离子计),原因是
(以配离子计),原因是___________ 。
 ;Y与Z同周期,
;Y与Z同周期,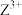 的
的 轨道半充满;四种元素可形成化合物
轨道半充满;四种元素可形成化合物 。回答下列问题:
。回答下列问题:(1)W的三种单质分别是共价晶体、分子晶体、混合型晶体,则三种单质分别是
(2)单质
 化学性质很稳定,其原因是
化学性质很稳定,其原因是 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为(3)阴离子
 的结构如图所示,五个X原子位于同一平面,则X原子均采用
的结构如图所示,五个X原子位于同一平面,则X原子均采用 键,
键, 中的
中的 键总数为
键总数为 键的电子共有
键的电子共有
 的化学式为
的化学式为 。该配离子的中心离子是
。该配离子的中心离子是(5)
 有剧毒,但
有剧毒,但 却允许用作食盐的抗结剂,其最大使用量为
却允许用作食盐的抗结剂,其最大使用量为 (以配离子计),原因是
(以配离子计),原因是
您最近一年使用:0次
名校
解题方法
6 . 下列有关物质结构和性质的说法错误的是
| A.有机物分子中手性碳所连4个原子一定不同 |
| B.互为手性异构体的两种药物,其药效差异可能很大 |
| C.邻羟基苯甲酸的沸点低于对羟基苯甲酸是因为二者形成的氢键不同 |
D.“杯酚”与 通过分子间作用力形成超分子可实现“分子识别” 通过分子间作用力形成超分子可实现“分子识别” |
您最近一年使用:0次
7 . 镁 可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:
可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:
(1)基态 原子的核外电子有
原子的核外电子有_______ 种空间运动状态,在元素周期表中, 和
和 均与
均与 相邻,这三种元素第一电离能由大到小的顺序是
相邻,这三种元素第一电离能由大到小的顺序是_______ 。
(2) 可用于
可用于 的冶炼:
的冶炼: ,基态
,基态 的价电子排布图(轨道表示式)为
的价电子排布图(轨道表示式)为_______ , 的熔点
的熔点 比
比 (714
(714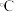 )低,其原因是
)低,其原因是_______ 。
(3)大黄素的分子结构如图所示,其中碳原子的杂化轨道类型是_______ ,分子中至少有_______ 个原子共平面,一定条件下,大黄素分子中的_______ 原子能提供孤对电子与 形成配位键。
形成配位键。 和
和 三种元素组成的晶体
三种元素组成的晶体 ,其立方晶胞如图,
,其立方晶胞如图, 与
与 的最小核间距大于
的最小核间距大于 与
与 的最小核间距,
的最小核间距, 与
与 为整数,则
为整数,则 在晶胞中的位置为
在晶胞中的位置为_______ , 的配位数是
的配位数是_______ ,若晶胞参数为 ,则晶体密度
,则晶体密度
_______  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:
可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:(1)基态
 原子的核外电子有
原子的核外电子有 和
和 均与
均与 相邻,这三种元素第一电离能由大到小的顺序是
相邻,这三种元素第一电离能由大到小的顺序是(2)
 可用于
可用于 的冶炼:
的冶炼: ,基态
,基态 的价电子排布图(轨道表示式)为
的价电子排布图(轨道表示式)为 的熔点
的熔点 比
比 (714
(714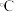 )低,其原因是
)低,其原因是(3)大黄素的分子结构如图所示,其中碳原子的杂化轨道类型是
 形成配位键。
形成配位键。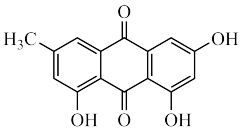
 和
和 三种元素组成的晶体
三种元素组成的晶体 ,其立方晶胞如图,
,其立方晶胞如图, 与
与 的最小核间距大于
的最小核间距大于 与
与 的最小核间距,
的最小核间距, 与
与 为整数,则
为整数,则 在晶胞中的位置为
在晶胞中的位置为 的配位数是
的配位数是 ,则晶体密度
,则晶体密度
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
8 . 铁及其化合物在生产生活中应用广泛。回答下列问题:
(1)基态Fe原子的价电子排布式是___________ 。
(2) 溶液与KSCN溶液混合,溶液呈红色,常用于检验
溶液与KSCN溶液混合,溶液呈红色,常用于检验 。
。
①基态K、S、N原子第一电离能大小顺序是___________ , 的空间构型是
的空间构型是___________ 。
②从结构角度分析 易被氧化成
易被氧化成 的原因:
的原因:___________ 。
(3)邻二氮菲( )与
)与 形成图1所示的红色配合物离子,常用于测定
形成图1所示的红色配合物离子,常用于测定 的浓度。
的浓度。___________ 。
②与邻二氮菲相比,配合物离子中∠CNC较___________ (填“大”“小”或“相同”),原因是___________ 。
③测定 浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:
浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:___________ 。
(4)铁和碳能形成图2所示的晶胞。该晶胞可以看成是在铁晶胞中插入若干碳原子,但晶胞体积不变。铁碳晶体的化学式是___________ ,铁晶体转化为铁碳晶体时晶体密度净增___________ %(结果保留2位有效数字)。
(1)基态Fe原子的价电子排布式是
(2)
 溶液与KSCN溶液混合,溶液呈红色,常用于检验
溶液与KSCN溶液混合,溶液呈红色,常用于检验 。
。①基态K、S、N原子第一电离能大小顺序是
 的空间构型是
的空间构型是②从结构角度分析
 易被氧化成
易被氧化成 的原因:
的原因:(3)邻二氮菲(
 )与
)与 形成图1所示的红色配合物离子,常用于测定
形成图1所示的红色配合物离子,常用于测定 的浓度。
的浓度。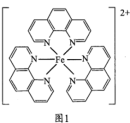
②与邻二氮菲相比,配合物离子中∠CNC较
③测定
 浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:
浓度时,加入盐酸使溶液pH不断减小,红色逐渐变浅。从化学键角度分析原因:(4)铁和碳能形成图2所示的晶胞。该晶胞可以看成是在铁晶胞中插入若干碳原子,但晶胞体积不变。铁碳晶体的化学式是

您最近一年使用:0次
解题方法
9 . 氟及其化合物用途非常广泛,自然界中氟多以化合态形式存在,形成的化合物有:N2F2、HBF4、 等。回答下列问题:
等。回答下列问题:
(1)氟元素基态原子最高能级电子的电子云形状为___________ ,下列为氟原子激发态的电子排布式的是___________ (填序号)。
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为___________ 。
②N2F2结构式为___________ ,其分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因___________ 。
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性___________ (填“增强”或“减弱”), 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的___________ (填“长”或“短”)。___________ ,设NA为阿伏加德罗常数的值则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
 等。回答下列问题:
等。回答下列问题:(1)氟元素基态原子最高能级电子的电子云形状为
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为
②N2F2结构式为
 键与
键与 键的数目之比为
键的数目之比为(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物
 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的
 (列出计算式)。
(列出计算式)。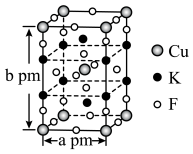
您最近一年使用:0次
名校
解题方法
10 . 以甲醇为原料,采用钴碘催化法循环制醋酸,过程如图所示。下列说法正确的是

A.总反应的原子利用率为 |
B. 和 和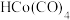 可降低该反应的活化能及反应热 可降低该反应的活化能及反应热 |
C. 与CH4为等电子体 与CH4为等电子体 |
D. 中 中 键数目 键数目 |
您最近一年使用:0次



