2024届四川省绵阳市高中高三下学期第三次诊断性考试理科综合试卷-高中化学
四川
高三
三模
2024-05-17
169次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、化学与STSE、常见无机物及其应用、认识化学科学、物质结构与性质、化学实验基础
2024届四川省绵阳市高中高三下学期第三次诊断性考试理科综合试卷-高中化学
四川
高三
三模
2024-05-17
169次
整体难度:
适中
考查范围:
化学反应原理、有机化学基础、化学与STSE、常见无机物及其应用、认识化学科学、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 化学开启美好生活每一天。下列叙述正确的是
| A.起床洗漱,使用含氟牙膏,利用水解生成的HF预防龋齿 |
| B.准备早餐,打开天然气灶,天然气与液化石油气成分相同 |
| C.穿上纯棉材质外套出门,棉、麻水解生成氨基酸和葡萄榶 |
| D.驾驶汽车上班,目前新能源汽车使用的能源有电能、氢能等 |
您最近一年使用:0次
单选题
|
较难(0.4)
名校
2. 唐代《酉阳杂俎》记载“安息香出波斯国,作药材用”。安息香转化为二苯乙二酮的过程如图,下列相关叙述正确的是
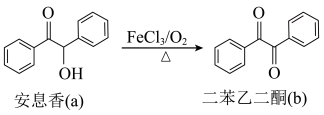
| A.a与b互为同系物 | B. 转化为 转化为 的过程属于消去反应 的过程属于消去反应 |
C. 分子中所有碳原子都可共平面 分子中所有碳原子都可共平面 | D. 分子的一氯取代产物数目相同 分子的一氯取代产物数目相同 |
您最近一年使用:0次
单选题
|
较易(0.85)
4. 设 为阿伏加爱罗常数的值。下列有关叙述正确的是
为阿伏加爱罗常数的值。下列有关叙述正确的是
 为阿伏加爱罗常数的值。下列有关叙述正确的是
为阿伏加爱罗常数的值。下列有关叙述正确的是A.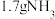 溶解于水中得到 溶解于水中得到 微粒数为 微粒数为 |
B. 号元素的原子一定含有 号元素的原子一定含有 个质子,可能含有 个质子,可能含有 个中子 个中子 |
C.常温下, 的 的 溶液中,水电离出的 溶液中,水电离出的 数为 数为 |
D.调整温度与压强,可使装有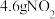 的密闭容器中的分子数目为 的密闭容器中的分子数目为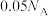 |
您最近一年使用:0次
单选题
|
较易(0.85)
5. 元素 的原子序数依次增大,
的原子序数依次增大, 可用作制冷剂,
可用作制冷剂, 和
和 能形成
能形成 型离子化合物,
型离子化合物, 的电子总数不超过40.下列叙述中正确的是
的电子总数不超过40.下列叙述中正确的是
 的原子序数依次增大,
的原子序数依次增大, 可用作制冷剂,
可用作制冷剂, 和
和 能形成
能形成 型离子化合物,
型离子化合物, 的电子总数不超过40.下列叙述中正确的是
的电子总数不超过40.下列叙述中正确的是| A.五种元素可能都位于短周期 | B.Y可以形成6种酸性氧化物 |
| C.简单氢化物的沸点: W>Z>Y | D.W最高价氧化物的水化物是强酸 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 我国科学家利用经表面修饰的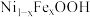 作催化剂,显著提升了光电催化水氧化反应速度。光照时,光催化电极产生电子
作催化剂,显著提升了光电催化水氧化反应速度。光照时,光催化电极产生电子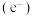 和空穴
和空穴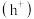 ,其反应历程如图所示。下列关于该历程的说法错误的是
,其反应历程如图所示。下列关于该历程的说法错误的是
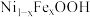 作催化剂,显著提升了光电催化水氧化反应速度。光照时,光催化电极产生电子
作催化剂,显著提升了光电催化水氧化反应速度。光照时,光催化电极产生电子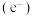 和空穴
和空穴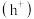 ,其反应历程如图所示。下列关于该历程的说法错误的是
,其反应历程如图所示。下列关于该历程的说法错误的是
A.I转化为II时,生成的物质 为 为 | B.III是II转化为IV过程中生成的中间体 |
| C.存在极性键的断裂和非极性键的形成 | D.反应历程中 元素的化合价未发生变化 元素的化合价未发生变化 |
您最近一年使用:0次
单选题
|
较难(0.4)
7. 新型高性能 可充电电池的工作原理如图所示,正极材料中可反复进行
可充电电池的工作原理如图所示,正极材料中可反复进行 的嵌入和脱出反应。下列说法错误的是
的嵌入和脱出反应。下列说法错误的是
 可充电电池的工作原理如图所示,正极材料中可反复进行
可充电电池的工作原理如图所示,正极材料中可反复进行 的嵌入和脱出反应。下列说法错误的是
的嵌入和脱出反应。下列说法错误的是
A.充电时, 在正极材料中发生脱出反应 在正极材料中发生脱出反应 |
B.放电时,负极反应为 |
C.放电时,转移 溶液减少 溶液减少 |
D.充电时,电池总反应为:  |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
8. 实验过程应根据具体的实验情况进行灵活设计,实验室为了提纯某粗盐样品(含有 、
、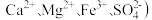 获得精盐,设计的具体步骤如下:
获得精盐,设计的具体步骤如下:
I.称取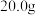 粗盐样品,加入
粗盐样品,加入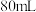 蒸馏水溶解。
蒸馏水溶解。
II.加入 溶液
溶液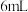 ,产生白色沉淀,加热
,产生白色沉淀,加热 ,使沉淀颗粒长大以易于沉淀。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液I。
,使沉淀颗粒长大以易于沉淀。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液I。
Ⅲ.将滤液1转移至200mL烧杯中,并加热至近沸,边搅拌,边滴加饱和Na2CO3溶液,直到不生成沉淀为止,再多加 饱和
饱和 溶液,静置。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液2。
溶液,静置。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液2。
Ⅳ.将滤液2转移至200mL烧杯中,滴加6mol/LHCl溶液,加热搅拌,调整溶液pH为3左右。
 .将调整
.将调整 后的溶液蒸发到原体积的三分之一,冷却结晶,减压过滤,然后洗涤晶体、抽干。烘干产品,得到精盐。
后的溶液蒸发到原体积的三分之一,冷却结晶,减压过滤,然后洗涤晶体、抽干。烘干产品,得到精盐。
回答下列问题:
(1)步骤I用到的玻璃仪器有烧杯、玻璃棒、_______ (填名称)和酒精灯。为保证充分溶解,采取的操作是_______ 、搅拌。
(2)步骤II确定沉淀完全的方法是_______ 。
(3)步骤III沉淀 的离子反应方程式为
的离子反应方程式为_______ ,若检验到滤液2中 未除尽,可以继续滴加合适浓度的
未除尽,可以继续滴加合适浓度的_______ 溶液加以除去。
(4)步骤IV中“加热搅拌”的目的是_______ 。
(5)步㵵V洗涤晶体可选用下列_______ 试剂(填标号),采用冷却结晶面不采取蒸发结晶的原因是_______ 。
a.无水酒精 b.少量蒸馏水 c.四氯化碳 d.二硫化碳
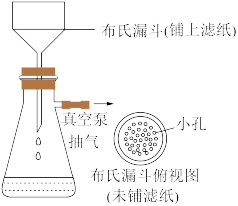
(6)减压过滤的装置如图所示,相比普通过滤的优点是_______ (写出2点)。
 、
、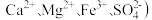 获得精盐,设计的具体步骤如下:
获得精盐,设计的具体步骤如下:I.称取
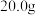 粗盐样品,加入
粗盐样品,加入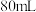 蒸馏水溶解。
蒸馏水溶解。II.加入
 溶液
溶液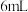 ,产生白色沉淀,加热
,产生白色沉淀,加热 ,使沉淀颗粒长大以易于沉淀。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液I。
,使沉淀颗粒长大以易于沉淀。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液I。Ⅲ.将滤液1转移至200mL烧杯中,并加热至近沸,边搅拌,边滴加饱和Na2CO3溶液,直到不生成沉淀为止,再多加
 饱和
饱和 溶液,静置。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液2。
溶液,静置。沉淀完全后,趁热减压过滤,弃去沉淀,得到滤液2。Ⅳ.将滤液2转移至200mL烧杯中,滴加6mol/LHCl溶液,加热搅拌,调整溶液pH为3左右。
 .将调整
.将调整 后的溶液蒸发到原体积的三分之一,冷却结晶,减压过滤,然后洗涤晶体、抽干。烘干产品,得到精盐。
后的溶液蒸发到原体积的三分之一,冷却结晶,减压过滤,然后洗涤晶体、抽干。烘干产品,得到精盐。回答下列问题:
(1)步骤I用到的玻璃仪器有烧杯、玻璃棒、
(2)步骤II确定沉淀完全的方法是
(3)步骤III沉淀
 的离子反应方程式为
的离子反应方程式为 未除尽,可以继续滴加合适浓度的
未除尽,可以继续滴加合适浓度的(4)步骤IV中“加热搅拌”的目的是
(5)步㵵V洗涤晶体可选用下列
a.无水酒精 b.少量蒸馏水 c.四氯化碳 d.二硫化碳
(6)减压过滤的装置如图所示,相比普通过滤的优点是
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
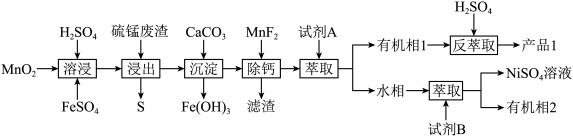
9. 硫锰废渣的主要成分是MnS,还含有NiS、CoS以及少量铁的化合物,利用常压酸浸—溶剂萃取法从硫锰废渣中回收有价金属锰、钻、镍的工艺流程如下: 与
与 均稍过量;②溶液中离子浓度小于
均稍过量;②溶液中离子浓度小于 为沉淀完全;③
为沉淀完全;③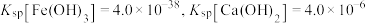 ;④
;④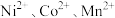 开始沉淀的
开始沉淀的 分别为7.2、7.7、8.1。
分别为7.2、7.7、8.1。
回答下列问题:
(1)“溶浸”中发生反应的还原产物是_______ (填化学式)。MnS溶于 会生成
会生成 ,但本工艺“浸出”过程中无
,但本工艺“浸出”过程中无 产生,利用离子方程式说明原因
产生,利用离子方程式说明原因_______ 。
(2)“沉淀”中调节溶液 为3.5,此时
为3.5,此时
_______ 。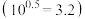
(3)“滤渣”中主要有 和
和_______ ,不能通过调节溶液的 完成“除钙”的原因是
完成“除钙”的原因是_______ 。
(4) 对萃取剂P204和P507萃取金属离子的影响如下图所示。据此推测,“产品1”中主要的金属阳离子是
对萃取剂P204和P507萃取金属离子的影响如下图所示。据此推测,“产品1”中主要的金属阳离子是_______ ,试剂B应选用_______ (填“P204”或“P507”)。 介质中,用
介质中,用 氧化
氧化 可沉淀出能用作镍镉电池正极材料的
可沉淀出能用作镍镉电池正极材料的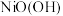 。写出该反应的离子方程式
。写出该反应的离子方程式_______ 。
 与
与 均稍过量;②溶液中离子浓度小于
均稍过量;②溶液中离子浓度小于 为沉淀完全;③
为沉淀完全;③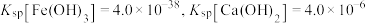 ;④
;④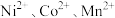 开始沉淀的
开始沉淀的 分别为7.2、7.7、8.1。
分别为7.2、7.7、8.1。回答下列问题:
(1)“溶浸”中发生反应的还原产物是
 会生成
会生成 ,但本工艺“浸出”过程中无
,但本工艺“浸出”过程中无 产生,利用离子方程式说明原因
产生,利用离子方程式说明原因(2)“沉淀”中调节溶液
 为3.5,此时
为3.5,此时
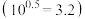
(3)“滤渣”中主要有
 和
和 完成“除钙”的原因是
完成“除钙”的原因是(4)
 对萃取剂P204和P507萃取金属离子的影响如下图所示。据此推测,“产品1”中主要的金属阳离子是
对萃取剂P204和P507萃取金属离子的影响如下图所示。据此推测,“产品1”中主要的金属阳离子是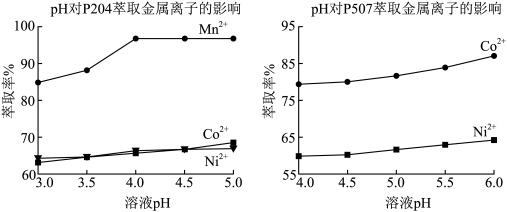
 介质中,用
介质中,用 氧化
氧化 可沉淀出能用作镍镉电池正极材料的
可沉淀出能用作镍镉电池正极材料的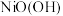 。写出该反应的离子方程式
。写出该反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
10. 异丙醇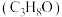 是重要的化工原料,丙烯直接水合法是工业制备异丙醇的常用方法,回答下列问题:
是重要的化工原料,丙烯直接水合法是工业制备异丙醇的常用方法,回答下列问题:
(1)丙烯直接水合法制异丙醇的反应可表示为
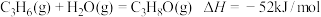
已知: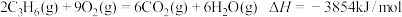
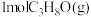 完全燃烧生成
完全燃烧生成 和
和 放出热量
放出热量_______ kJ。
(2)以上制备异丙醇反应的起始物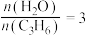 时,在不同条件下达到平衡,设体系中丙烯的转化率为
时,在不同条件下达到平衡,设体系中丙烯的转化率为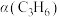 ,在
,在 ℃下的
℃下的 ,在
,在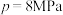 下的
下的 如图1所示:
如图1所示:_______ 。 点的反应条件为
点的反应条件为_______ ,该点的压强平衡常数
_______  。保持反应条件不变,下列可进一步提高
。保持反应条件不变,下列可进一步提高 平衡转化率的措施是(填字母)
平衡转化率的措施是(填字母)_______ 。
a.增大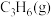 与
与 的进料比 b.充入惰性气体Ar
的进料比 b.充入惰性气体Ar
c.及时分离产品 d.换用更高效的催化剂
d.换用更高效的催化剂
(3)单程转化率反映了原料在第一次通过反应器时被转化的程度。将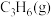 和
和 的混合气体以一定流速通过填充有催化剂的反应器,研究不同温度对
的混合气体以一定流速通过填充有催化剂的反应器,研究不同温度对 单程转化率和
单程转化率和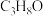 选择性的影响,结果如图2所示。由图可知,
选择性的影响,结果如图2所示。由图可知,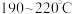 时
时 单程转化率很低,可能的原因是
单程转化率很低,可能的原因是_______ ,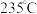 以后,随温度升高
以后,随温度升高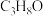 的选择性下降,可能的原因是
的选择性下降,可能的原因是_______ 。 转化为
转化为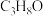 ,负极
,负极 迁移到正极,则正极上
迁移到正极,则正极上 发生的电极反应式为
发生的电极反应式为_______ 。
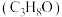 是重要的化工原料,丙烯直接水合法是工业制备异丙醇的常用方法,回答下列问题:
是重要的化工原料,丙烯直接水合法是工业制备异丙醇的常用方法,回答下列问题:(1)丙烯直接水合法制异丙醇的反应可表示为
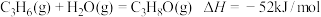
已知:
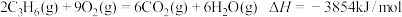
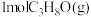 完全燃烧生成
完全燃烧生成 和
和 放出热量
放出热量(2)以上制备异丙醇反应的起始物
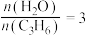 时,在不同条件下达到平衡,设体系中丙烯的转化率为
时,在不同条件下达到平衡,设体系中丙烯的转化率为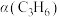 ,在
,在 ℃下的
℃下的 ,在
,在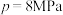 下的
下的 如图1所示:
如图1所示:
 点的反应条件为
点的反应条件为
 。保持反应条件不变,下列可进一步提高
。保持反应条件不变,下列可进一步提高 平衡转化率的措施是(填字母)
平衡转化率的措施是(填字母)a.增大
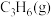 与
与 的进料比 b.充入惰性气体Ar
的进料比 b.充入惰性气体Arc.及时分离产品
 d.换用更高效的催化剂
d.换用更高效的催化剂(3)单程转化率反映了原料在第一次通过反应器时被转化的程度。将
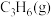 和
和 的混合气体以一定流速通过填充有催化剂的反应器,研究不同温度对
的混合气体以一定流速通过填充有催化剂的反应器,研究不同温度对 单程转化率和
单程转化率和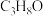 选择性的影响,结果如图2所示。由图可知,
选择性的影响,结果如图2所示。由图可知,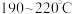 时
时 单程转化率很低,可能的原因是
单程转化率很低,可能的原因是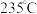 以后,随温度升高
以后,随温度升高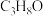 的选择性下降,可能的原因是
的选择性下降,可能的原因是
 转化为
转化为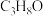 ,负极
,负极 迁移到正极,则正极上
迁移到正极,则正极上 发生的电极反应式为
发生的电极反应式为
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
11. 镁 可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:
可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:
(1)基态 原子的核外电子有
原子的核外电子有_______ 种空间运动状态,在元素周期表中, 和
和 均与
均与 相邻,这三种元素第一电离能由大到小的顺序是
相邻,这三种元素第一电离能由大到小的顺序是_______ 。
(2) 可用于
可用于 的冶炼:
的冶炼: ,基态
,基态 的价电子排布图(轨道表示式)为
的价电子排布图(轨道表示式)为_______ , 的熔点
的熔点 比
比 (714
(714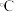 )低,其原因是
)低,其原因是_______ 。
(3)大黄素的分子结构如图所示,其中碳原子的杂化轨道类型是_______ ,分子中至少有_______ 个原子共平面,一定条件下,大黄素分子中的_______ 原子能提供孤对电子与 形成配位键。
形成配位键。 和
和 三种元素组成的晶体
三种元素组成的晶体 ,其立方晶胞如图,
,其立方晶胞如图, 与
与 的最小核间距大于
的最小核间距大于 与
与 的最小核间距,
的最小核间距, 与
与 为整数,则
为整数,则 在晶胞中的位置为
在晶胞中的位置为_______ , 的配位数是
的配位数是_______ ,若晶胞参数为 ,则晶体密度
,则晶体密度
_______  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
 可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:
可用作轻质合金,在航天器材与光学设备的生产制造方面有重要应用。回答下列问题:(1)基态
 原子的核外电子有
原子的核外电子有 和
和 均与
均与 相邻,这三种元素第一电离能由大到小的顺序是
相邻,这三种元素第一电离能由大到小的顺序是(2)
 可用于
可用于 的冶炼:
的冶炼: ,基态
,基态 的价电子排布图(轨道表示式)为
的价电子排布图(轨道表示式)为 的熔点
的熔点 比
比 (714
(714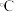 )低,其原因是
)低,其原因是(3)大黄素的分子结构如图所示,其中碳原子的杂化轨道类型是
 形成配位键。
形成配位键。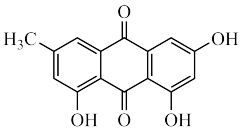
 和
和 三种元素组成的晶体
三种元素组成的晶体 ,其立方晶胞如图,
,其立方晶胞如图, 与
与 的最小核间距大于
的最小核间距大于 与
与 的最小核间距,
的最小核间距, 与
与 为整数,则
为整数,则 在晶胞中的位置为
在晶胞中的位置为 的配位数是
的配位数是 ,则晶体密度
,则晶体密度
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
解题方法
12. “百优解”被誉为传奇抗抑郁药,其化学名为盐酸氟西汀。一种利用聚合物支持的手性磺酰胺催化剂(Ligand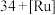 )实现不对称合成氟西汀(化合物
)实现不对称合成氟西汀(化合物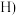 的合成路线如下所示:
的合成路线如下所示:
(1) 的化学名称为
的化学名称为_______ ,B中含氧官能团的名称是_______ 。
(2)由 生成
生成 的化学方程式为
的化学方程式为_______ 。 生成
生成 的反应条件Ⅰ可以选择
的反应条件Ⅰ可以选择_______ 。 (填标号)
a.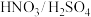 b.
b.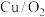 c.
c.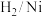 d.新制
d.新制
(3)合成路线中属于取代反应的过程有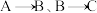 、
、_______ 和_______ 。
(4)化合物 的结构简式为
的结构简式为_______ 。化合物 与盐酸反应得到盐酸氟西汀,盐酸氟西汀的化学式应写作
与盐酸反应得到盐酸氟西汀,盐酸氟西汀的化学式应写作_______ 。
(5)已知有机物中若只含1个手性碳原子(连有4个不同的原子或原子团的碳原子),则存在两种立体异构体。满足下列条件的 的同分异构体(含立体异构)有
的同分异构体(含立体异构)有_______ 种。
①能与 发生显色反应;②苯环上仅有2个取代基;③含有—
发生显色反应;②苯环上仅有2个取代基;③含有—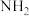 。
。
其中, 的核磁共振氢谱为5组峰,
的核磁共振氢谱为5组峰, 的结构简式为
的结构简式为_______ 。
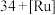 )实现不对称合成氟西汀(化合物
)实现不对称合成氟西汀(化合物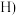 的合成路线如下所示:
的合成路线如下所示: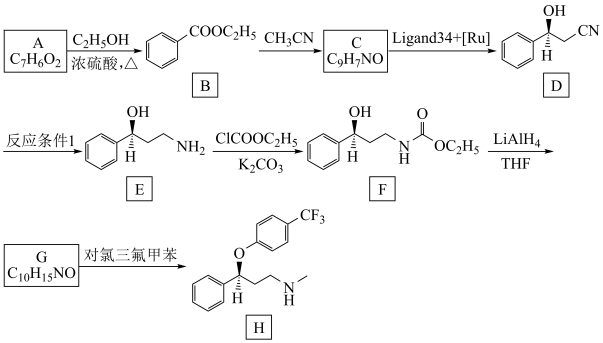
(1)
 的化学名称为
的化学名称为(2)由
 生成
生成 的化学方程式为
的化学方程式为 生成
生成 的反应条件Ⅰ可以选择
的反应条件Ⅰ可以选择a.
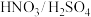 b.
b.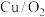 c.
c.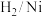 d.新制
d.新制
(3)合成路线中属于取代反应的过程有
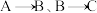 、
、(4)化合物
 的结构简式为
的结构简式为 与盐酸反应得到盐酸氟西汀,盐酸氟西汀的化学式应写作
与盐酸反应得到盐酸氟西汀,盐酸氟西汀的化学式应写作(5)已知有机物中若只含1个手性碳原子(连有4个不同的原子或原子团的碳原子),则存在两种立体异构体。满足下列条件的
 的同分异构体(含立体异构)有
的同分异构体(含立体异构)有①能与
 发生显色反应;②苯环上仅有2个取代基;③含有—
发生显色反应;②苯环上仅有2个取代基;③含有—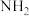 。
。其中,
 的核磁共振氢谱为5组峰,
的核磁共振氢谱为5组峰, 的结构简式为
的结构简式为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、有机化学基础、化学与STSE、常见无机物及其应用、认识化学科学、物质结构与性质、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 沉淀溶解平衡的应用 淀粉、纤维素的水解 化石能源 新能源的开发 | |
| 2 | 0.4 | 有机反应类型 同系物的判断 同分异构体的数目的确定 有机分子中原子共面的判断 | |
| 3 | 0.85 | 氯气的实验室制法 漂白粉和漂粉精的制备原理 氨气的实验室制法 二氧化硫的漂白性 | |
| 4 | 0.85 | 阿伏加德罗常数的求算 物质结构基础与NA相关推算 弱电解质在水溶液中的电离平衡 盐类水解规律理解及应用 | |
| 5 | 0.85 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 | |
| 6 | 0.65 | 氧化还原反应的几组概念 催化剂对化学反应速率的影响 共价键的形成及主要类型 | |
| 7 | 0.4 | 新型电池 原电池、电解池综合考查 电解池电极反应式及化学方程式的书写与判断 | |
| 二、解答题 | |||
| 8 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 水解的离子方程式书写 仪器使用与实验安全 物质分离、提纯综合应用 | 实验探究题 |
| 9 | 0.65 | 氧化还原反应方程式的书写与配平 溶度积常数相关计算 物质分离、提纯综合应用 萃取和分液 | 工业流程题 |
| 10 | 0.65 | 盖斯定律及其有关计算 温度对化学平衡移动的影响 转化率的相关计算及判断 | 原理综合题 |
| 11 | 0.4 | 电离能变化规律 利用杂化轨道理论判断化学键杂化类型 简单配合物的成键 晶胞的有关计算 | 结构与性质 |
| 12 | 0.4 | 有机反应类型 常见官能团名称、组成及结构 根据要求书写同分异构体 同分异构体的数目的确定 | 有机推断题 |





 漂白性
漂白性

