1 . 下列关于物质的结构或性质及解释都正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 钠与水反应比钙与水反应更剧烈 | 第一电离能: |
| B | 熔点: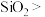 干冰 干冰 | 相对分子质量: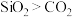 |
| C | 沸点: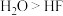 | 相同条件下, 中形成的氢键数目多于HF中的 中形成的氢键数目多于HF中的 |
| D |  与 与 分子极性相同 分子极性相同 | 二者都是由非极性键构成的分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:正戊烷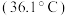 高于新戊烷 高于新戊烷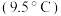 | 分子间作用力 |
| B | 熔点: | 晶体类型 |
| C | 酸性: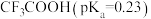 远强于 远强于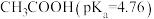 | 羟基极性 |
| D | 溶解度:甘油(丙三醇)与水互溶 | 分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列有关物质结构的说法正确的是
| A.含有不对称碳原子的分子一定是手性分子 |
| B.只含有非极性键的双原子分子一定是非极性分子 |
C.空间构型为正四面体形的分子键角一定是 |
D. 和 和 的空间构型均为直线形,两者中心原子一定为 的空间构型均为直线形,两者中心原子一定为 杂化 杂化 |
您最近一年使用:0次
解题方法
4 . 尿素 作为一种中性肥料,适用于各种土壤和植物。
作为一种中性肥料,适用于各种土壤和植物。
(1)十九世纪初,用氰酸银 与
与 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。
,实现了由无机物到有机物的合成。
① 位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为
位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为______ 。
② 与
与 中的C原子杂化方式分别为
中的C原子杂化方式分别为______ 、______ 。
(2)二十世纪初,工业上以 和
和 为原料在一定温度和压强下合成
为原料在一定温度和压强下合成 :
: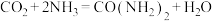 。
。
①上述物质中,属于非极性分子的是______ (填化学式)。
②键角比较:
______ (填“ ”或“
”或“ ”)
”) ,原因是
,原因是____________ 。
(3)尿素的结构和丙酮( )相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是
)相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是____________ 。
 作为一种中性肥料,适用于各种土壤和植物。
作为一种中性肥料,适用于各种土壤和植物。(1)十九世纪初,用氰酸银
 与
与 在一定条件下反应制得
在一定条件下反应制得 ,实现了由无机物到有机物的合成。
,实现了由无机物到有机物的合成。①
 位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为
位于第五周期第ⅠB族,其基态原子的价层电子轨道表示式为②
 与
与 中的C原子杂化方式分别为
中的C原子杂化方式分别为(2)二十世纪初,工业上以
 和
和 为原料在一定温度和压强下合成
为原料在一定温度和压强下合成 :
: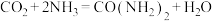 。
。①上述物质中,属于非极性分子的是
②键角比较:

 ”或“
”或“ ”)
”) ,原因是
,原因是(3)尿素的结构和丙酮(
 )相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是
)相似,相对分子质量相近,但常温下,丙酮是液体,尿素是固体,原因是
您最近一年使用:0次
解题方法
5 . 下列叙述及解释都正确的是
| 叙述 | 解释 | |
| A | 水中的溶解度:碳酸钠>碳酸氢钠 | 阴离子所带电荷数:碳酸钠>碳酸氢钠 |
| B | 三氟乙酸的酸性强于乙酸 | 相对分子质量:三氟乙酸>乙酸 |
| C | 正戊烷沸点高于新戊烷 | 新戊烷支链多,对称性好,分子间作用力小 |
| D |  与 与 分子极性相同 分子极性相同 |  与 与 都由非极性键构成 都由非极性键构成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 下列有关化学键类型的判断不正确的是
| A.s—sσ键与s—pσ键的对称性不同 |
| B.分子极性:H—F>H—Cl>H—Br>H—I |
C. 只有s—sp3σ键,其空间构型是三角锥形 只有s—sp3σ键,其空间构型是三角锥形 |
| D.H—F键是s—pσ键 |
您最近一年使用:0次
7 . 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。W、X、Y、Z、Q是核电荷数依次增大的短周期元素,W、Y原子序数之和等于Z,Y原子价电子数是Q原子价电子数的2倍。下列说法错误的是
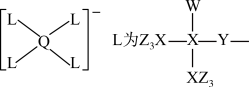
| A.W与X的化合物为极性分子 | B.第一电离能Z>X>Y |
| C.Q的氧化物是两性氧化物 | D.该阴离子中含有配位键 |
您最近一年使用:0次
名校
解题方法
8 . 物质的结构决定其性质。下列事实与解释相符的是
| 选项 | 事实 | 解释 |
| A | 一氟乙酸的 大于一溴乙酸 大于一溴乙酸 |  的电负性比 的电负性比 的大 的大 |
| B |  原子间难以形成 原子间难以形成 键 键 |  的原子半径较大,未杂化的 的原子半径较大,未杂化的 轨道很难重叠 轨道很难重叠 |
| C |  是非极性分子 是非极性分子 |  原子处在4个 原子处在4个 原子所组成的正方形中心,键的极性的向量和为零 原子所组成的正方形中心,键的极性的向量和为零 |
| D | 干冰的熔点低于 | 2个 键的键能之和小于4个 键的键能之和小于4个 键的键能之和 键的键能之和 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列叙述不正确的是
A.乳酸 分子中含有一个手性碳原子,该碳原子是 分子中含有一个手性碳原子,该碳原子是 杂化 杂化 |
B. 在水中的溶解度很小,是由于 在水中的溶解度很小,是由于 属于极性分子 属于极性分子 |
C.碘易溶于四氯化碳, 难溶于水,都可以用“相似相溶”原理解释 难溶于水,都可以用“相似相溶”原理解释 |
D. 价层电子对互斥模型为三角形,空间结构为角形,是极性分子 价层电子对互斥模型为三角形,空间结构为角形,是极性分子 |
您最近一年使用:0次
名校
解题方法
10 . a~h为元素周期表中前四周期相应元素。
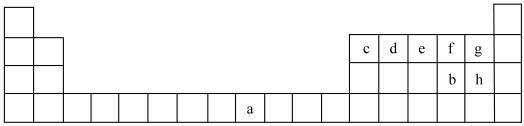
回答下列问题:
(1)元素a基态原子的价电子排布式为_______ 。
(2)元素d与b形成的稳定化合物属于_______ 分子(填“极性”或“非极性”)。
(3)df2、bf2与SiO2三个物质熔点由高到低的顺序为_______ (填化学式),理由为_______ 。
(4)化合物cg3分子的空间结构为_______ ,其中心原子的杂化方式为_______ ;键角cg3_______ eg3(填“>”“=”或“<”);a~h元素组成的含氧酸根离子中,空间结构与cg3相同的一种是_______ (填离子符号)。

回答下列问题:
(1)元素a基态原子的价电子排布式为
(2)元素d与b形成的稳定化合物属于
(3)df2、bf2与SiO2三个物质熔点由高到低的顺序为
(4)化合物cg3分子的空间结构为
您最近一年使用:0次

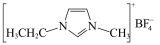 低于
低于


