名校
解题方法
1 . 下列描述正确的是
①CS2为V形的极性分子;② 的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和
的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和 的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键
的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键
①CS2为V形的极性分子;②
 的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和
的空间结构为平面三角形;③NF3键角小于NCl3的键角;④SiF4和 的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键
的中心原子均为sp3杂化;⑤HCHO分子中既含σ键又含π键| A.①②③ | B.②③④ | C.③④⑤ | D.①④⑤ |
您最近一年使用:0次
2024-04-13更新
|
241次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
2 . 某些元素在周期表中的位置如图所示,请用化学用语回答下列问题。

(1)基态b原子的电子排布式为______ ,其核外有______ 个未成对电子。
(2)基态d原子最外层电子的电子云轮廓图形状为______ 。
(3)基态h原子的价层电子排布图为______ 。

(4)e4f3可用于制造火柴,其分子结构如右图所示。该分子中f原子的杂化轨道类型为______ 。
(5)ic晶体中部分c原子被b原子替代后可以改善半导体性能。i—b键中离子键成分的百分数小于i—c键中离子键成分的百分数,原因是______ 。
(6)e4固体难溶于水,易溶于溶剂af2,原因是______ 。

(1)基态b原子的电子排布式为
(2)基态d原子最外层电子的电子云轮廓图形状为
(3)基态h原子的价层电子排布图为

(4)e4f3可用于制造火柴,其分子结构如右图所示。该分子中f原子的杂化轨道类型为
(5)ic晶体中部分c原子被b原子替代后可以改善半导体性能。i—b键中离子键成分的百分数小于i—c键中离子键成分的百分数,原因是
(6)e4固体难溶于水,易溶于溶剂af2,原因是
您最近一年使用:0次
名校
解题方法
3 . 下列关于物质的结构或性质及解释都正确的是
选项 | 物质的结构或性质 | 解释 |
A | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl的电负性,使CF3COOH的羧基中O—H的极性更大 |
B | 熔点:SiO2>CO2 | 相对分子质量:SiO2大于CO2 |
C | O2与O3分子极性相同 | 二者都是由非极性键构成的分子 |
D | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醛分子间范德华力更强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-03更新
|
426次组卷
|
3卷引用:湖南省长郡中学2023-2024学年高二下学期寒假检测(开学考试)化学试题
名校
4 . 甲醇是易燃液体,能与水、乙醇、丙酮等混溶。甲醇燃烧热为 。工业使用原料气
。工业使用原料气 、
、 气相法合成甲醇的主反应:
气相法合成甲醇的主反应: 。有少量
。有少量 存在时,会发生副反应:
存在时,会发生副反应: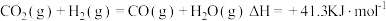 。甲醇是一种重要的工业原料,可用于制备二甲醚
。甲醇是一种重要的工业原料,可用于制备二甲醚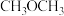 、甲醛、甲酸等有机物。下列说法正确的是
、甲醛、甲酸等有机物。下列说法正确的是
 。工业使用原料气
。工业使用原料气 、
、 气相法合成甲醇的主反应:
气相法合成甲醇的主反应: 。有少量
。有少量 存在时,会发生副反应:
存在时,会发生副反应: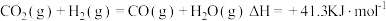 。甲醇是一种重要的工业原料,可用于制备二甲醚
。甲醇是一种重要的工业原料,可用于制备二甲醚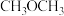 、甲醛、甲酸等有机物。下列说法正确的是
、甲醛、甲酸等有机物。下列说法正确的是A. 、 、 、 、 都属于非极性分子 都属于非极性分子 | B.用分液法分离甲醇和丙酮的二元混合物 |
| C.甲醇和二甲醚互为同分异构体 | D.甲醇和二氧化碳分子中碳原子杂化方式不同 |
您最近一年使用:0次
2024-04-02更新
|
300次组卷
|
2卷引用:江苏省海安高级中学2023-2024学年高三下学期开学考试化学试题
名校
5 . 无机物可根据其组成和性质进行分类。现有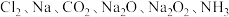 六种物质,完成下列填空:
六种物质,完成下列填空:
(1)由分子构成的单质是
(2)既有离子键又有共价键的物质的电子式为
(3)上述化合物中组成元素的原子半径由大到小的顺序是
(4)
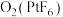 是离子化合物,其中
是离子化合物,其中 为
为 价。正确判断是___________。
价。正确判断是___________。| A.常温下为固体 | B.不存在共价键 | C.属于极性分子 | D.由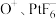 构成 构成 |
您最近一年使用:0次
名校
6 . 下列各组物质性质的比较,结论正确的是
| A.在水中的溶解度:CH3CH2Br>CH3CH2OH |
| B.溶液酸性:CF3COOH<CCl3COOH |
| C.分子的极性:BCl3>NCl3 |
| D.热稳定性:HF>H2O>NH3 |
您最近一年使用:0次
名校
解题方法
7 . 铜基催化剂Cu—M(M为 、
、 、
、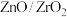 等)是
等)是 加氢制甲醇常用的催化剂,催化剂上有两个活动位点(
加氢制甲醇常用的催化剂,催化剂上有两个活动位点(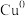 位点、氧化物载体位点),
位点、氧化物载体位点), 分别在中碱位(α)、强碱位(β)吸附发生反应,部分合成路线如图所示:
分别在中碱位(α)、强碱位(β)吸附发生反应,部分合成路线如图所示:

下列说法正确的是
 、
、 、
、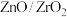 等)是
等)是 加氢制甲醇常用的催化剂,催化剂上有两个活动位点(
加氢制甲醇常用的催化剂,催化剂上有两个活动位点(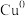 位点、氧化物载体位点),
位点、氧化物载体位点), 分别在中碱位(α)、强碱位(β)吸附发生反应,部分合成路线如图所示:
分别在中碱位(α)、强碱位(β)吸附发生反应,部分合成路线如图所示:
下列说法正确的是
A. 、 、 、 、 均为极性分子 均为极性分子 |
B. 过程中,有非极性键的断裂与形成 过程中,有非极性键的断裂与形成 |
| C.该催化剂可有效提高一定时间内产物的产率 |
D.生成 总反应的原子利用率为100% 总反应的原子利用率为100% |
您最近一年使用:0次
2024-03-18更新
|
200次组卷
|
3卷引用:甘肃省平凉市静宁县第一中学2023-2024学年高三下学期开学化学试题
解题方法
8 . 甲醛( )在Ni催化作用下加氢可得甲醇(CH3OH),以下说法错误的是
)在Ni催化作用下加氢可得甲醇(CH3OH),以下说法错误的是
 )在Ni催化作用下加氢可得甲醇(CH3OH),以下说法错误的是
)在Ni催化作用下加氢可得甲醇(CH3OH),以下说法错误的是| A.甲醛分子的空间结构为平面三角形 |
| B.甲醛分子和甲醇分子内碳原子均采取sp2杂化 |
| C.甲醛分子为极性分子 |
| D.甲醇的沸点高于甲醛的沸点 |
您最近一年使用:0次
名校
解题方法
9 . 尿素CO(NH2)2是一种高效化肥和化工原料。反应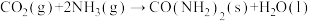 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是
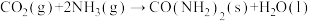 可用于尿素的制备。下列有关说法正确的是
可用于尿素的制备。下列有关说法正确的是| A.CO2分子为极性分子 | B.NH3分子的空间结构为平面三角形 |
C.H2O分子的空间填充模型 | D.尿素分子σ键和π键的数目之比为7:1 |
您最近一年使用:0次
10 . 过氧化氢是常用的氧化剂,其分子结构如右图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于 的判断错误的是
的判断错误的是
 的判断错误的是
的判断错误的是
A.电子式为 | B.属于非极性分子 |
| C.分子间存在氢键 | D.难溶于四氯化碳 |
您最近一年使用:0次
2024-03-11更新
|
112次组卷
|
2卷引用:四川省江油市太白中学2023-2024学年高二下学期开学考试化学试题



