名校
1 . NA为阿伏伽德罗常数的值,下列叙述错误的是
| A.18g H2O中含的质子数为10NA |
| B.12g 金刚石含有的共价键数为4NA |
| C.28g N2中含有π键总数为2NA |
| D.1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
您最近一年使用:0次
2 . ⑴如图为碳的一种同素异形体C60分子,每个C60分子中含有σ键的数目为___________ ;

⑵如图为碳的另一种同素异形体——金刚石的晶胞结构,D与周围4个原子形成的空间结构是_______ ,所有键角均为_______ 。

⑶硼酸(H3BO3)的结构与石墨相似如图所示,层内的分子以氢键相连,含1 mol硼酸的晶体中有_____ mol氢键。

⑷每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)有____ 个,每个Na+周围等距且紧邻的Na+有_____ 个。


⑵如图为碳的另一种同素异形体——金刚石的晶胞结构,D与周围4个原子形成的空间结构是

⑶硼酸(H3BO3)的结构与石墨相似如图所示,层内的分子以氢键相连,含1 mol硼酸的晶体中有

⑷每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)有

您最近一年使用:0次
3 . (1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_______________ 形象化描述, 基态磷原子的核外电子排布式为______________ ,有__________________ 个未成对电子, 白磷(P4)的立体构型为__________________ ,其键角为__________________ 。
(2) [Cu(NH3)4]SO4的配体为__________________ ,[Cu(H2O)4]2+中提供孤电子对的是__________________ 原子。(填元素符号)
(3)有下列六种物质:①MgCl2晶体 ②石墨 ③ SiC ④白磷(P4)晶体 ⑤金刚石 ⑥铁,其中属于离子晶体的是__________________ ,属于分子晶体的是__________________ ,属于原子晶体的化合物是__________________ 。(填序号)
(4)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在25℃,101 kPa时,16.0 g N2H4在氧气中完全燃烧生成氮气和水,放出热量312 kJ,N2H4完全燃烧的热化学方程式是__________________ 。
(2) [Cu(NH3)4]SO4的配体为
(3)有下列六种物质:①MgCl2晶体 ②石墨 ③ SiC ④白磷(P4)晶体 ⑤金刚石 ⑥铁,其中属于离子晶体的是
(4)肼(N2H4)又称联氨,是一种可燃性液体,可用作火箭燃料。已知在25℃,101 kPa时,16.0 g N2H4在氧气中完全燃烧生成氮气和水,放出热量312 kJ,N2H4完全燃烧的热化学方程式是
您最近一年使用:0次
4 . 下列说法正确的是
| A.原子晶体中只存在非极性共价键 |
| B.干冰升华时,分子内共价键会发生断裂 |
| C.稀有气体形成的晶体属于分子晶体 |
| D.金属元素和非金属元素形成的化合物一定是离子化合物 |
您最近一年使用:0次
5 . (1)比较 S 和 Cl 元素非金属性相对强弱:S__ Cl(填“<”、“>”或“=”),用离子方程式说明Cl-和 S2-失电子能力的相对强弱_____ 。
(2)CSO 是共价化合物,各原子均满足 8 电子稳定结构,写出 CSO 的电子式_____ 。
(3)常压下,石英的硬度比晶体硅的硬度大,其主要原因是_____ 。
(2)CSO 是共价化合物,各原子均满足 8 电子稳定结构,写出 CSO 的电子式
(3)常压下,石英的硬度比晶体硅的硬度大,其主要原因是
您最近一年使用:0次
名校
6 . 下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | SO2为V形分子 | SO2分子中S原子采用sp3杂化 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-06-11更新
|
131次组卷
|
3卷引用:甘肃省武威第十八中学2018-2019学年高二下学期期中考试化学试题
7 . 下列关于离子晶体的说法正确的是
| A.形成离子晶体的阴、阳离子之间只存在静电引力 |
| B.阴、阳离子的配位数只与阴、阳离子的角标比有关 |
| C.离子化合物的熔点一定比共价化合物的熔点高 |
| D.熔融状态离子键被破坏,使离子自由移动能导电 |
您最近一年使用:0次
名校
8 . 下列各组物质的熔点均与所含化学键有关的是
| A.CaO与CO2 | B.NaCl与HCl | C.MgCl2与Si | D.Cl2与I2 |
您最近一年使用:0次
2019-05-28更新
|
127次组卷
|
3卷引用:【全国百强校】福建省厦门第一中学2018-2019学年高二上学期期中考试化学试题
【全国百强校】福建省厦门第一中学2018-2019学年高二上学期期中考试化学试题(已下线)2019年6月25日《每日一题》选修3—— 物质熔、沸点高低的比较规律陕西省西安中学2021-2022学年高二下学期期中考试化学试题
2019高三·浙江·专题练习
9 . 下列有关化学用语正确的是
A.比例模型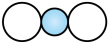 可以表示CO2分子或SiO2分子 可以表示CO2分子或SiO2分子 |
B.次氯酸的电子式: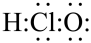 |
C.HCO3-的电离方程式:HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
| D.含18个中子的氯原子的核素符号:1735Cl |
您最近一年使用:0次
10 . 下图是氯化钠、氯化铯、二氧化硅、晶体硅的晶体结构一部分,有关晶体的叙述中,正确的是
A. SiC与二氧化硅晶体熔化时,所克服的微粒间相互作用不相同 SiC与二氧化硅晶体熔化时,所克服的微粒间相互作用不相同 |
B. 氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 氯化钠晶体中,每个Na+周围距离相等的Na+共有6个 |
C. 氯化铯晶体中,每个Cs+周围紧邻8个Cl- 氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
D. 在晶体硅中,硅原子与Si—Si键数目比为1:4 在晶体硅中,硅原子与Si—Si键数目比为1:4 |
您最近一年使用:0次



