解题方法
1 . 下列说法不正确的是
| A.熔点:NaF>MgF2>AlF3 | B.沸点:PH3<NH3<H2O |
| C.硬度:金刚石>碳化硅>晶体硅 | D.晶格能:NaF>NaCl>NaBr |
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
2 . 单质硼有无定形和晶体两种,参考表中数据。
(1)根据表中数据判断晶体硼的晶体类型属于__ 晶体。
(2)请解释金刚石的熔沸点高于晶体硅的原因是__ 。
| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点/K | >3823 | 1683 | 2573 |
| 沸点/K | 5100 | 2628 | 2823 |
| 硬度 | 10 | 7.0 | 9.5 |
(2)请解释金刚石的熔沸点高于晶体硅的原因是
您最近一年使用:0次
3 . 根据下列实验操作和现象所推导出的结论错误的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向苯酚浊液中滴加 溶液,浊液变清 溶液,浊液变清 | 苯酚的酸性强于 的酸性 的酸性 |
| B | 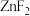 不溶于有机溶剂, 不溶于有机溶剂,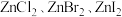 能够溶于乙醇、乙醚等有机溶剂 能够溶于乙醇、乙醚等有机溶剂 | 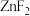 为离子化合物, 为离子化合物,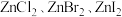 化学键以共价键为主,极性较小 化学键以共价键为主,极性较小 |
| C |  晶体的硬度大于金刚石 晶体的硬度大于金刚石 |  晶体 晶体 键长比金刚石中 键长比金刚石中 键长要短 键长要短 |
| D | 熔融 可以导电,熔融 可以导电,熔融 不能导电且易升华 不能导电且易升华 |  为离子晶体, 为离子晶体, 为分子晶体 为分子晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 碳族中的碳、硅、锗及其化合物在多领域有重要用途。
(1)基态 的电子排布式为
的电子排布式为___________ 。
(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。 分子中存在
分子中存在___________ 个 键和
键和___________ 个 键,
键, 分子是
分子是___________ 分子(填“极性”或“非极性”)。
(3)关于 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述不正确 的是___________。
(4) 与
与 -甲基咪唑(
-甲基咪唑(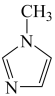 )反应可以得到
)反应可以得到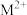 ,其结构如下图所示:
,其结构如下图所示:

 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有___________ 。
(5)汞( )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
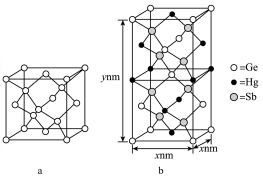
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为___________  (列出计算式)。注:
(列出计算式)。注:
(1)基态
 的电子排布式为
的电子排布式为(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
 分子中存在
分子中存在 键和
键和 键,
键, 分子是
分子是(3)关于
 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述A.键能 、 、 ,因此 ,因此 稳定性小于 稳定性小于 |
B. 是与金刚石结构相似的共价晶体,因此 是与金刚石结构相似的共价晶体,因此 具有较高的硬度 具有较高的硬度 |
C. 中 中 的化合价为 的化合价为 , , 中 中 的化合价为 的化合价为 ,因此 ,因此 还原性小于 还原性小于 |
D. 原子间难形成双键和三键而 原子间难形成双键和三键而 原子间可以,是因为 原子间可以,是因为 的原子半径大于 的原子半径大于 ,因此难以形成 ,因此难以形成 键 键 |
 与
与 -甲基咪唑(
-甲基咪唑( )反应可以得到
)反应可以得到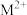 ,其结构如下图所示:
,其结构如下图所示:
 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有(5)汞(
 )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。注:
(列出计算式)。注:
您最近一年使用:0次
解题方法
5 . 下列各物质的熔点按由高到低的顺序排列的是
A.   | B. K Ca K Ca |
C.Si   | D.金刚石 硫磺 干冰 |
您最近一年使用:0次
解题方法
6 . 下列说法正确的是
| 物质 | 氧化铝 | 氯化铝 |
| 沸点/K | 2323 | 455.7 |
| A.氧化铝、氯化铝沸点相差极大,如表所示,是因为它们的晶体类型不同 |
B. 晶体中存在Na原子和氯原子 晶体中存在Na原子和氯原子 |
C.水从液态变成气态, 键断裂 键断裂 |
| D.同一主族的C和Si的最高价氧化物晶体类型相同,熔沸点相差不大 |
您最近一年使用:0次
名校
7 . 下列说法中,正确的是
| A.干冰熔化时,分子中C=O键发生断裂 |
| B.金属晶体的熔、沸点一定比分子晶体的高 |
| C.原子晶体中,共价键的键长越短,键能越大,熔点就越高 |
| D.分子晶体中,分子间作用力越大,则分子越稳定 |
您最近一年使用:0次
名校
解题方法
8 . 2019年12月17日,经中央军委批准,中国第一艘国产航母命名为“中国人民解放军海军山东舰”,舷号为“17”。2020年9月24日下午,国防部举行例行记者会,国防部新闻局副局长、国防部新闻发言人谭克非大校称:中国海军山东舰已完成例行训练和海上试验。
(1)航母用钢可由低硅生铁冶炼而成,则晶体硅、金刚石、碳化硅的熔点由高到低的顺序为___ ,原因:___ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___ 。
(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如图反应实现铜离子的富集,进行回收。
Cu2++2 →
→ +2H+
+2H+
①上述物质M中含有的作用力有___ 。
A.离子键B.金属键C.共价键D.氢键E.配位键
②X难溶于水、易溶于有机溶剂,则X晶体中铜元素与氮原子之间的共价键类型为___ 。
(1)航母用钢可由低硅生铁冶炼而成,则晶体硅、金刚石、碳化硅的熔点由高到低的顺序为
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如图反应实现铜离子的富集,进行回收。
Cu2++2
 →
→ +2H+
+2H+①上述物质M中含有的作用力有
A.离子键B.金属键C.共价键D.氢键E.配位键
②X难溶于水、易溶于有机溶剂,则X晶体中铜元素与氮原子之间的共价键类型为
您最近一年使用:0次
解题方法
9 . 下列物质的结构或性质与氢键无关的是
| A.冰的密度比水的小 | B.乙醇在水中的溶解度 |
| C.金刚石熔点高 | D.DNA的双螺旋结构 |
您最近一年使用:0次
2021-09-18更新
|
488次组卷
|
4卷引用:天津市静海区四校2020-2021学年高二下学期5月份阶段性检测化学试题
解题方法
10 . CrSi、Ge—GaAs、ZnGeAs2和碳化硅都是重要的半导体化合物,下列说法错误的是
| A.基态铬原子的价电子排布式为3d54s1 |
| B.Ge—GaAs中元素Ge、Ga、As的第一电离能由大到小的顺序为As>Ga>Ge |
| C.ZnGeAs2中元素Zn、Ge、As的电负性由大到小的顺序为As>Ge>Zn |
| D.碳化硅属于原子晶体,其熔沸点均大于晶体硅 |
您最近一年使用:0次
2021-09-11更新
|
799次组卷
|
4卷引用:湖北省新高考联考协作体2021-2022学年高三上学期起点考试化学试题



