名校
解题方法
1 . 下列对各组物质性质的比较中,不正确的是( )
| A.熔点:Li>Na>K |
| B.空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积 |
| C.密度:Na<Mg<Al |
| D.导电性:Ag>Cu>Al>Fe |
您最近一年使用:0次
名校
2 . 下列有关叙述卟啉配合物叶绿素的说法不正确的是( )
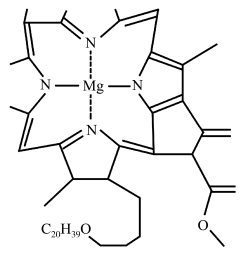

| A.该配合物的配位数为4 |
| B.该化合物所包含元素的非金属性:O>N>C>H>Mg |
| C.Mg单质晶体结构符合A3型最密堆积 |
| D.化合物中C元素的杂化方式sp2、sp3 |
您最近一年使用:0次
名校
解题方法
3 . 铁元素是最重要的金属元素之一,其不仅是各种钢材的主要成分,很多含铁化合物也具有重要意义。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于_________ 区。
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:_________ 。Mn2+的半径_________ Fe3+的半径(填“>”、“<”或“=”)。
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为_________ (用含π的式子表示)。
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为_________ ;[Fe(SCN)(H2O)5]2+中Fe3+的配位数为_________ ,H2O中氧原子的杂化方式为_________ 。
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则C5H
),则C5H 的大π键表示为
的大π键表示为________ 。二茂铁是黄色针状晶体,熔点173 ℃(在100 ℃时开始升华),沸点249 ℃,在水中难溶,但可溶于很多有机溶剂。下列相互作用中,二茂铁晶体中不存在的是________ (填标号)。
A 离子键 B 配位键 C σ 键 D 范德华力
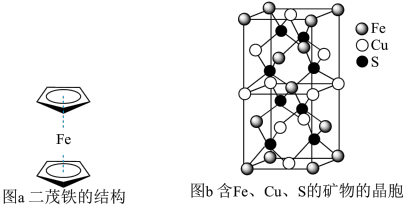
(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为_________ 。若晶胞的底面边长为A pm,高为C pm,阿伏加 德罗常数为NA,则该晶体的密度为__________ g/cm3(写出表达式)。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H
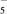 )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则C5H
),则C5H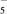 的大π键表示为
的大π键表示为A 离子键 B 配位键 C σ 键 D 范德华力

(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为
您最近一年使用:0次
2020-03-13更新
|
605次组卷
|
3卷引用:山东省临沂市临沂商城实验学校2020届高三新高考第七次阶段性模拟测试化学试题
4 . 铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法不正确的是
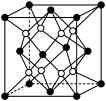

| A.铁镁合金的化学式为Mg2Fe |
| B.晶体中存在的化学键类型为共价键 |
| C.晶格能:氧化镁>氧化钙 |
D.该晶胞的质量是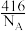 g(NA表示阿伏加 德罗常数的值) g(NA表示阿伏加 德罗常数的值) |
您最近一年使用:0次
2019-11-28更新
|
125次组卷
|
2卷引用:山东省烟台市2020届高三上学期期中考试化学试题
名校
5 . 四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是(假设金属的摩尔质量为Mg·mol-1金属原子半径为r cm,用NA表示阿伏加 德罗常数的值)
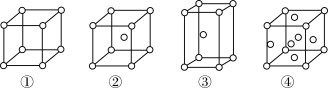

| A.金属Zn采用②堆积方式 |
| B.①和③中原子的配位数分别为:6、8 |
C.对于采用②堆积方式的金属的晶胞质量为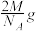 |
| D.金属锻压时,会破坏密堆积的排列方式 |
您最近一年使用:0次
2019-08-25更新
|
675次组卷
|
2卷引用:山东省德州市2018-2019学年高二下学期期末考试化学试题
名校
6 . 下列有关说法不正确的是( )
A.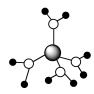 水合铜离子的模型如图所示,1个水合铜离子中有4个配位键 水合铜离子的模型如图所示,1个水合铜离子中有4个配位键 |
B.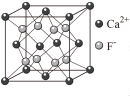 CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+ CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+ |
C. H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动 H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动 |
D. 金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12 金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12 |
您最近一年使用:0次
2019-06-04更新
|
1419次组卷
|
38卷引用:山东省德州市2021-2022学年高二下学期物质结构与性质模块综合测评化学试题
山东省德州市2021-2022学年高二下学期物质结构与性质模块综合测评化学试题2016-2017学年河南省商丘市第一高级中学高二上学期期末考试化学试卷四川省眉山中学2016-2017学年高二下学期期中考试理综化学试题安徽省合肥市第一中学2016-2017学年高二下学期期中考试化学试题山西省应县第一中学校2016-2017学年高二6月月考(月考八)化学试题福建省安溪一中、养正中学、惠安一中、泉州实验中学2016-2017学年高二下学期期末联考化学试题2018版化学(苏教版)高考总复习专题十一课时跟踪训练--微粒间作用力与物质性质宁夏石嘴山市第三中学2017-2018学年高二上学期期中考试化学试题甘肃省兰州市第一中学2017-2018学年高二下学期期中考试化学试题【全国校级联考】辽宁省六校协作体2017-2018学年高二下学期期中考试化学试题【全国百强校】山西省大同市第一中学2017-2018学年高二5月月考化学试题四川省眉山一中2017-2018学年高二下学期期中考试化学试题河南省兰考县第二高级中学2017-2018学年高二下学期期中考试化学试题【全国百强校】内蒙古北方重工业集团有限公司第三中学2017-2018学年高二下学期期末考试化学试题辽宁省实验中学2017-2018学年高二下学期期末考试化学试题福建省霞浦县第一中学2017-2018学年高二下学期第二次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二下学期期中考试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二下学期期中考试化学试题山西省吕梁市汾阳中学2018-2019学年高二下学期期中考试化学试题鲁科版高中化学选修3模块综合测评卷贵州省思南中学2018-2019学年高二下学期期末考试化学试题【全国百强校】四川省棠湖中学2018-2019学年高二下学期期末考试理综-化学试题2020高三总复习二轮复习——物质结构与性质复习卷河北省新乐市第一中学2018--2019学年高二下学期第二次月考化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题宁夏青铜峡市高级中学(吴忠中学青铜峡分校)2019-2020学年高二下学期期末考试化学试题宁夏海原县第一中学2019-2020学年高二下学期期末考试化学试题(已下线)第36讲 晶体结构与性质-2021年高考化学一轮复习名师精讲练陕西省西安市西安高新第一中学2018-2019学年高二下学期期末考试化学试题山西省朔州市怀仁县大地学校2019-2020学年高二下学期期末考试化学试题(已下线)第37讲 晶体结构与性质(精练)-2021年高考化学一轮复习讲练测新疆哈密市第八中学2019-2020学年高二下学期期末考试化学试题湖北省孝感市高级中学2020—2021学年高二下学期2月调研考试化学试题(已下线)专题18 物质结构与性质-备战2021届高考化学二轮复习题型专练江苏省盐城市东台创新高级中学2021-2022学年高二3月份月检测化学试题新疆乌鲁木齐高级中学2021-2022学年高二上学期期末考试化学试题河北省唐山市迁西县职教中心2021-2022学年高二(普职融通二部)下学期4月月考化学试题广西钦州市第一中学2022-2023学年高二下学期期中考试化学试题
名校
7 . 下列说法中,不正确的是
| A.金属晶体中一定含有金属键 |
| B.在含有阳离子的化合物的晶体中,一定含有阴离子 |
| C.含有金属元素的离子不一定是阳离子 |
| D.金属晶体中原子的堆积方式都是A3或A1型最密堆积 |
您最近一年使用:0次
2019-02-01更新
|
400次组卷
|
3卷引用:山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题
8 . 下列关于金属晶体和离子晶体的说法中错误的是 ( )
| A.都可采取“紧密堆积”的结构 | B.都含离子 |
| C.一般具有较高的熔点和沸点 | D.都能导电 |
您最近一年使用:0次
2019-01-02更新
|
152次组卷
|
4卷引用:山东省菏泽市单县第二中学2021-2022学年高二3月月考化学试题
名校
9 . 下面有关晶体的叙述中,不正确的是 ( )
| A.氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
| B.金刚石为空间网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子 |
| C.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
| D.金属铜属于六方最密堆积结构,金属镁属于面心立方最密堆积结构 |
您最近一年使用:0次
2018-11-27更新
|
237次组卷
|
3卷引用:山东省东营市一中2019-2020学年高二下学期期中考试化学试题
名校
解题方法
10 . 下列说法中,不正确的是
| A.X射线衍射实验是区别晶体与非晶体的最科学的方法 |
| B.金属键无方向性,金属晶体中原子尽可能采取紧密堆积 |
| C.凡AB3型的共价化合物,其中心原子A均采用sp2杂化轨道成键 |
| D.乙醇与水互溶可以用“相似相溶”原理和氢键来解释 |
您最近一年使用:0次
2018-04-28更新
|
299次组卷
|
3卷引用:山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题



