解题方法
1 . 已知X、Y、Z、W、R都是周期表中前四周期的元素,它们的核电荷数依次增大。X原子有1个2p空轨道,Y原子最外层电子数等于X原子核外电子总数,Z与X同主族,W原子3p轨道只有一个单电子,R3+的3d轨道为半充满状态。回答下列问题:
(1)元素X、Y、Z的电负性由大到小的顺序是__ (用元素符号表示)。
(2)元素X、Z的最简单气态氢化物的沸点由高到低的顺序是__ (用化学式表示)。
(3)元素X、Y形成的一种化合物在高温高压下所形成的晶体其晶胞如图所示,则该晶体类型属于__ 晶体,1个晶胞中含有__ 个X原子。

(4)R的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的图A~D中正确的是__ (填字母标号)。
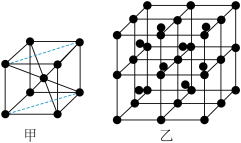
A.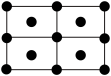 B.
B.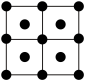 C.
C.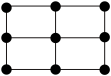 D.
D.
假设R原子的半径是apm,则该晶体的密度的计算式是__ g·cm-3(用含a的式子表示,设阿伏加 德罗常数的值为NA)。
(1)元素X、Y、Z的电负性由大到小的顺序是
(2)元素X、Z的最简单气态氢化物的沸点由高到低的顺序是
(3)元素X、Y形成的一种化合物在高温高压下所形成的晶体其晶胞如图所示,则该晶体类型属于

(4)R的一种晶体如甲、乙所示,若按甲虚线方向切乙得到的图A~D中正确的是

A.
 B.
B. C.
C. D.
D.
假设R原子的半径是apm,则该晶体的密度的计算式是
您最近一年使用:0次
解题方法
2 . 用NaBH4进行“化学镀”镀镍,可以得到坚硬、耐腐蚀的保护层(3Ni3B+Ni),反应的离子方程式为:20Ni2++16BH4-+34OH-+6H2O=2(3Ni3B+Ni)+10B(OH)4-+35H2 ,下列说法不正确的是
,下列说法不正确的是
 ,下列说法不正确的是
,下列说法不正确的是| A.1mol B(OH)4-含有σ键的数目为8NA |
| B.BH4—的立体构型是正四面体形 |
| C.B原子核外电子的运动状态和能量均不相同 |
D.Ni的晶胞结构如图所示: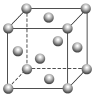 ,镍原子的配位数为12 ,镍原子的配位数为12 |
您最近一年使用:0次
名校
解题方法
3 . 铁元素是最重要的金属元素之一,其不仅是各种钢材的主要成分,很多含铁化合物也具有重要意义。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于_________ 区。
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:_________ 。Mn2+的半径_________ Fe3+的半径(填“>”、“<”或“=”)。
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为_________ (用含π的式子表示)。
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为_________ ;[Fe(SCN)(H2O)5]2+中Fe3+的配位数为_________ ,H2O中氧原子的杂化方式为_________ 。
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H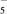 )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则C5H
),则C5H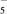 的大π键表示为
的大π键表示为________ 。二茂铁是黄色针状晶体,熔点173 ℃(在100 ℃时开始升华),沸点249 ℃,在水中难溶,但可溶于很多有机溶剂。下列相互作用中,二茂铁晶体中不存在的是________ (填标号)。
A 离子键 B 配位键 C σ 键 D 范德华力
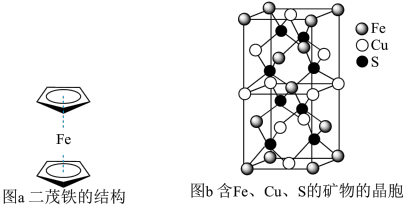
(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为_________ 。若晶胞的底面边长为A pm,高为C pm,阿伏加 德罗常数为NA,则该晶体的密度为__________ g/cm3(写出表达式)。
(1)按照电子排布,可把元素周期表中的元素划分成五个区,铁元素属于
(2)Mn2+在水溶液中难被氧化,而Fe2+则易被氧化为Fe3+ ,请从离子的价电子式角度解释Mn2+与Fe2+还原能力的差别:
(3)金属铁晶体中铁原子采用体心立方堆积,该铁晶体的空间利用率为
(4)向含Fe3+的溶液中滴加少量的KSCN溶液,溶液中生成红色的[Fe(SCN)(H2O)5]2+。N、H、O三种元素的电负性由大到小的顺序为
(5)二茂铁是一种含铁的有机化合物,其化学式为Fe(C5H5)2,可看作是Fe2+离子与两个正五边形的环戊二烯负离子(C5H
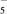 )配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π
)配体形成的夹心型分子(如下图a所示)。已知大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则C5H
),则C5H 的大π键表示为
的大π键表示为A 离子键 B 配位键 C σ 键 D 范德华力

(6)一种含有Fe、Cu、S三种元素的矿物的晶胞(如上图b所示),属于四方晶系(晶胞底面为正方形),晶胞中S原子位于内部,Fe原子位于体心和晶胞表面,Cu原子位于晶胞表面。此矿物的化学式为
您最近一年使用:0次
2020-03-13更新
|
605次组卷
|
3卷引用:山东省临沂市临沂商城实验学校2020届高三新高考第七次阶段性模拟测试化学试题
4 . 铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法不正确的是
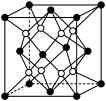

| A.铁镁合金的化学式为Mg2Fe |
| B.晶体中存在的化学键类型为共价键 |
| C.晶格能:氧化镁>氧化钙 |
D.该晶胞的质量是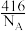 g(NA表示阿伏加 德罗常数的值) g(NA表示阿伏加 德罗常数的值) |
您最近一年使用:0次
2019-11-28更新
|
125次组卷
|
2卷引用:山东省烟台市2020届高三上学期期中考试化学试题
解题方法
5 . 下列说法中不正确的是
| A.在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
| B.在金刚石晶体中,最小碳原子环由6个碳原子构成 |
| C.在石墨晶体中,每个环上平均占有3个碳原子 |
D.银晶体晶胞如图,银原子的配位数为12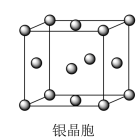 |
您最近一年使用:0次
解题方法
6 . X、Y、Z、M、W为五种原子序数递增的前36号元素。X、Y是同周期元素,原子序数相差1,价电子数之和为11;Z为第三周期元素,价电子数为2;基态M原子有6个未成对电子;W属于ds区元素,有1个未成对电子。下列说法错误的是( )
| A.原子半径:Z>X>Y,电负性:Y>X>Z |
| B.X和Y的简单氢化物分子间均存在氢键,二者均可以作为配合物中的配体 |
| C.Z(XY3)2晶体含离子键和共价键,酸根离子的中心原子杂化方式为sp2 |
| D.M为ⅥB族元素,Z单质和W单质晶体的配位数均为12,空间利用率均为68% |
您最近一年使用:0次
名校
7 . 四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是(假设金属的摩尔质量为Mg·mol-1金属原子半径为r cm,用NA表示阿伏加 德罗常数的值)
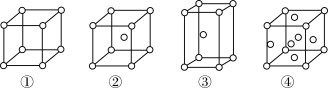

| A.金属Zn采用②堆积方式 |
| B.①和③中原子的配位数分别为:6、8 |
C.对于采用②堆积方式的金属的晶胞质量为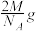 |
| D.金属锻压时,会破坏密堆积的排列方式 |
您最近一年使用:0次
2019-08-25更新
|
675次组卷
|
2卷引用:山东省德州市2018-2019学年高二下学期期末考试化学试题
名校
8 . 下列说法中,不正确的是
| A.金属晶体中一定含有金属键 |
| B.在含有阳离子的化合物的晶体中,一定含有阴离子 |
| C.含有金属元素的离子不一定是阳离子 |
| D.金属晶体中原子的堆积方式都是A3或A1型最密堆积 |
您最近一年使用:0次
2019-02-01更新
|
400次组卷
|
3卷引用:山东省枣庄市第三中学2019-2020学年高二下学期3月网上测试化学试题
9 . 下列关于金属晶体和离子晶体的说法中错误的是 ( )
| A.都可采取“紧密堆积”的结构 | B.都含离子 |
| C.一般具有较高的熔点和沸点 | D.都能导电 |
您最近一年使用:0次
2019-01-02更新
|
152次组卷
|
4卷引用:山东省菏泽市单县第二中学2021-2022学年高二3月月考化学试题
名校
解题方法
10 . 下列说法中,不正确的是
| A.X射线衍射实验是区别晶体与非晶体的最科学的方法 |
| B.金属键无方向性,金属晶体中原子尽可能采取紧密堆积 |
| C.凡AB3型的共价化合物,其中心原子A均采用sp2杂化轨道成键 |
| D.乙醇与水互溶可以用“相似相溶”原理和氢键来解释 |
您最近一年使用:0次
2018-04-28更新
|
299次组卷
|
3卷引用:山东师范大学附属中学2017-2018学年高二下学期期中考试(理)化学试题



