2021高三·浙江·专题练习
名校
解题方法
1 . 某酸性废液中含有Fe3+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对该废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
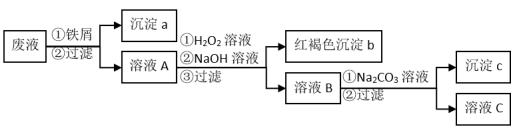
请回答:
(1)沉淀a中含有的单质是_____ 。
(2)沉淀c的化学式是_____ 。
(3)溶液A与H2O2溶液在酸性条件下反应的离子方程式是_____ 。

请回答:
(1)沉淀a中含有的单质是
(2)沉淀c的化学式是
(3)溶液A与H2O2溶液在酸性条件下反应的离子方程式是
您最近一年使用:0次
2021-10-19更新
|
347次组卷
|
3卷引用:新疆柯坪县柯坪湖州国庆中学2021-2022学年高三上学期第一次月考化学试题
新疆柯坪县柯坪湖州国庆中学2021-2022学年高三上学期第一次月考化学试题新疆乌鲁木齐市第八中学2021-2022学年高一上学期第二次月考化学试题(已下线)专题17.基础实验设计与评价-十年(2012-2021)高考化学真题分项汇编(浙江专用)
名校
2 . I对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、分液、结晶,渗析法等。请回答下列有关问题:
(1)除去食盐水中的泥沙,可用___ 的方法。
(2)2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖。生产上,可用乙醚(一种有机溶剂)提取黄花蒿中的青蒿素,该方法的名称是___ 。
(3)分离乙醇和水,可采用的方法___ 。
II用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2(HCl):试剂___ ,离子方程式为___ 。
(2)O2(CO2):试剂___ ,离子方程式为___ 。
(3)SO (CO
(CO ):试剂
):试剂___ ,离子方程式为___ 。
(1)除去食盐水中的泥沙,可用
(2)2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖。生产上,可用乙醚(一种有机溶剂)提取黄花蒿中的青蒿素,该方法的名称是
(3)分离乙醇和水,可采用的方法
II用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2(HCl):试剂
(2)O2(CO2):试剂
(3)SO
 (CO
(CO ):试剂
):试剂
您最近一年使用:0次
3 . 用于分离或提纯物质的方法有:A.蒸馏(分馏) B.萃取C.过滤 D.重结晶 E.分液。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号 )
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒___ ;
(2)分离四氯化碳与水的混合物____ ;
(3)分离汽油和煤油____ ;
(4)分离碘水中的碘单质____ ;
(5)提纯氯化钠和硝酸钾混合物中的硝酸钾____ 。
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒
(2)分离四氯化碳与水的混合物
(3)分离汽油和煤油
(4)分离碘水中的碘单质
(5)提纯氯化钠和硝酸钾混合物中的硝酸钾
您最近一年使用:0次
2021-03-25更新
|
78次组卷
|
2卷引用:新疆维吾尔自治区呼图壁县第一中学2020-2021学年高二下学期期初考试化学试题
名校
解题方法
4 . 下列是实验室常用的物质分离方法,请将合适的方法的字母填在横线上。
A.萃取分液 B.升华 C.降温结晶 D.分液 E.蒸馏 F.过滤 G.蒸发结晶
(1)分离食盐水与沙子的混合物___ ;
(2)从含有少量氯化钠的硝酸钾饱和液中获得硝酸钾___ ;
(3)分离水和CCl4的混合物___ ;
(4)分离酒精(沸点为78.5℃)和甲苯(沸点为110.6℃)两种互溶液体___ ;
(5)从含有少量碘单质的氯化钠中除去碘单质___ 。
A.萃取分液 B.升华 C.降温结晶 D.分液 E.蒸馏 F.过滤 G.蒸发结晶
(1)分离食盐水与沙子的混合物
(2)从含有少量氯化钠的硝酸钾饱和液中获得硝酸钾
(3)分离水和CCl4的混合物
(4)分离酒精(沸点为78.5℃)和甲苯(沸点为110.6℃)两种互溶液体
(5)从含有少量碘单质的氯化钠中除去碘单质
您最近一年使用:0次
名校
5 . (1)当光束通过下列物质时,会出现丁达尔效应的是_______ 。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来_______
②分离柴油和水的混合物_______
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物_______
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是_______ 。
Ⅱ、以上物质中属于非电解质的是_______ 。
Ⅲ、请写出①在水溶液中的电离方程式_______ 。
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有_______ (写仪器名称)。
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为_______ mL。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来
②分离柴油和水的混合物
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是
Ⅱ、以上物质中属于非电解质的是
Ⅲ、请写出①在水溶液中的电离方程式
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为
您最近一年使用:0次
6 . 为除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

请回答:
(1)步骤⑦需采用的主要物质分离提纯操作,名称是_______ ,所需要的玻璃仪器除酒精灯、玻璃棒、烧杯外,还要_______ 。
(2)步骤④加入过量Na2CO3的目的是_______ 。
(3)步骤⑥需加入适量的____ (填试剂名称),所发生反应的化学方程式为________ 。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
请回答:
(1)步骤⑦需采用的主要物质分离提纯操作,名称是
(2)步骤④加入过量Na2CO3的目的是
(3)步骤⑥需加入适量的
您最近一年使用:0次
解题方法
7 . (1)下列A、B、C、D、E是中学化学中常见的混合物分离或提纯的基本方法
A.蒸馏 B.过滤 C.萃取 D.蒸发 E.分液
请根据混合物分离或提纯的原理将所需正确操作的序号填入空格中:
用自来水制取蒸馏水___________ ;分离植物油和水___________ ;除去粗盐中的泥沙___________ 。
(2)实验室配制100mL 1mol/L的NaOH溶液,请回答下列问题:
①配制过程中需要的玻璃仪器除了烧杯、量筒、玻璃棒之外,还需要用到___________ 、___________ 。
②将烧杯中的溶液没有冷却就转移到容量瓶中,最后配成的溶液的物质的量浓度会___________ (填“偏大”、 “偏小”或 “无影响”)。
A.蒸馏 B.过滤 C.萃取 D.蒸发 E.分液
请根据混合物分离或提纯的原理将所需正确操作的序号填入空格中:
用自来水制取蒸馏水
(2)实验室配制100mL 1mol/L的NaOH溶液,请回答下列问题:
①配制过程中需要的玻璃仪器除了烧杯、量筒、玻璃棒之外,还需要用到
②将烧杯中的溶液没有冷却就转移到容量瓶中,最后配成的溶液的物质的量浓度会
您最近一年使用:0次
8 . 海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等。如图为海水蒸馏原理示意图,请回答下列问题:

(1)冷却水的进水口是______ (填“a”或“b”);
(2)碎瓷片的作用是______ (填“防止暴沸”或“作催化剂”)。

(1)冷却水的进水口是
(2)碎瓷片的作用是
您最近一年使用:0次
名校
9 . 根据下列装置填空
(1)分离水和植物油,选用____________ (填序号,下同)。
(2)配制100mL0.1mol·L-1NaOH溶液选用____________
(3)鉴别Na2CO3和NaHCO3固体选用____________
(4)可实现化学能直接转化为电能的是____________ ,该装置为____________ 装置,________ 作负极,外电路电子由 ________ 流向________ 。
(1)分离水和植物油,选用
(2)配制100mL0.1mol·L-1NaOH溶液选用
(3)鉴别Na2CO3和NaHCO3固体选用
(4)可实现化学能直接转化为电能的是
 |  |  |  |
| ① | ② | ③ | ④ |
您最近一年使用:0次
解题方法
10 . 由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是______ 价。 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于________ (填“酸”“碱”“盐”或“氧化物”)。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是________ (填序号)。
a.都不稳定,密封放置沉淀 b.两者均有丁达尔效应 c.分散质粒子可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的___ (填序号)。

(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于(2)明胶的水溶液和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置沉淀 b.两者均有丁达尔效应 c.分散质粒子可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的

您最近一年使用:0次
2020-10-26更新
|
77次组卷
|
2卷引用:新疆巴音郭楞蒙古自治州第一中学2022-2023学年高一上学期期中化学试卷



