22-23高一下·全国·单元测试
1 . 污水的处理方法
(1)常用的污水处理方法有_______ 、_______ 、和_______ 等。
(2)污水处理常用化学方法:_______ 、_______ 、沉淀法等。
(3)污水处理的流程
①一级处理:通常采用_______ 方法,即用格栅间、沉淀池等除去污水中不溶解的污染物。
②二级处理:采用_______ 方法(又称_______ 法)及某些化学方法,除去水中的可降解有机物等污染物。
③三级处理:主要采用_______ 、_______ 、离子交换法和_______ 等,对污水进行深度处理和净化。经过三级处理后的水可用于_______ 和_______ 用水等。
(1)常用的污水处理方法有
(2)污水处理常用化学方法:
(3)污水处理的流程
①一级处理:通常采用
②二级处理:采用
③三级处理:主要采用
您最近半年使用:0次
名校
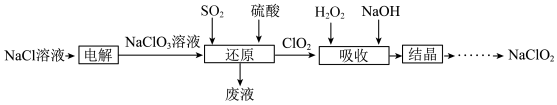
2 . NaClO2是一种重要的含氯消毒剂,也常用来漂白织物等,其一种生产工艺如下图。
(1)NaClO2中氯元素的化合价是___________ 。
(2)“电解”时,所用的食盐水可由粗盐水精制而成。精制食盐时,需除去粗盐中的Ca2+、Mg2+,加入的试剂分别为___________ 、___________ (填化学式)。
(3)“还原”中,发生反应的离子方程式为___________ 。
(4)“废液”中的主要溶质是___________ (填化学式)。
(5)“吸收”反应中,氧化剂和还原剂的物质的量之比为___________ ,该反应中氧
化产物为___________ 。
(1)NaClO2中氯元素的化合价是
(2)“电解”时,所用的食盐水可由粗盐水精制而成。精制食盐时,需除去粗盐中的Ca2+、Mg2+,加入的试剂分别为
(3)“还原”中,发生反应的离子方程式为
(4)“废液”中的主要溶质是
(5)“吸收”反应中,氧化剂和还原剂的物质的量之比为
化产物为
您最近半年使用:0次
3 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近半年使用:0次
名校
解题方法
4 . 海洋中的海带等海藻类植物具有富集碘的能力,工业上获取碘的主要流程如图所示: ,萃取碘可选择的有机试剂是___________。
,萃取碘可选择的有机试剂是___________。
硫元素和氮元素也存在于海洋中。
(2) 是海洋中硫元素的主要存在形式之一,其存在会干扰海水中
是海洋中硫元素的主要存在形式之一,其存在会干扰海水中 的检验。检验海水中
的检验。检验海水中 的方法是
的方法是___________ 。
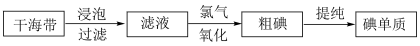
 ,萃取碘可选择的有机试剂是___________。
,萃取碘可选择的有机试剂是___________。| A.酒精 | B.苯 | C.四氯化碳 | D.乙酸 |
硫元素和氮元素也存在于海洋中。
(2)
 是海洋中硫元素的主要存在形式之一,其存在会干扰海水中
是海洋中硫元素的主要存在形式之一,其存在会干扰海水中 的检验。检验海水中
的检验。检验海水中 的方法是
的方法是
您最近半年使用:0次
名校
5 . 碳、硅及其化合物的开发由来已久,在现代生活中有广泛应用。
(1)SiO2是玻璃的主要成分之一,保存氢氟酸溶液不能使用玻璃瓶的原因是______________ (用化学方程式表示)。
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:
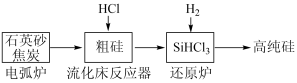
①用石英砂和焦炭在电弧炉中制粗硅,该反应的化学方程式为___________________________ 。
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和___________________ 。
(3)某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验),实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,关闭弹簧夹1,打开弹簧夹2,关闭活塞a。
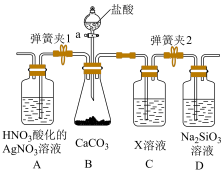
①通过步骤Ⅰ得知盐酸具有的性质是___________ (填字母)。
A.挥发性 B.还原性 C.氧化性 D.酸性
②C装置中的试剂X是______________ (写化学式)。
(1)SiO2是玻璃的主要成分之一,保存氢氟酸溶液不能使用玻璃瓶的原因是
(2)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如图:

①用石英砂和焦炭在电弧炉中制粗硅,该反应的化学方程式为
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和
物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
(3)某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验),实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,关闭弹簧夹1,打开弹簧夹2,关闭活塞a。

①通过步骤Ⅰ得知盐酸具有的性质是
A.挥发性 B.还原性 C.氧化性 D.酸性
②C装置中的试剂X是
您最近半年使用:0次
名校
解题方法
6 . 通常,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素。
海水晒盐使用的盐田法,相当于化学中的___________ 操作。
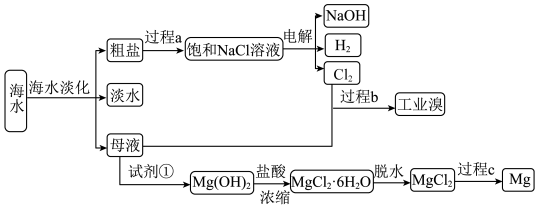
海水晒盐使用的盐田法,相当于化学中的
您最近半年使用:0次
2024高三·全国·专题练习
7 . 含氮化合物(NOx、NO 等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
 .NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。
.NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。___________ 。用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,第一步反应的化学方程式为___________ 。
 .用铁去除含氮废水中的硝酸盐(
.用铁去除含氮废水中的硝酸盐( )是重要的方法。一种去除
)是重要的方法。一种去除 的过程如图:
的过程如图:___________ 。酸化废水与铁粉反应的离子方程式是___________ 。
(3)研究发现Fe2+能与FeO(OH)反应生成Fe3O4,在去除 的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致
的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致 的去除率低。若要提高
的去除率低。若要提高 的去除率,可采取的措施是
的去除率,可采取的措施是___________ 。
 .测定某废水中
.测定某废水中 含量。先取V mL含
含量。先取V mL含 水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
已知:3Fe2++ +4H+=NO↑+3Fe3++2H2O,
+4H+=NO↑+3Fe3++2H2O,  +14H++6Fe2+=2Cr3++6Fe3++7H2O。
+14H++6Fe2+=2Cr3++6Fe3++7H2O。
(4)若需要480 mL FeSO4、K2Cr2O7标准溶液,配制时所需的仪器有天平、量筒、烧杯、玻璃棒、___________ 。
(5)加入稀硫酸的作用是___________ 。
(6)水样中NO 的含量为
的含量为___________ mol·L-1(用含c1、c2、V1、V2、V的代数式表示)。
 等)是大气主要污染物之一,消除含氮化合物的污染备受关注。
等)是大气主要污染物之一,消除含氮化合物的污染备受关注。 .NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。
.NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。NSR(NOx储存还原)工作原理:NOx的储存和还原在不同时段交替进行,如图1所示;若用H2模拟尾气中还原性气体研究Ba(NO3)2的催化还原过程,该过程分两步进行,图2表示该过程相关物质浓度随时间的变化关系。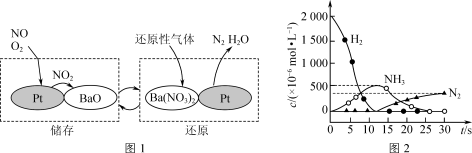
 .用铁去除含氮废水中的硝酸盐(
.用铁去除含氮废水中的硝酸盐( )是重要的方法。一种去除
)是重要的方法。一种去除 的过程如图:
的过程如图: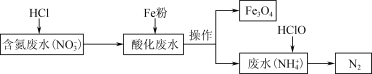
(3)研究发现Fe2+能与FeO(OH)反应生成Fe3O4,在去除
 的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致
的过程中,Fe3O4(导电)覆盖在铁粉表面,随着反应的进行,产生FeO(OH)(不导电),它覆盖在Fe3O4表面,形成钝化层,阻碍电子传输,导致 的去除率低。若要提高
的去除率低。若要提高 的去除率,可采取的措施是
的去除率,可采取的措施是 .测定某废水中
.测定某废水中 含量。先取V mL含
含量。先取V mL含 水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。
水样并将O2去除,加入催化剂、V1 mL c1 mol·L-1 FeSO4标准溶液(过量),再加入稀硫酸;最后用c2 mol·L-1的K2Cr2O7标准溶液滴定剩余的Fe2+,滴定至终点时消耗V2 mL。已知:3Fe2++
 +4H+=NO↑+3Fe3++2H2O,
+4H+=NO↑+3Fe3++2H2O,  +14H++6Fe2+=2Cr3++6Fe3++7H2O。
+14H++6Fe2+=2Cr3++6Fe3++7H2O。(4)若需要480 mL FeSO4、K2Cr2O7标准溶液,配制时所需的仪器有天平、量筒、烧杯、玻璃棒、
(5)加入稀硫酸的作用是
(6)水样中NO
 的含量为
的含量为
您最近半年使用:0次
解题方法
8 . 镍基合金是一种适宜于制造涡轮喷气发动机叶片的重要材料。某工厂用红土镍矿(主要成分为NiO,还含有FeO、 、
、 、MgO等)制取金属镍和高效催化剂黄铵铁矾
、MgO等)制取金属镍和高效催化剂黄铵铁矾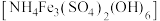 ,工艺流程如下:
,工艺流程如下: 、
、 不能氧化
不能氧化 。
。
②常温下, ,
,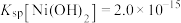 。
。
(1)提高红土镍矿“酸浸”浸取率的措施是___________ (任写一种)。
(2)滤渣的主要成分为___________ ,其重要用途为___________ (任写一种)。
(3)“氧化”时反应的离子方程式为___________ 。“沉铁”时反应的离子方程式为___________ 。
(4)“沉镁”前加入MgO将溶液pH调节至5.5~6.0的原因是___________ 。若调节pH后的溶液中 ,则至少需要加入
,则至少需要加入___________ molNaF 固体“沉镁”,使1L“沉镁”后的溶液中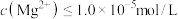 (忽略体积的变化)。
(忽略体积的变化)。
(5)工业上可用如图所示的装置电解 溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为
溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为___________ 。
 、
、 、MgO等)制取金属镍和高效催化剂黄铵铁矾
、MgO等)制取金属镍和高效催化剂黄铵铁矾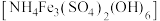 ,工艺流程如下:
,工艺流程如下: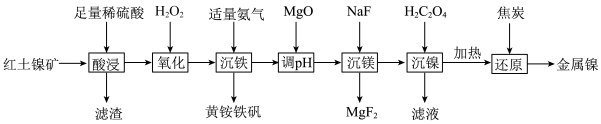
 、
、 不能氧化
不能氧化 。
。②常温下,
 ,
,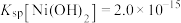 。
。(1)提高红土镍矿“酸浸”浸取率的措施是
(2)滤渣的主要成分为
(3)“氧化”时反应的离子方程式为
(4)“沉镁”前加入MgO将溶液pH调节至5.5~6.0的原因是
 ,则至少需要加入
,则至少需要加入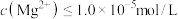 (忽略体积的变化)。
(忽略体积的变化)。(5)工业上可用如图所示的装置电解
 溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为
溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为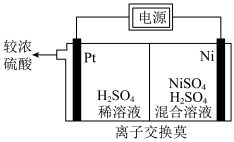
您最近半年使用:0次
名校
9 . 非金属元素与人类的生产生活关系密切,根据常见非金属元素及其化合物的性质回答下列问题。
(1)硅酸盐材料是传统无机非金属材料,硅酸盐具有特殊的性质与应用。下列产品属于硅酸盐的是_______ (填序号)。
①玻璃②陶瓷③水晶④硅芯片⑤光导纤维⑥水泥⑦砖瓦
(2)①实验室盛放氢氧化钠溶液的试剂瓶采用橡胶塞的原因是:_______ (用化学方程式表示)。
②熔化烧碱应选用的坩埚为_______ (填字母)。
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
(3)工业废气中往往含有 、
、 、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含
、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含 、
、 、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源:
、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源:_______ (填化学式)。
②工业废气中的 可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为
可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为_______ 。
③适量空气的作用是_______ 。
④吸收剂吸收的气体是_______ (填化学式),在汽车排气管安装催化转化装置,可使该气体和NO相互作用生成两种无污染气体,反应的化学方程式为_______ 。
(1)硅酸盐材料是传统无机非金属材料,硅酸盐具有特殊的性质与应用。下列产品属于硅酸盐的是
①玻璃②陶瓷③水晶④硅芯片⑤光导纤维⑥水泥⑦砖瓦
(2)①实验室盛放氢氧化钠溶液的试剂瓶采用橡胶塞的原因是:
②熔化烧碱应选用的坩埚为
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
(3)工业废气中往往含有
 、
、 、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含
、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含 、
、 、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源:
、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源: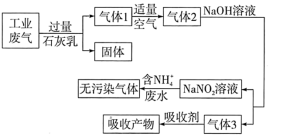
②工业废气中的
 可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为
可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为③适量空气的作用是
④吸收剂吸收的气体是
您最近半年使用:0次
10 . 从煤和石油中可得到多种常用燃料,将下列物质的转化或分离方法的序号填在横线上。
①分馏②液化③气化④裂化⑤裂解⑥干馏⑦蒸馏(每项只填写一种方法)
(1)用石油制取乙烯_____ 。
(2)从原油中分离出汽油、煤油、柴油等_____ 。
(3)将重油转化为汽油_____ 。
(4)把煤转化为焦炉气、煤焦油和焦炭等_____ 。
①分馏②液化③气化④裂化⑤裂解⑥干馏⑦蒸馏(每项只填写一种方法)
(1)用石油制取乙烯
(2)从原油中分离出汽油、煤油、柴油等
(3)将重油转化为汽油
(4)把煤转化为焦炉气、煤焦油和焦炭等
您最近半年使用:0次



