名校
1 . 已知环己胺(液体)微溶于水。实验室分离溴、溴苯、环己胺混合溶液的流程如图。下列说法正确的是
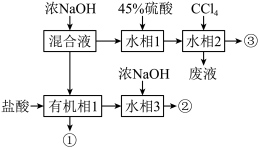
| A.上述过程未发生氧化还原反应 | B.②③均为两相混合体系 |
| C.溴、溴苯、环己胺依次由③②①得到 | D.由②③获得相应产品采取的操作方法不同 |
您最近一年使用:0次
2024-05-21更新
|
357次组卷
|
3卷引用:选择题6-10
解题方法
2 . 下列实验装置使用不正确 的是

| A.图1装置用于色谱法,可确定有机物的结构 |
| B.图2装置用于1-溴丁烷的消去反应 |
| C.图3装置用于用于酯化反应,其中长直导管起冷凝作用 |
| D.图4装置用于中和反应反应热的测定 |
您最近一年使用:0次
解题方法
3 . 斑铜矿(主要成分是Cu5FeS4,含少量SiO2)是自然界中最丰富的含铜矿物之一,以斑铜矿为原料可实现如下转化。
②Cu+酸性条件发生自身氧化还原反应生成Cu2+和Cu。
③ 加热时易失去NH3。
加热时易失去NH3。
请回答:
(1)①溶液A中加试剂X可实现FeCl3的循环利用,则试剂X是_______ 。
②固体C可通过溶解、过滤、蒸馏等操作分离出硫单质,溶解时最适宜的溶剂为_______ 。
A.水 B.NaOH溶液 C.CS2 D.酒精
(2)步骤Ⅱ需快速将固体B投入到NaCl溶液中,原因是_______ 。
(3)写出溶液D中的所有阳离子_______ 。
(4)写出反应I的离子方程式_______ 。
(5)将斑铜矿在有氧条件下用氨水浸出,可制得 晶体,反应原理为
晶体,反应原理为 (未配平)。设计由浸出液制取
(未配平)。设计由浸出液制取 晶体的实验方案:
晶体的实验方案:_______ 。

②Cu+酸性条件发生自身氧化还原反应生成Cu2+和Cu。
③
 加热时易失去NH3。
加热时易失去NH3。请回答:
(1)①溶液A中加试剂X可实现FeCl3的循环利用,则试剂X是
②固体C可通过溶解、过滤、蒸馏等操作分离出硫单质,溶解时最适宜的溶剂为
A.水 B.NaOH溶液 C.CS2 D.酒精
(2)步骤Ⅱ需快速将固体B投入到NaCl溶液中,原因是
(3)写出溶液D中的所有阳离子
(4)写出反应I的离子方程式
(5)将斑铜矿在有氧条件下用氨水浸出,可制得
 晶体,反应原理为
晶体,反应原理为 (未配平)。设计由浸出液制取
(未配平)。设计由浸出液制取 晶体的实验方案:
晶体的实验方案:
您最近一年使用:0次
4 . 某化学兴趣小组利用KBr废液制备溴单质,其流程如图所示(“氧化1”时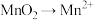 )。下列说法正确的是
)。下列说法正确的是
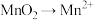 )。下列说法正确的是
)。下列说法正确的是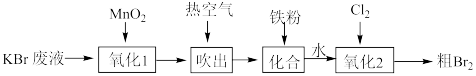
| A.“吹出”时涉及氧化还原反应 |
| B.可用乙醇从溴水中萃取溴 |
C.“氧化1”时若1 mol 发生反应,则转移4 mol电子 发生反应,则转移4 mol电子 |
D.“氧化2”时发生反应 |
您最近一年使用:0次
5 . 某固态化合物Y的组成为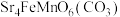 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化: 均不能形成配合物。请回答:
均不能形成配合物。请回答:
(1)写出溶液C中的所有阳离子____________ 。
(2)步骤V中的反应为 ,请说明
,请说明 能够较完全转化为
能够较完全转化为 的两个原因是:①生成
的两个原因是:①生成 降低了体系的能量;②
降低了体系的能量;②____________ 。
(3)下列说法正确的是____________。
(4)固体Y可与 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式____________ 。
(5)设计实验方案检验气体中除 以外的两种主要成分
以外的两种主要成分____________ 。
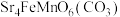 ,以Y为原料可实现如下转化:
,以Y为原料可实现如下转化: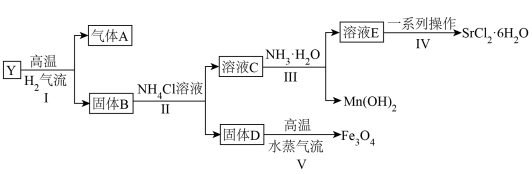
 均不能形成配合物。请回答:
均不能形成配合物。请回答:(1)写出溶液C中的所有阳离子
(2)步骤V中的反应为
 ,请说明
,请说明 能够较完全转化为
能够较完全转化为 的两个原因是:①生成
的两个原因是:①生成 降低了体系的能量;②
降低了体系的能量;②(3)下列说法正确的是____________。
A.固体B中含有 单质 单质 |
B.步骤Ⅱ反应促进了 水解平衡正向移动 水解平衡正向移动 |
C.步骤Ⅲ可推断碱性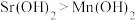 |
D.直接加热 不能得到 不能得到 |
(4)固体Y可与
 溶液反应,写出该反应的离子方程式
溶液反应,写出该反应的离子方程式(5)设计实验方案检验气体中除
 以外的两种主要成分
以外的两种主要成分
您最近一年使用:0次
2024-05-12更新
|
320次组卷
|
3卷引用:T18-无机推断题
6 . 金属 可以在高温条件下还原
可以在高温条件下还原 制备熔点较高金属
制备熔点较高金属 ,金属
,金属 是一种重要的航空材料,其性质稳定,常温下不与稀盐酸反应;工业用镁还原
是一种重要的航空材料,其性质稳定,常温下不与稀盐酸反应;工业用镁还原 制备金属
制备金属 ,工艺流程如图。下列说法
,工艺流程如图。下列说法不正确 的是
 可以在高温条件下还原
可以在高温条件下还原 制备熔点较高金属
制备熔点较高金属 ,金属
,金属 是一种重要的航空材料,其性质稳定,常温下不与稀盐酸反应;工业用镁还原
是一种重要的航空材料,其性质稳定,常温下不与稀盐酸反应;工业用镁还原 制备金属
制备金属 ,工艺流程如图。下列说法
,工艺流程如图。下列说法
A.工业上可通过电解熔融 制取金属 制取金属 |
B.用金属 还原 还原 过程中需要通入 过程中需要通入 作保护气 作保护气 |
C.“真空蒸馏”的目的是使 、 、 气化,实现与 气化,实现与 的分离 的分离 |
D.制得海绵针中含有少量金属 ,可以用稀盐酸浸泡除 ,可以用稀盐酸浸泡除 |
您最近一年使用:0次
7 . 黄铜矿的主要成分为 ,以
,以 为原料实现如下转化。
为原料实现如下转化。
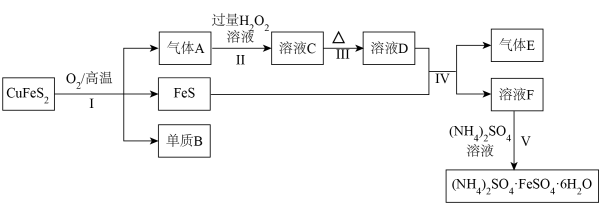
请回答:
(1)步骤Ⅰ的化学方程式是__________ 。
步骤Ⅲ的目的是__________ 。
步骤Ⅴ的操作是蒸发浓缩、冷却结晶,据此可以推测F的溶质、 和
和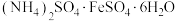 中溶解度最小的是
中溶解度最小的是__________ 。
(2)下列说法正确的是__________。
(3)设计实验方案证明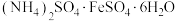 中金属阳离子
中金属阳离子__________ 。
 ,以
,以 为原料实现如下转化。
为原料实现如下转化。
请回答:
(1)步骤Ⅰ的化学方程式是
步骤Ⅲ的目的是
步骤Ⅴ的操作是蒸发浓缩、冷却结晶,据此可以推测F的溶质、
 和
和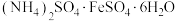 中溶解度最小的是
中溶解度最小的是(2)下列说法正确的是__________。
| A.气体A是常见的漂白剂 |
| B.单质B和溶液C不能发生反应 |
C.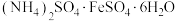 可以用作污水处理的混凝剂 可以用作污水处理的混凝剂 |
| D.气体E的水溶液在空气中长期放置易变质 |
(3)设计实验方案证明
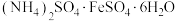 中金属阳离子
中金属阳离子
您最近一年使用:0次
2024-04-18更新
|
282次组卷
|
3卷引用:T18-无机推断题
解题方法
8 . 过氧化钙( )微溶于水,碱性条件下较稳定,可作为医用防腐剂和消毒剂,也可作为改良剂为农业、园艺和生物技术应用提供氧气。以下是一种实验室制备较高纯度过氧化钙的流程图:
)微溶于水,碱性条件下较稳定,可作为医用防腐剂和消毒剂,也可作为改良剂为农业、园艺和生物技术应用提供氧气。以下是一种实验室制备较高纯度过氧化钙的流程图: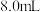 盐酸,所用的仪器是___________。
盐酸,所用的仪器是___________。
(2)下列说法正确的是___________。
(3)写出步骤Ⅲ发生反应的化学方程式___________ ,步骤Ⅲ采用冰水浴可提高产率,其原因有(回答两点)___________ 。
(4)准确称取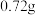 产品配成
产品配成 溶液。取
溶液。取 溶液,加入
溶液,加入 醋酸溶液和2-3滴
醋酸溶液和2-3滴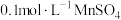 溶液,用
溶液,用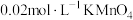 标准溶液滴定至浅红色,半分钟不褪色;平行测定3次,消耗
标准溶液滴定至浅红色,半分钟不褪色;平行测定3次,消耗 标准溶液的平均值为
标准溶液的平均值为 。
。
① 溶液的作用是
溶液的作用是___________ 。
② 的纯度为
的纯度为___________ 。
 )微溶于水,碱性条件下较稳定,可作为医用防腐剂和消毒剂,也可作为改良剂为农业、园艺和生物技术应用提供氧气。以下是一种实验室制备较高纯度过氧化钙的流程图:
)微溶于水,碱性条件下较稳定,可作为医用防腐剂和消毒剂,也可作为改良剂为农业、园艺和生物技术应用提供氧气。以下是一种实验室制备较高纯度过氧化钙的流程图:
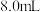 盐酸,所用的仪器是___________。
盐酸,所用的仪器是___________。A. 量筒 量筒 | B. 量筒 量筒 |
C. 碱式滴定管 碱式滴定管 | D. 烧杯 烧杯 |
(2)下列说法正确的是___________。
| A.步骤I中应使用过量的盐酸,以提高碳酸钙的利用率 |
| B.步骤Ⅱ中的煮沸操作的主要目的是加快反应速率 |
| C.步骤Ⅲ中的混合操作,应将氯化钙溶液滴入氨水-双氧水混合液中 |
| D.步骤V中可用冰水洗涤 |
(3)写出步骤Ⅲ发生反应的化学方程式
(4)准确称取
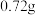 产品配成
产品配成 溶液。取
溶液。取 溶液,加入
溶液,加入 醋酸溶液和2-3滴
醋酸溶液和2-3滴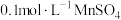 溶液,用
溶液,用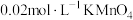 标准溶液滴定至浅红色,半分钟不褪色;平行测定3次,消耗
标准溶液滴定至浅红色,半分钟不褪色;平行测定3次,消耗 标准溶液的平均值为
标准溶液的平均值为 。
。①
 溶液的作用是
溶液的作用是②
 的纯度为
的纯度为
您最近一年使用:0次
解题方法
9 . 硫代尿素 是重要的工业原料.某小组按如图流程开展制备实验(部分装置及夹持仪器已省略)。主要反应:
是重要的工业原料.某小组按如图流程开展制备实验(部分装置及夹持仪器已省略)。主要反应:
步骤Ⅱ: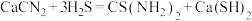
步骤Ⅲ: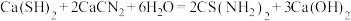
已知:硫代尿素 可溶于水、乙醇,微溶于乙醚
可溶于水、乙醇,微溶于乙醚_________ (填仪器名称)。
(2)下列说法不正确的是_________。
(3)步骤Ⅰ、Ⅱ、Ⅲ的部分操作如下,其正确的顺序是:________ 。
(_________)→(_________)→a→(_________)→e→f→(_________)
c.调节装置B温控磁力搅拌器,并控制温度为
d.调节装置B温控磁力搅拌器,并迅速控温在
g.检测气体纯净后连接三通阀
(4)步骤Ⅳ的主要 操作是(请补上第一步):_________ →洗涤、合并滤液→冷冻结晶。
上述步骤中的最适宜洗涤剂是_________ 。
A.冷水 B.热水 C.乙醚 D.滤液
(5)产品含量的测定:
滴定反应: ;
;
主要步骤:
Ⅰ.称取 产品用蒸馏水溶解并定容至
产品用蒸馏水溶解并定容至 。移取该溶液
。移取该溶液 注入碘量瓶中,加
注入碘量瓶中,加 碘标准液,
碘标准液, 氢氧化钠溶液,于暗处放置
氢氧化钠溶液,于暗处放置 。加适量水及盐酸摇匀,用
。加适量水及盐酸摇匀,用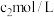 硫代硫酸钠标准溶液滴定,
硫代硫酸钠标准溶液滴定,近终点时,加 3mL淀粉指示液 ,继续滴定至终点,消耗体积 。
。
Ⅱ.空白实验:将上述样品溶液改为蒸馏水 注入碘量瓶中,重复后续步骤,滴定至终点时消耗体积
注入碘量瓶中,重复后续步骤,滴定至终点时消耗体积 。
。
①需要加入淀粉指示液时,锥形瓶中溶液的现象是_________ 。
②产品的质量分数为_________ 。
 是重要的工业原料.某小组按如图流程开展制备实验(部分装置及夹持仪器已省略)。主要反应:
是重要的工业原料.某小组按如图流程开展制备实验(部分装置及夹持仪器已省略)。主要反应:步骤Ⅱ:
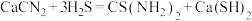
步骤Ⅲ:
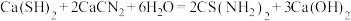
已知:硫代尿素
 可溶于水、乙醇,微溶于乙醚
可溶于水、乙醇,微溶于乙醚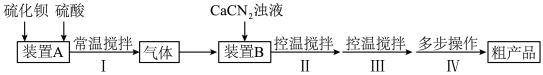
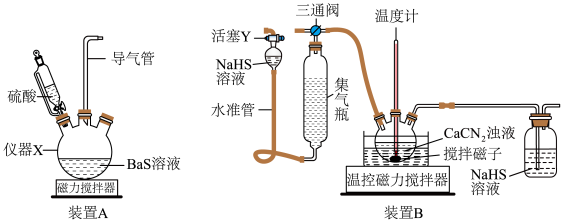
(2)下列说法不正确的是_________。
A.配制5%的 溶液必须用到的玻璃仪器有烧杯、玻璃棒、容量瓶等 溶液必须用到的玻璃仪器有烧杯、玻璃棒、容量瓶等 |
| B.装置A使用恒压分液漏斗添加硫酸溶液时,可以打开漏斗上部的玻璃塞 |
C.在反应前若向装置B中通入一段时间 ,能提高产品的产率 ,能提高产品的产率 |
| D.步骤Ⅱ反应完全的现象是溶液变澄清,集气瓶液面不再改变 |
(3)步骤Ⅰ、Ⅱ、Ⅲ的部分操作如下,其正确的顺序是:
(_________)→(_________)→a→(_________)→e→f→(_________)
a.调节三通阀如图 ,收集气体一段时间
,收集气体一段时间
c.调节装置B温控磁力搅拌器,并控制温度为

d.调节装置B温控磁力搅拌器,并迅速控温在

e.调节三通阀如图
g.检测气体纯净后连接三通阀
(4)步骤Ⅳ的
上述步骤中的最适宜洗涤剂是
A.冷水 B.热水 C.乙醚 D.滤液
(5)产品含量的测定:
滴定反应:
 ;
;
主要步骤:
Ⅰ.称取
 产品用蒸馏水溶解并定容至
产品用蒸馏水溶解并定容至 。移取该溶液
。移取该溶液 注入碘量瓶中,加
注入碘量瓶中,加 碘标准液,
碘标准液, 氢氧化钠溶液,于暗处放置
氢氧化钠溶液,于暗处放置 。加适量水及盐酸摇匀,用
。加适量水及盐酸摇匀,用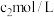 硫代硫酸钠标准溶液滴定,
硫代硫酸钠标准溶液滴定, 。
。Ⅱ.空白实验:将上述样品溶液改为蒸馏水
 注入碘量瓶中,重复后续步骤,滴定至终点时消耗体积
注入碘量瓶中,重复后续步骤,滴定至终点时消耗体积 。
。①需要加入淀粉指示液时,锥形瓶中溶液的现象是
②产品的质量分数为
您最近一年使用:0次
2024-04-01更新
|
395次组卷
|
4卷引用:压轴题12 化学实验综合题(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
(已下线)压轴题12 化学实验综合题(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)2024届浙江省温州市高三下学期第二次适应性考试(二模)化学试题浙江省温州市普通高中2024届高三下学期第二次适应性考试(二模)化学试题(已下线)化学(浙江卷02)-2024年高考押题预测卷
名校
10 . 某学习小组欲从含有 、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵
、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵 晶体,设计方案如下,下列说法
晶体,设计方案如下,下列说法不正确 的是
 、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵
、乙醇和氨水的实验室废液中分离乙醇并制备硫酸铜铵 晶体,设计方案如下,下列说法
晶体,设计方案如下,下列说法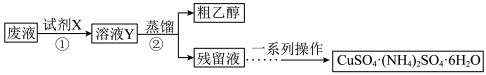
A.试剂X是硫酸,其中发生的反应之一: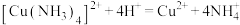 |
| B.步骤②蒸馏实验可用水浴加热 |
| C.若得到的粗乙醇中乙醇的含量明显偏低,可能是蒸馏时加热温度偏低 |
D.将残留液加热浓缩、冷却结晶可得到硫酸铜铵 晶体 晶体 |
您最近一年使用:0次
2024-04-01更新
|
449次组卷
|
6卷引用:压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
(已下线)压轴题03 物质的制备检验分离与提纯(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)(已下线)选择题6-102024届浙江省温州市高三下学期第二次适应性考试(二模)化学试题浙江省温州市普通高中2024届高三下学期第二次适应性考试(二模)化学试题(已下线)化学(浙江卷01)-2024年高考押题预测卷湖北省沙市中学2024届高三下学期模拟预测化学试题



