解题方法
1 . 下列有关实验操作的说法正确的是
| A.实验时手指不小心沾上苯酚,立即用浓NaOH溶液清洗 |
| B.用润湿的红色石蕊试纸置于试管口,试纸变蓝,证明有氨气产生 |
| C.将氯化铝溶液加热蒸发,最后可得到氯化铝晶体 |
| D.酸碱中和滴定时,锥形瓶需用待测液润洗后,再加入待测液 |
您最近一年使用:0次
名校
解题方法
2 . “化学多米诺实验”是只需控制第一个反应,就能使若干化学实验依次发生,如图所示。已知:①Cu2++4NH3•H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2的催化剂);②已知装置A、C中所用硫酸的浓度相同,装置B、D中所用金属锌的质量完全相同

下列说法错误的是( )

下列说法错误的是( )
| A.该实验成功的关键条件是整套装置的气密性良好 |
| B.因为形成原电池,所以装置D中生成氢气的反应速率一定大于B |
| C.导管a的作用是平衡A和B内气压 |
| D.装置H中出现浅黄色浑浊,可证明非金属性:O>S |
您最近一年使用:0次
2020-06-16更新
|
703次组卷
|
4卷引用:山西省太原市2020届高三模拟试题(二)理科综合化学试题
山西省太原市2020届高三模拟试题(二)理科综合化学试题(已下线)第26讲 化学实验基本操作及实验安全-2021年高考化学一轮复习名师精讲练安徽省淮北市第一中学 2021-2022学年高二上学期第一次月考化学试题湖南省临澧县第一中学2021-2022学年高一下学期第三次阶段性考试化学试题
解题方法
3 . 某同学欲利用浓盐酸、MnO2、Fe等试剂制取无水氯化铁、收集一定量的氯气并验证其某些性质,实验装置如图所示(制气装置省略)。下列说法错误的是
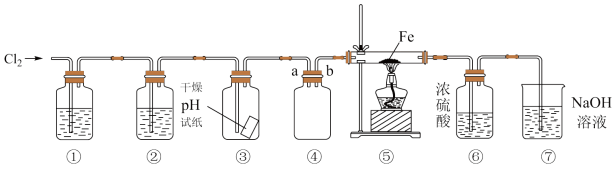

| A.④中a导管应向下延伸至接近瓶底 |
| B.若撤去⑥,则⑤中可能有Fe2O3生成 |
| C.当⑤中充满黄绿色气体时再点燃⑤处酒精灯 |
| D.③中试纸若是湿润的,则根据产生的现象可证明氯气有酸性,漂白性 |
您最近一年使用:0次
2020-05-12更新
|
533次组卷
|
4卷引用:天一大联考2019-2020学年高中毕业班阶段性测试(五)化学试卷
天一大联考2019-2020学年高中毕业班阶段性测试(五)化学试卷河南省濮阳市2020届高三毕业班第一次模拟考试理综化学试题(已下线)第12讲 富集在海水中的元素——卤素(精讲)-2022年一轮复习讲练测(已下线)第12讲 富集在海水中的元素——卤素(讲)-2023年高考化学一轮复习讲练测(全国通用)
名校
4 . 富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
(1)上述流程中能加快反应速率的措施有_____ 、_____ 等。
(2)酸浸时发生反应
2MgO·SiO2 +2H2SO4=2MgSO4+SiO2+2H2O,
2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4______ H3BO3(填“>”或“<”)。
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:___________ 、____________ 。
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH- =B(OH)4-。下列关于硼酸的说法正确的是_____ 。
a.硼酸的电离方程式可表示为:H3BO3 + H2O B(OH)4-+H+
B(OH)4-+H+
b.硼酸是一元弱酸
c.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验浸出液中的杂质离子
取少量浸出液,______ (填操作和现象),证明溶液中含有Fe2+。
(4)除去浸出液中的杂质离子
用MgO调节溶液的pH至____ 以上,使杂质离子转化为______ (填化学式)沉淀,过滤。
(5)获取晶体
ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
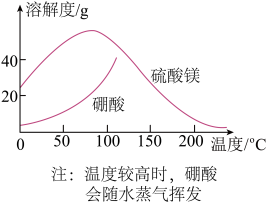
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜(高压环境可保证在高温条件下水为液态)中,__________ (将方法补充完整)。

已知:生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol/L)
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀时 | 1.9 | 3.4 | 7.0 | 9.1 |
| 完全沉淀时 | 3.2 | 4.7 | 9.0 | 11.1 |
(2)酸浸时发生反应
2MgO·SiO2 +2H2SO4=2MgSO4+SiO2+2H2O,
2MgO·B2O3+2H2SO4+H2O=2H3BO3+2MgSO4。
①上述反应体现出酸性强弱:H2SO4
②酸浸时,富硼渣中所含Al2O3和FeO也同时溶解,写出相关反应的离子方程式:
③已知硼酸与过量NaOH溶液发生的中和反应为:H3BO3+OH- =B(OH)4-。下列关于硼酸的说法正确的是
a.硼酸的电离方程式可表示为:H3BO3 + H2O
 B(OH)4-+H+
B(OH)4-+H+b.硼酸是一元弱酸
c.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生
(3)检验浸出液中的杂质离子
取少量浸出液,
(4)除去浸出液中的杂质离子
用MgO调节溶液的pH至
(5)获取晶体
ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.控制温度使两种晶体分别从溶液中结晶。结合下图溶解度曲线,简述ⅱ的方法:将浓缩液加入到高压釜(高压环境可保证在高温条件下水为液态)中,

您最近一年使用:0次
5 . 草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。某学生拟用下图装置做草酸晶体的分解实验并验证部分产物,下列说法错误的是
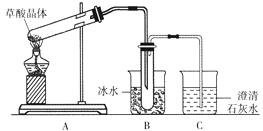
| A.装置A中的大试管口应略向下倾斜,是因为加热草酸晶体时会产生水 |
| B.装置B的主要作用是冷凝(水蒸气、草酸)等,防止草酸进入装置C中,干扰CO2的检验 |
| C.装置C中可观察到的现象是有气泡冒出,澄清石灰水变浑浊 |
| D.本实验能证明草酸晶体的分解产物有二氧化碳 |
您最近一年使用:0次
2017-12-12更新
|
366次组卷
|
8卷引用:河南省2018届高三高中毕业班阶段性测试(二)化学试题
名校
6 . 下列有关实验操作说法正确的是
| A.用容量瓶配制溶液时,若加水超过刻度线,立即用滴管吸出多余液体 |
| B.实验室提取碘水中的碘可以采取加酒精进行萃取的方法 |
| C.需要用浓氢氧化钠溶液和湿润的红色石蕊试纸证明溶液中含有NH4+ |
| D.做焰色反应时需要用稀硫酸或稀盐酸洗涤铂丝 |
您最近一年使用:0次
7 . 下列说法不正确 的是
| A.用pH试纸检验某干燥气体的酸碱性时,一定要先用蒸馏水湿润 |
| B.烧瓶、烧杯、锥形瓶在酒精灯上加热时,都需要要垫石棉网,以防仪器炸裂 |
| C.焰色反应时,透过蓝色钴玻璃,观察到火焰颜色为紫色,证明被检物是钾盐 |
| D.35Cl与37Cl互为同位素 |
您最近一年使用:0次
8 . 实验室对茶叶中铁元素的检验,可经以下四个步骤完成:①将茶叶灼烧灰化;②茶叶灰用浓硝酸浸取并加蒸馏水稀释;③过滤得到滤液;④用KSCN溶液进行检验。下列说法中正确的是
| A.步骤①所用仪器包括蒸发皿、酒精灯、玻璃棒等 |
| B.步骤②所用的浓硝酸应保存在带橡皮塞的棕色试剂瓶中 |
| C.步骤③可以不做,改为将悬浊液静置一段时间 |
| D.步骤④观察到溶液变红色,证明茶叶中含有Fe3+ |
您最近一年使用:0次
9 . 现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。
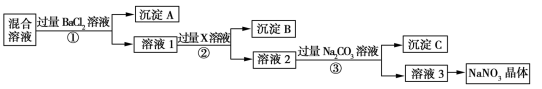
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_____ 沉淀B_____ 。
(2)上述实验流程中①②③步均要进行的实验操作是_____ (填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:_____ 、_____ 。
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有_____ 杂质。为了解决这个问题,可以向溶液3中加入适量的_____ 。
(5)在①步操作中如何证明加的BaCl2溶液已过量?_____ 。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有
(5)在①步操作中如何证明加的BaCl2溶液已过量?
您最近一年使用:0次
10 . 工业原料粗氯铂酸铵[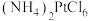 ,黄色,难溶于水,易溶于盐酸]中含有大量
,黄色,难溶于水,易溶于盐酸]中含有大量 、
、 ,某同学设计实验制备海绵铂,步骤如下:
,某同学设计实验制备海绵铂,步骤如下:
步骤1:取适量样品于小烧杯中,加入蒸馏水洗涤、过滤,收集滤渣;
步骤2:向“步骤1”的滤渣中加入稀盐酸,固体溶解后加入水合肼 ,搅拌,充分反应生成易溶于水的氯亚铂酸铵
,搅拌,充分反应生成易溶于水的氯亚铂酸铵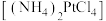 ;
;
步骤3:向“步骤2”所得溶液中通入足量 ,过滤洗涤得到
,过滤洗涤得到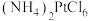 ;
;
步骤4:充分煅烧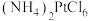 获得海绵铂。
获得海绵铂。
回答下列问题:
(1)“步骤1”洗涤时所用到的玻璃仪器有烧杯、漏斗、_______ ,该步骤的目的是_______ ,证明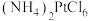 已洗涤干净的具体操作为
已洗涤干净的具体操作为_______ 。
(2)“步骤2”在溶解时的固液比、溶液的酸度(盐酸浓度)、反应时间等对海绵铂的产率均有较大影响。在不同酸度下达到较高产率所需时间,以及不同固液比在最佳酸度下反应时间与产率关系如图所示。
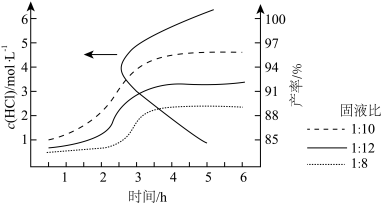
①由图1可得最佳反应条件是反应时间2.5~3h、_______ (填字母)。
A.酸度 、固液比
、固液比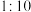 B.酸度
B.酸度 、固液比
、固液比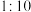
C.酸度 、固液比
、固液比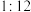 D.酸度
D.酸度 、固液比
、固液比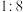
②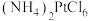 转化为
转化为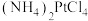 反应的化学方程式为
反应的化学方程式为_______ (还有 、
、 、
、 、
、 生成,不考虑水合肼自身分解)。
生成,不考虑水合肼自身分解)。
(3)步骤3所用装置(部分夹持仪器已省略)如图所示。

①装置a的烧瓶中盛放的固体为_______ (填化学式)。
②装置b中生成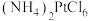 的化学方程式为
的化学方程式为_______ 。
③选择下列装置吸收尾气,宜选择_______ (填字母)。
A.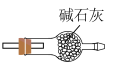 B.
B.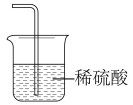 C.
C.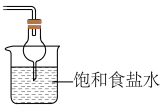 D.
D.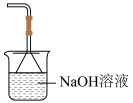
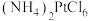 ,黄色,难溶于水,易溶于盐酸]中含有大量
,黄色,难溶于水,易溶于盐酸]中含有大量 、
、 ,某同学设计实验制备海绵铂,步骤如下:
,某同学设计实验制备海绵铂,步骤如下:步骤1:取适量样品于小烧杯中,加入蒸馏水洗涤、过滤,收集滤渣;
步骤2:向“步骤1”的滤渣中加入稀盐酸,固体溶解后加入水合肼
 ,搅拌,充分反应生成易溶于水的氯亚铂酸铵
,搅拌,充分反应生成易溶于水的氯亚铂酸铵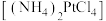 ;
;步骤3:向“步骤2”所得溶液中通入足量
 ,过滤洗涤得到
,过滤洗涤得到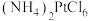 ;
;步骤4:充分煅烧
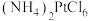 获得海绵铂。
获得海绵铂。回答下列问题:
(1)“步骤1”洗涤时所用到的玻璃仪器有烧杯、漏斗、
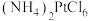 已洗涤干净的具体操作为
已洗涤干净的具体操作为(2)“步骤2”在溶解时的固液比、溶液的酸度(盐酸浓度)、反应时间等对海绵铂的产率均有较大影响。在不同酸度下达到较高产率所需时间,以及不同固液比在最佳酸度下反应时间与产率关系如图所示。

①由图1可得最佳反应条件是反应时间2.5~3h、
A.酸度
 、固液比
、固液比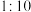 B.酸度
B.酸度 、固液比
、固液比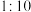
C.酸度
 、固液比
、固液比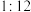 D.酸度
D.酸度 、固液比
、固液比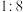
②
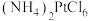 转化为
转化为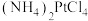 反应的化学方程式为
反应的化学方程式为 、
、 、
、 、
、 生成,不考虑水合肼自身分解)。
生成,不考虑水合肼自身分解)。(3)步骤3所用装置(部分夹持仪器已省略)如图所示。

①装置a的烧瓶中盛放的固体为
②装置b中生成
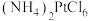 的化学方程式为
的化学方程式为③选择下列装置吸收尾气,宜选择
A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次



