解答题-实验探究题
|
适中(0.65)
|
解题方法
1 . 实验室欲用NaOH固体配制 的NaOH溶液,回答下列问题:
的NaOH溶液,回答下列问题:
(1)需称量氢氧化钠固体______  。
。
(2)在配制的过程中一定不需要使用到的仪器是____  填字母
填字母 ,还缺少的仪器有
,还缺少的仪器有______ 。
A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管
(3)从配制好的NaOH溶液中取出 ,OH-的物质的量浓度为
,OH-的物质的量浓度为______  ;将这
;将这 的NaOH溶液稀释至
的NaOH溶液稀释至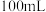 ,稀释后的溶液中
,稀释后的溶液中 的浓度为
的浓度为 _____  。
。
(4)下列的实验操作可能导致配制的溶液浓度偏低的是______  填字母
填字母 。
。
A.容量瓶内原来存有少量的水未进行干燥
B.称量固体时,所用砝码已生锈
C.NaOH固体溶解后,未冷却至室温就开始进行转移
D.定容时仰视视刻度线
E.定容时液面超过刻度线,用胶头滴管吸出
(5)金属铝可溶解在NaOH溶液中,写出反应的化学方程式_________________ 。
 的NaOH溶液,回答下列问题:
的NaOH溶液,回答下列问题:(1)需称量氢氧化钠固体
 。
。(2)在配制的过程中一定不需要使用到的仪器是
 填字母
填字母 ,还缺少的仪器有
,还缺少的仪器有A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管
(3)从配制好的NaOH溶液中取出
 ,OH-的物质的量浓度为
,OH-的物质的量浓度为 ;将这
;将这 的NaOH溶液稀释至
的NaOH溶液稀释至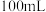 ,稀释后的溶液中
,稀释后的溶液中 的浓度为
的浓度为  。
。(4)下列的实验操作可能导致配制的溶液浓度偏低的是
 填字母
填字母 。
。A.容量瓶内原来存有少量的水未进行干燥
B.称量固体时,所用砝码已生锈
C.NaOH固体溶解后,未冷却至室温就开始进行转移
D.定容时仰视视刻度线
E.定容时液面超过刻度线,用胶头滴管吸出
(5)金属铝可溶解在NaOH溶液中,写出反应的化学方程式
您最近一年使用:0次
2 . 化学与人类生产、生活密切相关,按要求回答下列问题。
(1)生活中为了延长鲜花的寿命,通常会在花瓶中加入鲜花保鲜剂。下表是500mL某鲜花保鲜剂中含有的成分及含量:
①上述鲜花保鲜剂成分中,属于电解质的是_______ (填字母)。
②“鲜花保鲜剂”中蔗糖的物质的量浓度为_______  。
。
(2)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是_______ (填化学式)。
(3)钠的化合物中,可用作潜水艇中供氧剂的是_______ ,其与 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(4)某校兴趣小组同学用浓硫酸配制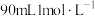 的稀硫酸,配制结束后,对所配制的稀硫酸进行测定,发现其浓度大于
的稀硫酸,配制结束后,对所配制的稀硫酸进行测定,发现其浓度大于 ,下列各项操作可能引起该误差的是_______(填字母)。
,下列各项操作可能引起该误差的是_______(填字母)。
(1)生活中为了延长鲜花的寿命,通常会在花瓶中加入鲜花保鲜剂。下表是500mL某鲜花保鲜剂中含有的成分及含量:
| 成分 | 质量(g) | 摩尔质量(g/mol) |
a.蔗糖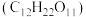 | 68.4 | 342 |
b.硫酸钾 | 0.5 | 174 |
c.高锰酸钾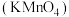 | 0.5 | 158 |
d.硝酸银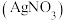 | 0.04 | 170 |
②“鲜花保鲜剂”中蔗糖的物质的量浓度为
 。
。(2)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是
(3)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(4)某校兴趣小组同学用浓硫酸配制
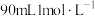 的稀硫酸,配制结束后,对所配制的稀硫酸进行测定,发现其浓度大于
的稀硫酸,配制结束后,对所配制的稀硫酸进行测定,发现其浓度大于 ,下列各项操作可能引起该误差的是_______(填字母)。
,下列各项操作可能引起该误差的是_______(填字母)。| A.用量筒量取浓硫酸时仰视读数 |
| B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水 |
| C.将稀释后的稀硫酸立即转入容量瓶,紧接着就进行后面的实验操作 |
| D.转移溶液时,不慎将少量溶液洒到容量瓶外面 |
您最近一年使用:0次
名校
3 . 某学习小组为认识铁及其化合物的性质和分散系的性质做了如下一系列综合实验。运用所学知识,回答下列问题:
(1)可利用___________ 来区分 胶体和
胶体和 溶液。
溶液。
(2)向盛有 溶液的试管中滴加
溶液的试管中滴加 溶液,请描述发生的现象
溶液,请描述发生的现象___________ 。
(3)铁粉与水蒸气在高温条件下反应的化学方程式是___________ 。
(4)电子工业中,人们常用 溶液腐蚀覆铜板来制作印刷电路板。现欲配制
溶液腐蚀覆铜板来制作印刷电路板。现欲配制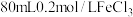 溶液,回答下列问题:
溶液,回答下列问题:
①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需___________ 。
②使用托盘天平称量 的质量为
的质量为___________ g。
③定容时,若仰视容量瓶刻度线会使配制的 溶液浓度
溶液浓度________ (填“偏大”“偏小”或“不变”)。
(5)实验室模拟用 溶液腐蚀铜板并从废液中回收
溶液腐蚀铜板并从废液中回收 和
和 溶液流程如图所示:
溶液流程如图所示:
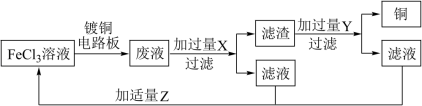
①请写出 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式___________ 。
②试剂 在反应中体现
在反应中体现___________ (填“氧化性”或“还原性”)。
③Z可选用的试剂有___________ (填序号)。
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
(1)可利用
 胶体和
胶体和 溶液。
溶液。(2)向盛有
 溶液的试管中滴加
溶液的试管中滴加 溶液,请描述发生的现象
溶液,请描述发生的现象(3)铁粉与水蒸气在高温条件下反应的化学方程式是
(4)电子工业中,人们常用
 溶液腐蚀覆铜板来制作印刷电路板。现欲配制
溶液腐蚀覆铜板来制作印刷电路板。现欲配制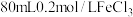 溶液,回答下列问题:
溶液,回答下列问题:①配制该溶液时所需玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外,还需
②使用托盘天平称量
 的质量为
的质量为③定容时,若仰视容量瓶刻度线会使配制的
 溶液浓度
溶液浓度(5)实验室模拟用
 溶液腐蚀铜板并从废液中回收
溶液腐蚀铜板并从废液中回收 和
和 溶液流程如图所示:
溶液流程如图所示:
①请写出
 溶液与铜反应的离子方程式
溶液与铜反应的离子方程式②试剂
 在反应中体现
在反应中体现③Z可选用的试剂有
A.硝酸 B.酸性高锰酸钾溶液 C.过氧化氢 D.氯气
您最近一年使用:0次
2023-08-03更新
|
364次组卷
|
5卷引用:湖南省株洲市南方中学2022-2023学年高一上学期期末考试化学试题
湖南省株洲市南方中学2022-2023学年高一上学期期末考试化学试题湖南省娄底市新化县2023-2024学年高一上学期期末考试化学试题(已下线)巩固测试卷02-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)甘肃省天水市第一中学2023-2024学年高一下学期开学化学试题山东省滨州市惠民县第二中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
4 . 实验室用NaOH固体配制100mL 0.50mol/L的NaOH溶液,请回答:
(1)需称取NaOH固体的质量为___________ g。
(2)容量瓶使用之前需要进行检漏,该操作为___________ 。
(3)配制的正确流程为(填序号)①⑥___________ 。
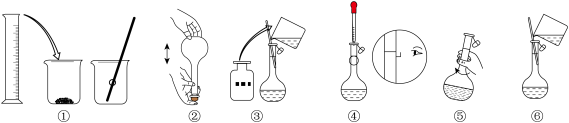
(4)下列说法不正确 的是___________。
(1)需称取NaOH固体的质量为
(2)容量瓶使用之前需要进行检漏,该操作为
(3)配制的正确流程为(填序号)①⑥

(4)下列说法
| A.NaOH固体可放在干燥的小烧杯中称量 |
| B.转移操作时不慎洒出几滴洗涤液,将导致最终浓度偏低 |
| C.容量瓶用后洗净、晾干,磨口玻璃瓶塞与瓶口处应垫一张纸条 |
D.若NaOH固体中混有少量的 ,将导致溶液中的 ,将导致溶液中的 偏低 偏低 |
您最近一年使用:0次
2023-07-29更新
|
173次组卷
|
2卷引用:浙江省台州市2022-2023学年高一上学期期末质量评估化学试题
解答题-实验探究题
|
适中(0.65)
|
解题方法
5 . Ⅰ.实验室欲使用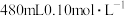 的
的 溶液,据此回答下列问题:
溶液,据此回答下列问题:
(1)需用托盘天平称量 固体的质量是
固体的质量是_________ g。
(2)配制过程中需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管及_________ 。
(3)如图是某同学配置 溶液的过程:
溶液的过程:
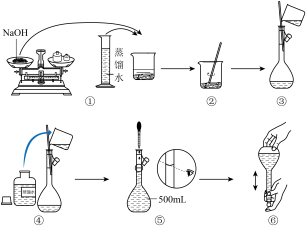
该同学的错误步骤有_________。
(4)下列实验操作可能导致配制的溶液浓度偏高的是_________。
Ⅱ.过氧化钙是一种温和的氧化剂,常温下为白色的固体,易溶于酸,难溶于水、乙醇等溶剂。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。
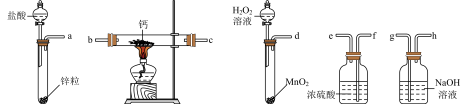
(5)盛装 溶液的仪器名称为
溶液的仪器名称为_________ 。
(6)实验中需要使用两次浓硫酸,第二次使用的浓硫酸的作用为_________ 。
(7)按照dfebef的顺序连接实验装置进行实验,步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞,通入一段时间气体,加热药品;③反应结束后,________________ (填操作);④拆除装置,取出产物。
 的
的 溶液,据此回答下列问题:
溶液,据此回答下列问题:(1)需用托盘天平称量
 固体的质量是
固体的质量是(2)配制过程中需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管及
(3)如图是某同学配置
 溶液的过程:
溶液的过程:
该同学的错误步骤有_________。
| A.1处 | B.2处 | C.3处 | D.4处 |
| A.容量瓶内原来存有少量的水 |
| B.定容时液面超过刻度线,用胶头滴管吸出 |
C.称量所需 固体的质量时,物品与砝码的位置放反了( 固体的质量时,物品与砝码的位置放反了( 以下用游码) 以下用游码) |
| D.定容时俯视刻度线 |
Ⅱ.过氧化钙是一种温和的氧化剂,常温下为白色的固体,易溶于酸,难溶于水、乙醇等溶剂。某实验小组拟选用如下装置(部分固定装置略)制备过氧化钙。

(5)盛装
 溶液的仪器名称为
溶液的仪器名称为(6)实验中需要使用两次浓硫酸,第二次使用的浓硫酸的作用为
(7)按照dfebef的顺序连接实验装置进行实验,步骤如下:①检验装置的气密性后,装入药品;②打开分液漏斗活塞,通入一段时间气体,加热药品;③反应结束后,
您最近一年使用:0次
名校
6 . 某化学兴趣小组为研究Na2CO3和NaHCO3的性质,完成了如下实验。
【实验一】溶解性比较。
(1)室温下,Na2CO3的溶解度大于NaHCO3的实验证据是___________ 。
(2)根据两试管中的温度变化情况,可得出的结论是___________ 。
【实验二】配制0.05mol·L-1Na2CO3溶液和0.05mol·L-1NaHCO3溶液。
(3)若要配制500mL上述Na2CO3溶液,需用托盘天平称量Na2CO3固体___________ g。
(4)配制上述Na2CO3溶液时需要用到的玻璃仪器有烧杯、玻璃棒和___________ 。
(5)下列情况中,会使所配溶液浓度偏高的是___________ (填字母)。
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
【实验三】测量下述实验过程的pH变化,实验操作及实验现象如下表所示。
【资料查阅】pH越小,OH-的物质的量浓度越小,溶液碱性越弱。
(6)当烧杯②中加入2mLNa2CO3溶液或烧杯③中加入2mLNaHCO3溶液时,两烧杯中产生白色沉淀的质量相等,其理由是___________ ,烧杯③中反应的离子方程式为___________ 。
【实验一】溶解性比较。
| 实验操作 | 实验现象 | |
| Na2CO3 | NaHCO3 | |
| 在两支试管中加入1gNa2CO3或1gNaHCO3,再加入5mL水,振荡;将温度计分别插入其中 | 温度由17.6℃变为23.2℃;放置至室温时,试管内无固体 | 温度由17.6℃变为17.2℃;放置至室温时,试管内有少量固体残留 |
(2)根据两试管中的温度变化情况,可得出的结论是
【实验二】配制0.05mol·L-1Na2CO3溶液和0.05mol·L-1NaHCO3溶液。
(3)若要配制500mL上述Na2CO3溶液,需用托盘天平称量Na2CO3固体
(4)配制上述Na2CO3溶液时需要用到的玻璃仪器有烧杯、玻璃棒和
(5)下列情况中,会使所配溶液浓度偏高的是
a.转移时,没有洗涤烧杯和玻璃棒
b.定容时,眼睛俯视刻度线
c.摇匀后,发现液面低于刻度线,继续加水至液面与刻度线相切
【实验三】测量下述实验过程的pH变化,实验操作及实验现象如下表所示。
【资料查阅】pH越小,OH-的物质的量浓度越小,溶液碱性越弱。
| 实验操作 | 实验现象 |
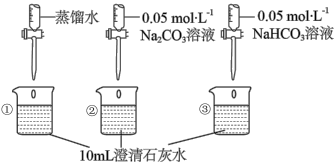 | I.②和③中均产生白色沉淀。 II.  |
您最近一年使用:0次
名校
7 . 实验室保存的浓盐酸标签如图所示,某同学用此浓盐酸配制500mL 0.2mol·L-1的稀盐酸。下列说法错误的是
| 盐酸 | |
| 分子式 | HCl |
| 相对分子量 | 36.5 |
| 密度 | 1.19g·cm3 |
| HCl的质量分数 | 36.5% |
| A.该浓盐酸的物质的量浓度为11.9 mol·L-1 |
| B.配制溶液所用的容量瓶不需要干燥 |
| C.若定容时仰视刻度线,所配溶液浓度偏小 |
| D.实验需用到的玻璃仪器有烧杯、容量瓶、胶头滴管三种 |
您最近一年使用:0次
2023-06-13更新
|
244次组卷
|
5卷引用:江苏省南通市海门中学2021-2022学年高一上学期期末考试化学试题
江苏省南通市海门中学2021-2022学年高一上学期期末考试化学试题(已下线)专题03 研究物质的实验方法 一定物质的量浓度溶液的配制-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)江苏省苏州市西安交通大学苏州附属中学2023-2024学年高一上学期12月月考化学试题浙江省浙南名校2023-2024学年高一下学期开学化学试题河北省唐山市第十二高级中学2023-2024学年高一上学期12月月考化学试题
解题方法
8 . 实验室配制0.20mol/LNaOH溶液,下列操作正确的是
| A.称量时,将NaOH固体放在托盘天平的右盘 |
| B.溶解NaOH后,将溶液立即转移到容量瓶中 |
| C.移液后,将洗涤烧杯和玻璃棒的溶液也转移到容量瓶中 |
| D.定容后,将容量瓶倒置摇匀,发现液面降低,继续加水至刻度线 |
您最近一年使用:0次
解答题-实验探究题
|
较易(0.85)
|
解题方法
9 . 实验室需用480mL1.0mol/LNaOH溶液,现用NaOH固体配制该溶液。请回答下列问题:
(1)配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、_______ 、______ 。
(2)用托盘天平准确称取_______ gNaOH固体。
(3)配制溶液时,其正确的操作顺序是_______ (用字母表示,每个操作只能用一次)。
A.将容量瓶盖紧,振荡、摇匀
B.用托盘天平准确称量所需的NaOH,放入烧杯中,再加入适量水,用玻璃棒慢慢搅拌,使其溶解
C.用适量水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将已冷却的溶液沿玻璃棒注入容量瓶中
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(4)定容时的操作正确,将容量瓶的玻璃塞盖紧,颠倒摇匀后取出10mL该NaOH溶液稀释至20mL,稀释后的NaOH溶液的物质的量浓度为_______ mol/L。
(5)配制该溶液时,玻璃棒的作用为_______ 。下列操作会造成所配溶液的浓度偏高的是_______ (填序号)。
①定容时俯视刻度线
②称量固体时所用的砝码生锈
③用称量纸称量氢氧化钠固体
④溶解时有溶液溅出烧杯
(1)配制时需要使用的玻璃仪器有烧杯、玻璃棒、量筒、
(2)用托盘天平准确称取
(3)配制溶液时,其正确的操作顺序是
A.将容量瓶盖紧,振荡、摇匀
B.用托盘天平准确称量所需的NaOH,放入烧杯中,再加入适量水,用玻璃棒慢慢搅拌,使其溶解
C.用适量水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将已冷却的溶液沿玻璃棒注入容量瓶中
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(4)定容时的操作正确,将容量瓶的玻璃塞盖紧,颠倒摇匀后取出10mL该NaOH溶液稀释至20mL,稀释后的NaOH溶液的物质的量浓度为
(5)配制该溶液时,玻璃棒的作用为
①定容时俯视刻度线
②称量固体时所用的砝码生锈
③用称量纸称量氢氧化钠固体
④溶解时有溶液溅出烧杯
您最近一年使用:0次
2023-06-07更新
|
181次组卷
|
2卷引用:安徽省蚌埠市2022-2023学年高一上学期期末学业水平监测化学试题
名校
10 . 回答下列问题
(1)实验室欲用Na2CO3·10H2O晶体配制100 mL 1 mol/L的Na2CO3溶液,需称取Na2CO3·10H2O晶体___________ g;完成本实验需用到的仪器有天平、药匙、玻璃棒、烧杯和___________ ;下列情况会使所配溶液浓度偏低的是___________ (填序号)。
①用天平称量质量时,被称量物与砝码的位置放颠倒了
②转移溶液前容量瓶内有少量蒸馏水
③定容时俯视刻度线
④定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(2)某混合溶液中,含有K+、Mg2+、Al3+、Cl-和SO 五种离子(不考虑溶液中少量H+和OH-),其中c(K+)=3 mol/L、c(Mg2+)=2 mol/L、c(Al3+)=2 mol/L、c(Cl-)=7 mol/L,则溶液中SO
五种离子(不考虑溶液中少量H+和OH-),其中c(K+)=3 mol/L、c(Mg2+)=2 mol/L、c(Al3+)=2 mol/L、c(Cl-)=7 mol/L,则溶液中SO 的物质的量浓度是
的物质的量浓度是___________ 。
(3)同温同压下,某容器充满O2重116 g,若充满CO2重122 g,现充满某气体重114 g,则该气体的相对分子质量为___________ 。
(4)相同状况下,若气体X2与氮气以体积比1∶4混合,该混合气体相对氢气的密度为14.4,则X2的相对分子质量为___________ 。
(5)若标准状况下气体X2的密度为1.25 g·L-1,X原子最外层有___________ 个电子。
(1)实验室欲用Na2CO3·10H2O晶体配制100 mL 1 mol/L的Na2CO3溶液,需称取Na2CO3·10H2O晶体
①用天平称量质量时,被称量物与砝码的位置放颠倒了
②转移溶液前容量瓶内有少量蒸馏水
③定容时俯视刻度线
④定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(2)某混合溶液中,含有K+、Mg2+、Al3+、Cl-和SO
 五种离子(不考虑溶液中少量H+和OH-),其中c(K+)=3 mol/L、c(Mg2+)=2 mol/L、c(Al3+)=2 mol/L、c(Cl-)=7 mol/L,则溶液中SO
五种离子(不考虑溶液中少量H+和OH-),其中c(K+)=3 mol/L、c(Mg2+)=2 mol/L、c(Al3+)=2 mol/L、c(Cl-)=7 mol/L,则溶液中SO 的物质的量浓度是
的物质的量浓度是(3)同温同压下,某容器充满O2重116 g,若充满CO2重122 g,现充满某气体重114 g,则该气体的相对分子质量为
(4)相同状况下,若气体X2与氮气以体积比1∶4混合,该混合气体相对氢气的密度为14.4,则X2的相对分子质量为
(5)若标准状况下气体X2的密度为1.25 g·L-1,X原子最外层有
您最近一年使用:0次
2023-05-04更新
|
391次组卷
|
2卷引用:陕西省西安市长安区第一中学2022-2023学年高一上学期期末考试化学试题



