名校
1 . 下列实验有关操作不正确 的是
| 被提纯物(杂质) | 除杂方法 | |
| A | 苯甲酸( ) ) | 加热溶解,冷却结晶,过滤、洗涤、干燥 |
| B |  | 加入生石灰,蒸馏 |
| C | 乙炔( ) ) | 酸性高锰酸钾溶液,洗气 |
| D | 乙酸乙酯(乙酸) | 加入饱和碳酸钠溶液,分液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 氮化硅可用作耐高温、耐腐蚀材料。由石英砂和原料气(含 和少量
和少量 )制备
)制备 (粗硅中含
(粗硅中含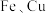 的单质及化合物,高温氮化时杂质未参加反应)的一种工艺流程如图所示。
的单质及化合物,高温氮化时杂质未参加反应)的一种工艺流程如图所示。
 和少量
和少量 )制备
)制备 (粗硅中含
(粗硅中含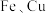 的单质及化合物,高温氮化时杂质未参加反应)的一种工艺流程如图所示。
的单质及化合物,高温氮化时杂质未参加反应)的一种工艺流程如图所示。
A.“还原”时焦炭主要被氧化为 | B.“高温氮化”时 作还原剂 作还原剂 |
| C. “操作X”可将原料气通过灼热的铜粉 | D. “酸洗”时,“稀酸Y”选用稀硫酸 |
您最近一年使用:0次
2024-05-18更新
|
251次组卷
|
4卷引用:重庆市主城区(九龙坡区)2024届高三下学期学业质量调研抽测(第三次)化学试题
重庆市主城区(九龙坡区)2024届高三下学期学业质量调研抽测(第三次)化学试题(已下线)暑假作业06 以简单工艺流程突破元素化合物知识和应用-【暑假分层作业】2024年高二化学暑假培优练(2025届一轮复习通用)第16讲 碳、硅及无机非金属材料考点专练陕西省安康市高新中学2023-2024学年高一下学期6月月考化学试题
名校
解题方法
3 .  纳米材料是一种很有发展前景的储能材料,用菱锰矿(主要成分为
纳米材料是一种很有发展前景的储能材料,用菱锰矿(主要成分为 ,含有少量CaO、MgO、FeO、
,含有少量CaO、MgO、FeO、 、
、 等)制备
等)制备 纳米材料的工艺流程如图所示。
纳米材料的工艺流程如图所示。 如表所示。
如表所示。
回答下列问题:
(1)“酸浸”中提高反应速率的可行措施有___________ (任答一条);酸浸渣的主要成分是___________ (填化学式)。
(2)加入 的目的是氧化
的目的是氧化___________ (填离子符号),写出该离子被氧化生成沉淀的离子方程式:___________ 。
(3)回收的沉淀可与浓硫酸反应生成能腐蚀玻璃的气体, 与浓硫酸在加热的条件下反应的化学方程式为
与浓硫酸在加热的条件下反应的化学方程式为___________ ;25℃时,沉淀后的滤液中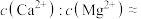
___________ (写最简整数比)。
(4)用去离子水多次洗涤 纳米材料,检验沉淀是否洗涤干净的操作为
纳米材料,检验沉淀是否洗涤干净的操作为___________ 。
(5)“高压釜水热反应”溶液pH应调节为中性,而不能过高的原因是___________ 。
 纳米材料是一种很有发展前景的储能材料,用菱锰矿(主要成分为
纳米材料是一种很有发展前景的储能材料,用菱锰矿(主要成分为 ,含有少量CaO、MgO、FeO、
,含有少量CaO、MgO、FeO、 、
、 等)制备
等)制备 纳米材料的工艺流程如图所示。
纳米材料的工艺流程如图所示。
 如表所示。
如表所示。| 物质 |  |  |  |  |
 | 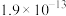 |  | 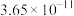 | 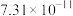 |
| 物质 |  |  |  | |
 | 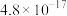 | 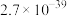 |  |
(1)“酸浸”中提高反应速率的可行措施有
(2)加入
 的目的是氧化
的目的是氧化(3)回收的沉淀可与浓硫酸反应生成能腐蚀玻璃的气体,
 与浓硫酸在加热的条件下反应的化学方程式为
与浓硫酸在加热的条件下反应的化学方程式为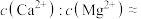
(4)用去离子水多次洗涤
 纳米材料,检验沉淀是否洗涤干净的操作为
纳米材料,检验沉淀是否洗涤干净的操作为(5)“高压釜水热反应”溶液pH应调节为中性,而不能过高的原因是
您最近一年使用:0次
2024-05-17更新
|
268次组卷
|
2卷引用:2024届重庆市渝西中学高三下学期模拟预测化学试题
名校
4 . 除去下列物质中的杂质所选用的试剂或操作方法均正确的是
| 序号 | 物质 | 杂质 | 应选用的试剂或操作方法 |
| ① |  |  | 在坩埚中灼烧至固体质量不再减少 |
| ② |  | HCl | 分别通过饱和食盐水和浓硫酸 |
| ③ | 辛烷 | 辛烯 | 加入溴水,并分液 |
| ④ | NaCl固体 |  固体 固体 | 加少量热水、搅拌、趁热过滤 |
| A.①②③④ | B.①③④ | C.②③④ | D.①②④ |
您最近一年使用:0次
2024-05-17更新
|
283次组卷
|
2卷引用:2024届重庆市渝西中学高三下学期模拟预测化学试题
5 . 鱼浮灵是一种化学增氧剂,主要成分为过氧碳酸钠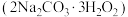 ,有
,有 和
和 的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用
的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用 与稳定剂的混合液(稳定剂不参与制备反应)和
与稳定剂的混合液(稳定剂不参与制备反应)和 化合制备过氧碳酸钠,制备装置如图。
化合制备过氧碳酸钠,制备装置如图。_______ ,仪器A中冷凝水的进口是_______ (填“a”或“b”)。
(2)烧瓶中发生主要反应的方程式为_______ 。
(3)下列物质可做该反应的稳定剂的是_______。
(4)实验时反应温度应控制在15~20℃,可采取的措施是_______ 。
(5)反应结束后,为了获得干燥的过氧碳酸钠固体,可在反应液中加入适量的_______ ,再进行静置、抽滤、洗涤、_______ 。
(6)取4g过氧碳酸钠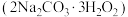 产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用
产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用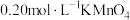 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液15.00mL。滴定的化学反应方程式
溶液15.00mL。滴定的化学反应方程式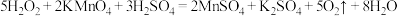 ,该过氧碳酸钠的产品纯度为
,该过氧碳酸钠的产品纯度为_______ 。
(7)为了探究过氧碳酸钠在溶液中的增氧机理,在相同时间测得体系的pH和溶解氧的含量如下表,结合以上数据分析“鱼浮灵”溶于水后在水产养殖中速效增氧的原理_______ 。
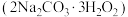 ,有
,有 和
和 的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用
的双重性质,50℃开始分解,在异丙醇中溶解度较低。实验室用 与稳定剂的混合液(稳定剂不参与制备反应)和
与稳定剂的混合液(稳定剂不参与制备反应)和 化合制备过氧碳酸钠,制备装置如图。
化合制备过氧碳酸钠,制备装置如图。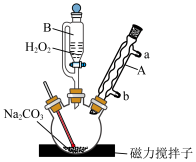
(2)烧瓶中发生主要反应的方程式为
(3)下列物质可做该反应的稳定剂的是_______。
A. | B. | C. | D. |
(4)实验时反应温度应控制在15~20℃,可采取的措施是
(5)反应结束后,为了获得干燥的过氧碳酸钠固体,可在反应液中加入适量的
(6)取4g过氧碳酸钠
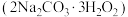 产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用
产品配成100mL溶液,取25.00mL溶液于锥形瓶,加入足量稀硫酸,用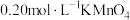 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液15.00mL。滴定的化学反应方程式
溶液15.00mL。滴定的化学反应方程式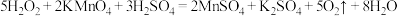 ,该过氧碳酸钠的产品纯度为
,该过氧碳酸钠的产品纯度为(7)为了探究过氧碳酸钠在溶液中的增氧机理,在相同时间测得体系的pH和溶解氧的含量如下表,结合以上数据分析“鱼浮灵”溶于水后在水产养殖中速效增氧的原理
| 试剂 |  |  | 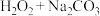 | 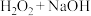 | 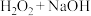 |
| pH | 6.0 | 15.97 | 8.14 | 8.15 | 9.26 |
| 溶解氧 | 6.44 | 6.48 | 9.11 | 9.12 | 10.97 |
您最近一年使用:0次
名校
6 .  可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分
可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分 ,杂质为
,杂质为 )和黄铁矿
)和黄铁矿 为原料制备
为原料制备 其流程如图。
其流程如图。
回答下列问题:
(1) 的价层电子排布图
的价层电子排布图_______ ,“酸浸”过程中,滤渣1的主要成分为S、_______ (填化学式)。
(2)“酸浸”过程中 、
、 的质量浓度、Mn的浸出率与时间的关系如图所示。
的质量浓度、Mn的浸出率与时间的关系如图所示。_______ 。
②80~100min时, 浓度上升的原因可能是
浓度上升的原因可能是_______ 。
(3)“沉铁”过程中依次加入的试剂X、Y为_______ (填字母)。
A.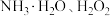 B.
B. C.
C.
(4)“滤液”萃取前调 ,若有机萃取剂用HR表示,则发生萃取的反应可表示为
,若有机萃取剂用HR表示,则发生萃取的反应可表示为 。若,
。若,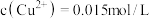 多次萃取后水相中
多次萃取后水相中 为
为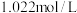 ,则铜的萃取率为
,则铜的萃取率为_______ (结果保留小数点后一位,溶液体积变化忽略不计)。
(5)利用 溶液,用空气氧化法制备
溶液,用空气氧化法制备 。在
。在 溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备
溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备 。写出上述反应的离子方程式:
。写出上述反应的离子方程式:_______ 。
(6)结合图像分析,若要获得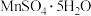 晶体的系列操作步骤为加热
晶体的系列操作步骤为加热_______ 得到_______ ℃饱和溶液,_______ ,过滤酒精洗涤,低温干燥。
 可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分
可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分 ,杂质为
,杂质为 )和黄铁矿
)和黄铁矿 为原料制备
为原料制备 其流程如图。
其流程如图。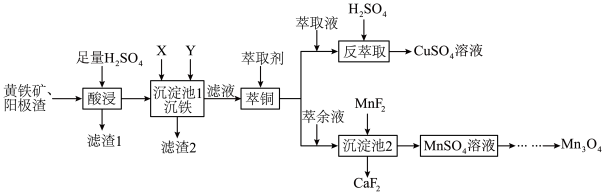
 |  |  |  | |
| 完全沉淀时的pH | 3.7 | 9.7 | 7.4 | 9.8 |
(1)
 的价层电子排布图
的价层电子排布图(2)“酸浸”过程中
 、
、 的质量浓度、Mn的浸出率与时间的关系如图所示。
的质量浓度、Mn的浸出率与时间的关系如图所示。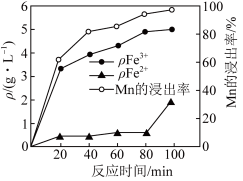
②80~100min时,
 浓度上升的原因可能是
浓度上升的原因可能是(3)“沉铁”过程中依次加入的试剂X、Y为
A.
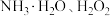 B.
B. C.
C.
(4)“滤液”萃取前调
 ,若有机萃取剂用HR表示,则发生萃取的反应可表示为
,若有机萃取剂用HR表示,则发生萃取的反应可表示为 。若,
。若,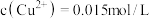 多次萃取后水相中
多次萃取后水相中 为
为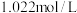 ,则铜的萃取率为
,则铜的萃取率为(5)利用
 溶液,用空气氧化法制备
溶液,用空气氧化法制备 。在
。在 溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备
溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备 。写出上述反应的离子方程式:
。写出上述反应的离子方程式:(6)结合图像分析,若要获得
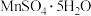 晶体的系列操作步骤为加热
晶体的系列操作步骤为加热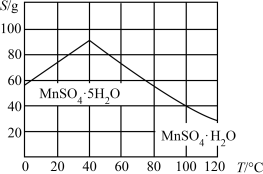
您最近一年使用:0次
名校
7 . 高纯 在光子晶体等领域应用广泛。一种利用工业
在光子晶体等领域应用广泛。一种利用工业 (含少量Ca、Fe、Mn等元素的氧化物)制备高纯
(含少量Ca、Fe、Mn等元素的氧化物)制备高纯 的工艺如下。
的工艺如下。
回答下列问题:
(1)F的原子结构示意图为___________ 。 的电子式为
的电子式为___________ 。
(2)反应釜1中,加入稀硝酸溶解后,调节pH至7.5,生成的沉淀主要是___________ 。再加入 ,除去的金属元素是
,除去的金属元素是___________ 。
(3)反应釜2中,为使 沉淀完全,
沉淀完全, 浓度应大于
浓度应大于___________ mol/L[已知:当溶液中某种离子的浓度低于 时,可认为该种离子已经全部被除去。可用
时,可认为该种离子已经全部被除去。可用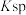 来衡量某种物质在水中所能溶解的最大量,例如
来衡量某种物质在水中所能溶解的最大量,例如 的
的 ]。
]。
(4)反应釜3中,反应的离子方程式为___________ 。
(5)离心后的溶液经浓缩结晶,所得固体的主要成分是___________ 。现称取一定量该固体配成溶液,取20.00mL,加入足量HCHO,反应为:
 的酸性与醋酸接近。以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的
的酸性与醋酸接近。以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的 浓度为
浓度为___________ mol/L。
 在光子晶体等领域应用广泛。一种利用工业
在光子晶体等领域应用广泛。一种利用工业 (含少量Ca、Fe、Mn等元素的氧化物)制备高纯
(含少量Ca、Fe、Mn等元素的氧化物)制备高纯 的工艺如下。
的工艺如下。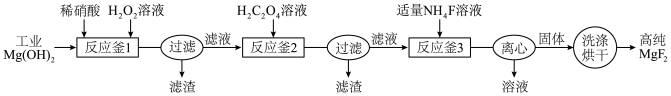
| 离子 |  |  |  |  |  |
| 完全沉淀的pH | 10.6 | 13.9 | 9.0 | 2.8 | 10.1 |
(1)F的原子结构示意图为
 的电子式为
的电子式为(2)反应釜1中,加入稀硝酸溶解后,调节pH至7.5,生成的沉淀主要是
 ,除去的金属元素是
,除去的金属元素是(3)反应釜2中,为使
 沉淀完全,
沉淀完全, 浓度应大于
浓度应大于 时,可认为该种离子已经全部被除去。可用
时,可认为该种离子已经全部被除去。可用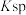 来衡量某种物质在水中所能溶解的最大量,例如
来衡量某种物质在水中所能溶解的最大量,例如 的
的 ]。
]。(4)反应釜3中,反应的离子方程式为
(5)离心后的溶液经浓缩结晶,所得固体的主要成分是

 的酸性与醋酸接近。以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的
的酸性与醋酸接近。以酚酞作指示剂,用0.2000mol/LNaOH标准溶液滴定,消耗24.00mL,则所配溶液的 浓度为
浓度为
您最近一年使用:0次
名校
解题方法
8 . 铈(Ce)的氧化物在半导体材料、高级颜料及汽车尾气的净化器方面有广泛应用。以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
(1) 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有_______ (填序号)。
a. b.
b. c.
c. d.
d.
(2) 中非金属元素的第一电离能从小到大依次为
中非金属元素的第一电离能从小到大依次为_______ 。
(3)“氧化焙烧”后, 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:_______ 。
(4)实验室进行操作①所需的玻璃仪器有_______ 。
(5)“系列操作”包含下图几个过程: 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应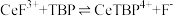 。“滤液A”中加入有机物
。“滤液A”中加入有机物 后的分离方法是
后的分离方法是_______ 。
(6)已知25℃时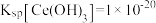 ,“调pH”时,要使
,“调pH”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于_______ 。
(7) 立方晶胞结构如图所示。
立方晶胞结构如图所示。_______ 。
 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图: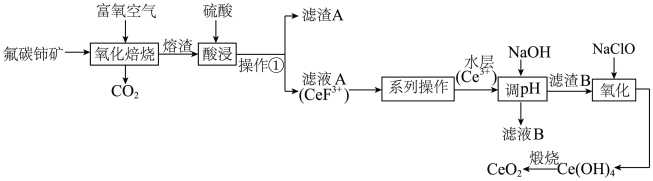
(1)
 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有a.
 b.
b. c.
c. d.
d.
(2)
 中非金属元素的第一电离能从小到大依次为
中非金属元素的第一电离能从小到大依次为(3)“氧化焙烧”后,
 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:(4)实验室进行操作①所需的玻璃仪器有
(5)“系列操作”包含下图几个过程:
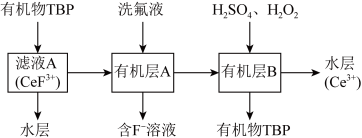
 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应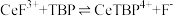 。“滤液A”中加入有机物
。“滤液A”中加入有机物 后的分离方法是
后的分离方法是(6)已知25℃时
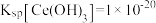 ,“调pH”时,要使
,“调pH”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于(7)
 立方晶胞结构如图所示。
立方晶胞结构如图所示。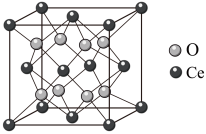
您最近一年使用:0次
名校
9 . 工业上可用红土镍矿(主要成分为NiO、FeO、 )制备
)制备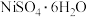 并回收副产物黄铵铁矾[
并回收副产物黄铵铁矾[ ]的工艺流程如下。
]的工艺流程如下。______ ℃,“初步沉铁”中,向酸浸后的溶液中通入NH3调节溶液的pH至1.5左右,溶液温度保持80℃左右,鼓入空气,一段时间后沉淀出黄铵铁矾。鼓入的“空气”的作用是______ 。 随时间t的变化关系如图2所示,反应开始10~20min内
随时间t的变化关系如图2所示,反应开始10~20min内 迅速减小,同时有大量气体产生,其原因是
迅速减小,同时有大量气体产生,其原因是______ 。______ 。
(4)滤液溶质的主要成分是 ,加
,加 过滤后得到
过滤后得到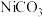 固体,再加适量稀硫酸溶解又生成
固体,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是______ 。
(5)得到的 溶液经
溶液经______ 过滤、洗涤、干燥等一系列操作可得到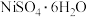 晶体。为了提高产率,“一系列操作”后得到的母液要循环使用,则应该回流到流程中的
晶体。为了提高产率,“一系列操作”后得到的母液要循环使用,则应该回流到流程中的______ 位置(选填“a”、“b”、“c”、“d”)。
 )制备
)制备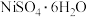 并回收副产物黄铵铁矾[
并回收副产物黄铵铁矾[ ]的工艺流程如下。
]的工艺流程如下。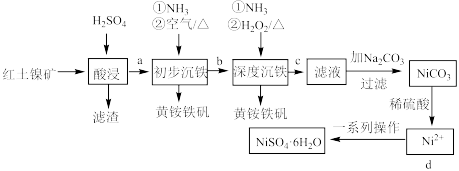
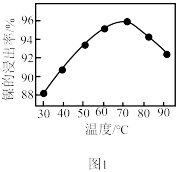
 随时间t的变化关系如图2所示,反应开始10~20min内
随时间t的变化关系如图2所示,反应开始10~20min内 迅速减小,同时有大量气体产生,其原因是
迅速减小,同时有大量气体产生,其原因是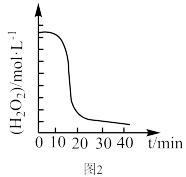
(4)滤液溶质的主要成分是
 ,加
,加 过滤后得到
过滤后得到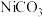 固体,再加适量稀硫酸溶解又生成
固体,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是(5)得到的
 溶液经
溶液经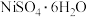 晶体。为了提高产率,“一系列操作”后得到的母液要循环使用,则应该回流到流程中的
晶体。为了提高产率,“一系列操作”后得到的母液要循环使用,则应该回流到流程中的
您最近一年使用:0次
名校
解题方法
10 . 下列混合物进行分离、提纯的方法正确的是
| A.分离水和溴苯的混合物的最佳方法是蒸馏 |
B.将混合气体通过酸性  溶液的洗气瓶除去混在乙烷中的乙烯 溶液的洗气瓶除去混在乙烷中的乙烯 |
| C.提取碘水中的碘,用无水酒精作萃取剂进行萃取后分液 |
D.用蒸馏的方法分离四氯化碳 (沸点为 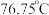 )和甲苯 (沸点为 )和甲苯 (沸点为 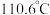 )的混合物 )的混合物 |
您最近一年使用:0次
2024-05-06更新
|
115次组卷
|
3卷引用:重庆市第十一中学校2023-2024学年高二下学期期中考试化学试题



