1 . 下列实验设计思路正确的是
A.用湿润的pH试纸检验 是否为酸性气体 是否为酸性气体 |
| B.直接加热饱和氯化铁溶液制氢氧化铁胶体 |
| C.除去氨气中混有的氢气,将混合气体通过灼热的氧化铜 |
| D.检验铜和浓硫酸在加热条件下是否生成铜离子,往混合溶液中加入水,观察溶液颜色是否变蓝 |
您最近一年使用:0次
名校
2 . 某工业废水中存在大盘的Na+、 、Cu2+、
、Cu2+、 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计的工艺流程如图所示:
,设计的工艺流程如图所示:

(1)加入NaOH溶液时反应的离子方程式:_______ 。
(2)试剂a为_______ ,试剂b为_______ 。
(3)流程图中操作X为_______ 。
(4)检验废水中的 已沉淀完全的方法为
已沉淀完全的方法为_______ 。
 、Cu2+、
、Cu2+、 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计的工艺流程如图所示:
,设计的工艺流程如图所示:
(1)加入NaOH溶液时反应的离子方程式:
(2)试剂a为
(3)流程图中操作X为
(4)检验废水中的
 已沉淀完全的方法为
已沉淀完全的方法为
您最近一年使用:0次
名校
解题方法
3 . 重钢集团含钛高炉渣(主要成分为 ,还含有少量
,还含有少量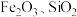 )可以用于生产
)可以用于生产 ,其工艺流程有如下两种:
,其工艺流程有如下两种:
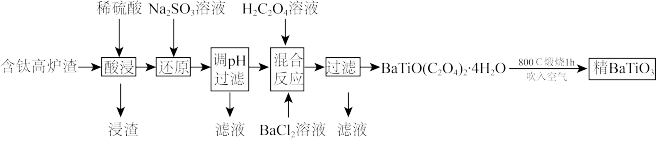
流程Ⅰ:
已知:a.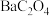 难溶于水,能溶于强酸;
难溶于水,能溶于强酸;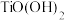 难溶于水,具有两性,溶于草酸生成
难溶于水,具有两性,溶于草酸生成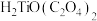 ;
;
b.相关离子[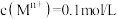 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如下表:
范围如下表:
(1)“浸渣”的成分主要是_______ 。
(2)“酸浸”后 以
以 形式存在,该反应的离子方程式为
形式存在,该反应的离子方程式为_______ 。
(3)“还原”的最终目的是_______ 。
(4)“混合反应”时,试剂添加顺序合理的是_______ (填序号)。
A.先加入过量 溶液,再加入适量
溶液,再加入适量 溶液
溶液
B.先加入过量 溶液,再加入适量
溶液,再加入适量 溶液
溶液
C.先按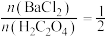 混合后,再加入反应体系中
混合后,再加入反应体系中
流程Ⅱ:
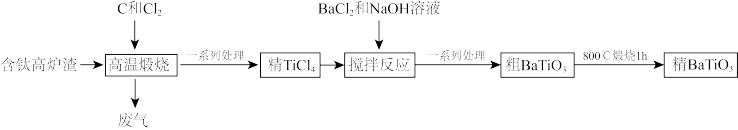
(5)实验测得,粗 的纯度为
的纯度为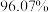 ,其中含
,其中含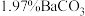 、
、 杂质,煅烧
杂质,煅烧 后,最终产品的产率和纯度(仅含微量
后,最终产品的产率和纯度(仅含微量 杂质)均明显提高。试回答下列问题:
杂质)均明显提高。试回答下列问题:
①用化学方程式解释“800℃煅烧”时产率提高的原因:_______ 。
②最终产品的纯度为_______ %(保留1位小数)。
(6)流程Ⅰ_______ (填“优于”或“劣于”)流程Ⅱ,理由是_______ 。
 ,还含有少量
,还含有少量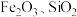 )可以用于生产
)可以用于生产 ,其工艺流程有如下两种:
,其工艺流程有如下两种:流程Ⅰ:

已知:a.
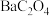 难溶于水,能溶于强酸;
难溶于水,能溶于强酸;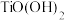 难溶于水,具有两性,溶于草酸生成
难溶于水,具有两性,溶于草酸生成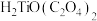 ;
;b.相关离子[
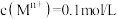 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如下表:
范围如下表:| 离子 |  |  |  |
开始沉淀的 | 0.5 | 6.3 | 1.5 |
完全沉淀的 | 2.5 | 8.3 | 2.8 |
(1)“浸渣”的成分主要是
(2)“酸浸”后
 以
以 形式存在,该反应的离子方程式为
形式存在,该反应的离子方程式为(3)“还原”的最终目的是
(4)“混合反应”时,试剂添加顺序合理的是
A.先加入过量
 溶液,再加入适量
溶液,再加入适量 溶液
溶液B.先加入过量
 溶液,再加入适量
溶液,再加入适量 溶液
溶液C.先按
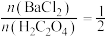 混合后,再加入反应体系中
混合后,再加入反应体系中流程Ⅱ:

(5)实验测得,粗
 的纯度为
的纯度为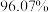 ,其中含
,其中含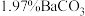 、
、 杂质,煅烧
杂质,煅烧 后,最终产品的产率和纯度(仅含微量
后,最终产品的产率和纯度(仅含微量 杂质)均明显提高。试回答下列问题:
杂质)均明显提高。试回答下列问题:①用化学方程式解释“800℃煅烧”时产率提高的原因:
②最终产品的纯度为
(6)流程Ⅰ
您最近一年使用:0次
名校
4 . 下列实验操作能达到对应目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将 通入漂白粉溶液中 通入漂白粉溶液中 | 证明 的酸性强于 的酸性强于 |
| B | 向混合溶液加入氢氧化钠,反应后静置、分液 | 除去溴苯中混有的 |
| C | 向 溶液中滴加酸性高锰酸钾溶液 溶液中滴加酸性高锰酸钾溶液 | 证明 的氧化性强于 的氧化性强于 |
| D | 将表面打磨过的铝片迅速投入正在沸腾的水中 | 验证 是否和沸水发生反应 是否和沸水发生反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . I.已知 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
(1)试管 的溶液中所含的上述离子有
的溶液中所含的上述离子有___________ 。
(2)若将试管 和试管
和试管 中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为___________ 、___________ 。(不考虑氢氧化银的存在)
(3)若向由试管 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为___________ 。
II.为除去粗盐中的 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
称取粗盐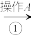
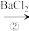
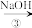
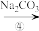
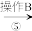 滤液
滤液
 精盐
精盐
(4)第①步中,操作 是
是___________ ,第⑤步中,操作
___________ ;
(5)第④步中,写出相应的离子方程式(设粗盐溶液中 的主要存在形式为CaCl2)
的主要存在形式为CaCl2)___________ ,___________ ;
(6)若先用盐酸调 再过滤,将对实验结果产生影响,其原因是
再过滤,将对实验结果产生影响,其原因是___________ 。
 和
和 两支试管所盛的溶液中共含有
两支试管所盛的溶液中共含有 、
、 、
、 、
、 、
、 、
、 六种离子,向试管
六种离子,向试管 的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
的溶液中滴入酚酞试液呈粉红色。请回答下列问题:(1)试管
 的溶液中所含的上述离子有
的溶液中所含的上述离子有(2)若将试管
 和试管
和试管 中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为(3)若向由试管
 溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量
溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量 溶液,则发生反应的离子方程式为
溶液,则发生反应的离子方程式为II.为除去粗盐中的
 、
、 、
、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):称取粗盐
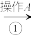
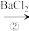
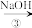
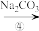
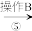 滤液
滤液
 精盐
精盐(4)第①步中,操作
 是
是
(5)第④步中,写出相应的离子方程式(设粗盐溶液中
 的主要存在形式为CaCl2)
的主要存在形式为CaCl2)(6)若先用盐酸调
 再过滤,将对实验结果产生影响,其原因是
再过滤,将对实验结果产生影响,其原因是
您最近一年使用:0次
2022-03-27更新
|
210次组卷
|
2卷引用:重庆市第七中学校2021-2022学年高一下学期3月月考化学试题
名校
解题方法
6 . 下列除杂方法正确的是
| A.除去N2中的少量O2:通过灼热的CuO |
| B.除去BaCl2溶液中的少量盐酸:加入过量BaCO3固体,过滤 |
| C.除去KCl溶液中的少量MgCl2:加入过量NaOH溶液,过滤 |
| D.除去CO2中的少量HCl:通过足量的NaOH溶液 |
您最近一年使用:0次
名校
7 . 下列除杂方法不正确的是(括号内的物质为杂质)
| A.NaHCO3溶液(Na2CO3):加入适量CaCl2溶液 |
| B.Na2CO3粉末 (NaHCO3):加热至不再产生气体 |
| C.Cl2(HCl):依次通入饱和食盐水、浓硫酸中洗气 |
| D.Na2O2 (Na2O):将混合物置于氧气中加热 |
您最近一年使用:0次
名校
解题方法
8 . 下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去Al2O3中的Fe2O3 | 向固体中先加入过量NaOH溶液,过滤后向滤液中加入过量盐酸 |
| B | 证明溶液中无NH | 向某溶液中滴加少量稀NaOH溶液,将湿润的红色石蕊试纸置于试管口试纸不变蓝 |
| C | 证明二氧化硫具有还原性 | 将二氧化硫通入Ba(NO3)2溶液中,有白色沉淀生成 |
| D | 验证:Ksp(AgI)<Ksp(AgCl) | 向盛有1mL0.1mol·L-1AgNO3溶液的试管中滴加2滴0.1mol·L-1NaCl溶液,有白色沉淀生成,向其中继续滴加0.1mol·L-1KI溶液,有黄色沉淀产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-10-18更新
|
368次组卷
|
3卷引用:重庆市南开中学校2021-2022学年高二上学期期末考试化学试题
名校
9 . 下列有关实验的说法正确的是
A.除去粗盐中的Ca2+、Mg2+、SO 时,应依次加入Na2CO3、BaCl2、NaOH溶液 时,应依次加入Na2CO3、BaCl2、NaOH溶液 |
| B.用硫酸和锌粒制取H2时,加几滴CuSO4溶液可以加快化学反应的速率 |
| C.测中和反应的△H时,将NaOH溶液倒入盐酸后,立即读数会使最终结果偏低 |
| D.配制100mL1mol·L-1NaCl溶液,定容时仰视刻度线会使所配溶液的浓度偏高 |
您最近一年使用:0次
名校
10 . 除去下列物质中所含的杂质,选用的试剂正确的是
| 选项 | 物质(杂质) | 试剂 |
| A | NO2(NO) | O2 |
| B | SO2(HCl) | 饱和NaHSO3溶液 |
| C | FeCl2溶液(FeCl3) | Cu |
| D | NaCl固体(NH4Cl) | NaOH溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-13更新
|
195次组卷
|
2卷引用:重庆市第七中学校2020-2021学年高一下学期半期考试化学试题



