名校
解题方法
1 . 以硫酸工业的尾气 为主要原料制备
为主要原料制备 、
、 的工艺流程如下图所示:
的工艺流程如下图所示:
(1)反应I的化学方程式为___________ 。
(2)生产过程中,得到滤液时,操作所需的玻璃仪器除烧杯外还有___________ 。
(3)反应Ⅲ所得的 可在反应
可在反应___________ (填“I”、“Ⅱ”或“Ⅳ”)中重复使用,检验滤液中阳离子的操作方法是___________ 。
(4)已知 能将氮氧化物转化为无污染性气体(
能将氮氧化物转化为无污染性气体( 不参与氧化还原反应),则
不参与氧化还原反应),则 与
与 反应(忽略
反应(忽略 和
和 的转化),还原剂和氧化剂的比值为
的转化),还原剂和氧化剂的比值为___________ ,当生成的无污染性气体体积为 (标准状况),该反应转移的电子数目为
(标准状况),该反应转移的电子数目为___________ 。
(5)将一定比例的氢气和二氧化硫以一定流速通过装有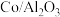 催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:
催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:___________ 。
 为主要原料制备
为主要原料制备 、
、 的工艺流程如下图所示:
的工艺流程如下图所示: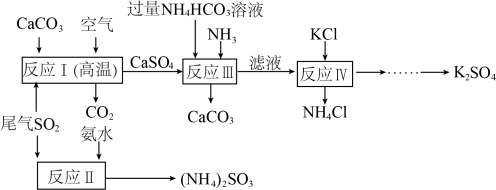
(1)反应I的化学方程式为
(2)生产过程中,得到滤液时,操作所需的玻璃仪器除烧杯外还有
(3)反应Ⅲ所得的
 可在反应
可在反应(4)已知
 能将氮氧化物转化为无污染性气体(
能将氮氧化物转化为无污染性气体( 不参与氧化还原反应),则
不参与氧化还原反应),则 与
与 反应(忽略
反应(忽略 和
和 的转化),还原剂和氧化剂的比值为
的转化),还原剂和氧化剂的比值为 (标准状况),该反应转移的电子数目为
(标准状况),该反应转移的电子数目为(5)将一定比例的氢气和二氧化硫以一定流速通过装有
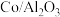 催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:
催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式: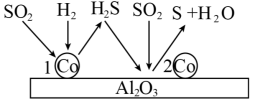
您最近一年使用:0次
名校
解题方法
2 . 海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素。_____________ 操作。
(2)过程c的化学反应方程式_____________________________________ 。
(3)过程b用于海水提溴.主要工业生产流程如下图所示。 ,利用了
,利用了 的氧化性,写出对应反应的离子方程式
的氧化性,写出对应反应的离子方程式_____________________________________________ 。
②吹出塔中通入热空气吹出 ,利用了
,利用了 的
的_____________ (填字母)。
A.氧化性 B.还原性 C.挥发性,沸点比水低 D.易溶于水
(4)实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。
①仪器B的名称是_____________ 。
②该装置中有一处明显的错误是________________________ 。
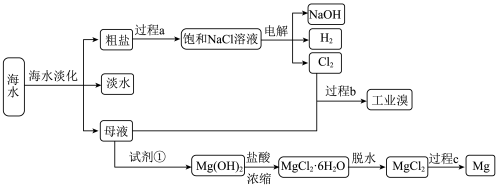
(2)过程c的化学反应方程式
(3)过程b用于海水提溴.主要工业生产流程如下图所示。

 ,利用了
,利用了 的氧化性,写出对应反应的离子方程式
的氧化性,写出对应反应的离子方程式②吹出塔中通入热空气吹出
 ,利用了
,利用了 的
的A.氧化性 B.还原性 C.挥发性,沸点比水低 D.易溶于水
(4)实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。
①仪器B的名称是
②该装置中有一处明显的错误是

您最近一年使用:0次
名校
3 .  是一种常见的化肥,某工厂用石膏、
是一种常见的化肥,某工厂用石膏、 、
、 和
和 制备
制备 的工艺流程如下:
的工艺流程如下:
(1)通入 和
和 的顺序
的顺序__________ (填“能”或“否”)互换,原因为____________ 。
(2)工序②中反应的离子方程式为______________ 。
(3)工序②中 气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量
气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量______ 溶液,若无浑浊出现则 未过量。
未过量。
(4)下列仪器在工序③中不需要的是___________ (填序号)。
①分液漏斗 ②蒸发皿 ③玻璃棒 ④坩埚 ⑤烧杯
(5)工序④的操作步骤为_____________ 、____________ 、过滤、洗涤、干燥。
(6)工厂后面还可以如何操作,提高制备 的经济效益
的经济效益_______________ 。
 是一种常见的化肥,某工厂用石膏、
是一种常见的化肥,某工厂用石膏、 、
、 和
和 制备
制备 的工艺流程如下:
的工艺流程如下:
(1)通入
 和
和 的顺序
的顺序(2)工序②中反应的离子方程式为
(3)工序②中
 气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量
气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量 未过量。
未过量。(4)下列仪器在工序③中不需要的是
①分液漏斗 ②蒸发皿 ③玻璃棒 ④坩埚 ⑤烧杯
(5)工序④的操作步骤为
(6)工厂后面还可以如何操作,提高制备
 的经济效益
的经济效益
您最近一年使用:0次
名校
4 . 下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
| 物质(括号内为杂质) | 除杂试剂 | |
| A | 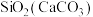 | 稀盐酸 |
| B | 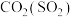 |  溶液 溶液 |
| C | 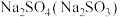 | 稀 |
| D | 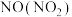 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 由重晶石矿(主要成分是 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是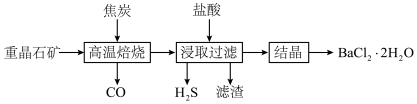
| A.“高温焙烧”前将原料研磨处理,能加快“高温焙烧”的反应速率 |
B.“高温焙烧”时只有 被C还原 被C还原 |
| C.“浸取过滤”发生的主要反应是氧化还原反应 |
| D.“高温焙烧”和“结晶”两处操作均需用到蒸发皿 |
您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组尝试以辉铜矿(Cu2S)为原料制备硫酸铜,其制备路线如下:
(1)Cu2S难溶于稀硫酸中,故需将Cu2S置于________ (填仪器名称)中:灼烧,将其转化为Cu2O。
(2)步骤①生成的SO2会污染大气,可以将其回收利用制取硫酸,工业上以SO2为原料制取硫酸的两步反应的化学方程式是Ⅰ.________________ ,Ⅱ. 。
。
(3)Cu2O加入稀硫酸发生的反应中,氧化剂是________ (填化学式),反应后进行的步骤②的操作名称是________ 。
(4)为了充分利用铜元素,还需在步骤③中将Cu转化为CuSO4。该小组成员提出了两种不同的氧化试剂方案:
请写出利用方案A达成转化目标的反应方程式:____________ 。最终他们选择了方案B,方案B对应的化学方程式为 ,采取方案B的优点是
,采取方案B的优点是______________ (请写出两点)。
(5)采用上述方案B,若最初称取的Cu2S质量为16.0g,为了使Cu完全转化为CuSO4,理论至少需要体积为________ mL的上述H2O2溶液。

(1)Cu2S难溶于稀硫酸中,故需将Cu2S置于
(2)步骤①生成的SO2会污染大气,可以将其回收利用制取硫酸,工业上以SO2为原料制取硫酸的两步反应的化学方程式是Ⅰ.
 。
。(3)Cu2O加入稀硫酸发生的反应中,氧化剂是
(4)为了充分利用铜元素,还需在步骤③中将Cu转化为CuSO4。该小组成员提出了两种不同的氧化试剂方案:
| 方案 | A | B |
| 氧化试剂 | 浓硫酸 | 1 mol/L的H2O2溶液+稀硫酸 |
 ,采取方案B的优点是
,采取方案B的优点是(5)采用上述方案B,若最初称取的Cu2S质量为16.0g,为了使Cu完全转化为CuSO4,理论至少需要体积为
您最近一年使用:0次
名校
解题方法
7 . 2019年诺贝尔化学奖授予在开发锂离子电池方面做出卓越贡献的三位化学家。锂离子二次电池正极铝钴膜主要含有 、Al等,处理该废料的一种工艺如图所示,下列说法正确的是
、Al等,处理该废料的一种工艺如图所示,下列说法正确的是
 、Al等,处理该废料的一种工艺如图所示,下列说法正确的是
、Al等,处理该废料的一种工艺如图所示,下列说法正确的是
A.酸溶时 做氧化剂,且温度不宜过高 做氧化剂,且温度不宜过高 |
| B.加氨水调pH的目的是除铝 |
C.沉钴的离子方程式为: |
| D.该流程中涉及的反应都是氧化还原反应 |
您最近一年使用:0次
名校
8 . 海水是巨大的资源宝库,工业上从海水中获取某些重要化工原料的流程如下图示。 、
、 和
和 等。回答下列问题:
等。回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:____________________ 。
(2)试剂1最好选用__________ (填编号)。
a. b.
b. c.
c. d.NaOH
d.NaOH
(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是____________________ 。
(4)将吹出后的含 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。
①流程中可用热空气吹出溴的原因为_____________________ 。
②“吸收塔”内发生反应的离子方程式:_____________________ 。
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是_____________________ 。
(5)检验吸收塔里的溶液是否含 的方法是
的方法是_______________________ 。
(6)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示:__________ (填一种仪器名称)中加热灼烧。
②向酸化的滤液中加入过氧化氢溶液,可将 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:__________________ 。

 、
、 和
和 等。回答下列问题:
等。回答下列问题:(1)请列举除蒸馏法外海水淡化的一种方法:
(2)试剂1最好选用
a.
 b.
b. c.
c. d.NaOH
d.NaOH(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是
(4)将吹出后的含
 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。①流程中可用热空气吹出溴的原因为
②“吸收塔”内发生反应的离子方程式:
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是
(5)检验吸收塔里的溶液是否含
 的方法是
的方法是(6)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示: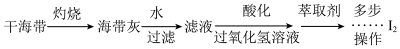
②向酸化的滤液中加入过氧化氢溶液,可将
 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:
您最近一年使用:0次
9 . 废旧锌锰干电池内部的黑色物质A主要含有 、MnOOH、
、MnOOH、 、
、 、碳单质,用黑色物质A制备高纯
、碳单质,用黑色物质A制备高纯 的流程如图:
的流程如图: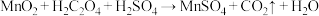 (未配平)。
(未配平)。
(1)第Ⅰ步操作是为了除去可溶性的__________ (填化学式)。
(2)第Ⅰ步后在空气中灼烧的目的有两个,一个是将MnOOH转化为 ,另一个是
,另一个是__________ 为灼烧时,MnOOH与空气中的氧气反应的化学方程式为____________________________ 。
(3)已知: 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
沉淀。第Ⅳ步中的多步操作可按如图步骤进行: 溶滴调节溶液pH的过程中有
溶滴调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为____________ ,你认为操作③中检测的方法及现象是________________ 时可继续进行操作④:操作④中用无水乙醇洗涤的目的是_________________________ (答一条即可)。
 、MnOOH、
、MnOOH、 、
、 、碳单质,用黑色物质A制备高纯
、碳单质,用黑色物质A制备高纯 的流程如图:
的流程如图: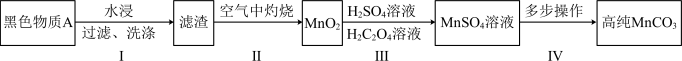
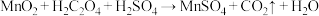 (未配平)。
(未配平)。(1)第Ⅰ步操作是为了除去可溶性的
(2)第Ⅰ步后在空气中灼烧的目的有两个,一个是将MnOOH转化为
 ,另一个是
,另一个是(3)已知:
 难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解;
难溶于水和乙醇,潮湿时易被空气氧化,100℃时开始分解; 在pH大于7.7时,开始转化为
在pH大于7.7时,开始转化为 沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
沉淀。第Ⅳ步中的多步操作可按如图步骤进行:
 溶滴调节溶液pH的过程中有
溶滴调节溶液pH的过程中有 产生,则
产生,则 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
名校
10 . 某硫酸厂用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制备绿矾粗产品(FeSO4·7H2O),设计了如下流程:
回答下列问题:
(1)“试剂a”的化学式为___________ ,“操作”的名称是___________ 。
(2)“酸浸”后溶液呈黄色,“还原”操作是向溶液逐步加入试剂b,溶液变为浅绿色,写出溶液变为浅绿色的离子方程式___________ 。
(3)在“调pH至5-6”步骤中,写出生成Al(OH)3的离子方程式___________ 。
(4)鉴别“滤液1”中金属阳离子的实验方案:取少量滤液1进行___________ (填实验名称),若观察到火焰呈黄色,则证明含有Na+;另外取少量滤液1于试管中,依次滴入___________ 和氯水,若实验现象依次为溶液先无红色,后变红色,则证明含有Fe2+,写出该过程中属于氧化还原反应的离子方程式___________ 。

回答下列问题:
(1)“试剂a”的化学式为
(2)“酸浸”后溶液呈黄色,“还原”操作是向溶液逐步加入试剂b,溶液变为浅绿色,写出溶液变为浅绿色的离子方程式
(3)在“调pH至5-6”步骤中,写出生成Al(OH)3的离子方程式
(4)鉴别“滤液1”中金属阳离子的实验方案:取少量滤液1进行
您最近一年使用:0次



