名校
1 . 铝元素是地壳中含量最多的金属元素(约占地壳总量的7.73%),主要以铝土矿形式存在(主要成分是 )。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
 )。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
A.碱溶①后,溶液中主要含有的阳离子为 和 和 |
B.步骤②通入足量 反应的离子方程式为 反应的离子方程式为 |
| C.灼烧③一般在蒸发皿中进行 |
D.电解④添加冰晶石 (Na3AlF6)的主要作用是降低 的熔融温度 的熔融温度 |
您最近一年使用:0次
2024-01-14更新
|
306次组卷
|
3卷引用:热点11 自然资源的开发利用
名校
2 . 由粗SiO2制备纯SiO2的流程如图所示,下列说法不正确的是
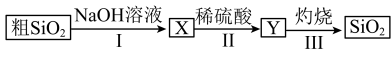
| A.X可用作木材防火剂 |
B.步骤Ⅱ的反应是 |
| C.步骤Ⅱ中的稀硫酸不可用CO2替代 |
| D.若在实验室中完成步骤Ⅲ,一般在蒸发皿中进行 |
您最近一年使用:0次
2023-09-24更新
|
65次组卷
|
16卷引用:合格考汇编8硅及其化合物
(已下线)合格考汇编8硅及其化合物2015-2016学年北京市朝阳区高一上学期期末考试化学试卷安徽省定远重点中学2018-2019学年高一下学期开学考试化学试题【全国百强校】四川省阆中中学2018-2019学年高一下学期期中考试化学试题必修第二册RJ第5章第三节 无机非金属材料 易错疑难集训(三)江苏省南京市中华中学2020-2021学年高一下学期期中考试化学试题人教版(2019)必修第二册第五章第三节 易错疑难集训广东省佛山市顺德区容山中学2022-2023学年高一下学期3月月考化学试题陕西省横山清源中学2022-2023学年高一下学期3月月考化学试题吉林省长春市新解放学校2022-2023学年高一下学期4月月考化学试题浙江台州市永宁中学(筹)2022-2023学年高一下学期3月月考化学试题河南省洛阳市第一高级中学2022-2023学年高一下学期3月月考化学试题江西省乐安县第二中学2022-2023学年高一下学期5月期中考试化学试题安徽省芜湖市第一中学2022-2023学年高一下学期3月份教学质量诊断测试化学试卷黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期开学验收考试化学试题新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高二上学期开学考试化学试题
3 . 氯化钡在工农业生产中应用广泛,常用作媒染剂、消光剂和杀虫剂等。工业上以重晶石(主要成分BaSO4)为原料生产BaCl2的一种工艺流程如图所示。

已知:BaS和BaCl2均易溶于水。
回答下列问题:
(1)“煅烧”前常将重晶石和煤粉碎,目的是_________ 。
(2)“煅烧”过程中,BaSO4中硫元素_________ (填“被氧化”成“被还原”)。
(3)“反应”过程中,生成BaCl2的化学方程式是_________ 。
(4)“系列操作”包括蒸发浓缩、冷却结晶、_________ 、洗涤、干燥等。
(5)若要制得20.8tBaCl2,理论上需消耗BaSO4_________ t。(忽略流程中钡元素损失)

已知:BaS和BaCl2均易溶于水。
回答下列问题:
(1)“煅烧”前常将重晶石和煤粉碎,目的是
(2)“煅烧”过程中,BaSO4中硫元素
(3)“反应”过程中,生成BaCl2的化学方程式是
(4)“系列操作”包括蒸发浓缩、冷却结晶、
(5)若要制得20.8tBaCl2,理论上需消耗BaSO4
您最近一年使用:0次
解题方法
4 . 氯、铁及其化合物在很多领域有重要的用途。
Ⅰ.“84消毒液”能有效杀灭新冠病毒,其有效成分是NaClO。已知某“84消毒液”中NaClO的物质的量浓度为4.00mol/L。
(1)某化学实验小组用该品牌消毒液配制480mL0.20mol/L的NaClO稀溶液,需要此消毒液_____ mL。
(2)完成上述实验必须用到的仪器有玻璃棒、烧杯、胶头滴管、量筒、还有_____ 。
(3)用氢氧化钠溶液和氯气反应制备“84消毒液”反应的化学方程式:_____ 。
Ⅱ.某工厂的工业废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题:
和金属铜。请根据以下流程图,回答下列问题:

(4)操作a的名称为_____ 。
(5)鉴别溶液⑥中的金展阳离子时,应滴加的试剂依次是_____ ,请写出该鉴别过程中属于氧化还原反应的离子方程式_____ 。
(6)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是_____ 。
(7)工业上常用绿矾( )处理工业废水中有毒的重铬酸根离子(
)处理工业废水中有毒的重铬酸根离子( )。反应的离子方程式为
)。反应的离子方程式为 。该反应中
。该反应中_____ 是还原剂;若消耗 ,则转移电子的物质的量为
,则转移电子的物质的量为_____ mol。
Ⅰ.“84消毒液”能有效杀灭新冠病毒,其有效成分是NaClO。已知某“84消毒液”中NaClO的物质的量浓度为4.00mol/L。
(1)某化学实验小组用该品牌消毒液配制480mL0.20mol/L的NaClO稀溶液,需要此消毒液
(2)完成上述实验必须用到的仪器有玻璃棒、烧杯、胶头滴管、量筒、还有
(3)用氢氧化钠溶液和氯气反应制备“84消毒液”反应的化学方程式:
Ⅱ.某工厂的工业废水中含有大量的
 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程图,回答下列问题:
和金属铜。请根据以下流程图,回答下列问题:
(4)操作a的名称为
(5)鉴别溶液⑥中的金展阳离子时,应滴加的试剂依次是
(6)若取2mL溶液⑥加入试管中,然后滴加氢氧化钠溶液,产生的现象是
(7)工业上常用绿矾(
 )处理工业废水中有毒的重铬酸根离子(
)处理工业废水中有毒的重铬酸根离子( )。反应的离子方程式为
)。反应的离子方程式为 。该反应中
。该反应中 ,则转移电子的物质的量为
,则转移电子的物质的量为
您最近一年使用:0次
5 . 根据下图海水综合利用的工业流程图,判断下列说法正确的是
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
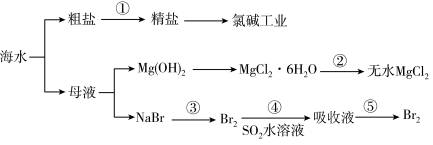
A.除去粗盐中杂质(Mg2+、SO 、Ca2+),加入的药品顺序为: NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 、Ca2+),加入的药品顺序为: NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D.过程④与⑤的目的是为了提纯Br2 |
您最近一年使用:0次
2023-06-15更新
|
271次组卷
|
3卷引用:专题二 物质的检验、除杂和鉴别
名校
6 . 实验室利用废弃旧电池的铜帽(主要成分为Zn和Cu)回收Cu并制备ZnO的实验流程如下:
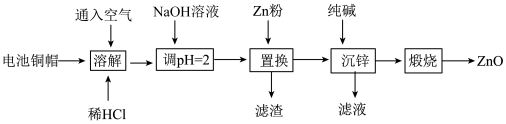
(1)“溶解”时Cu发生反应的离子方程式为___________ 。
(2)“溶解”可适当升高温度以加快反应速率,但温度不宜过高。温度不宜过高的原因是___________ 。
(3)滤渣中的主要物质是___________ (填化学式)。
(4)“沉锌”时生成碱式碳酸锌[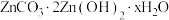 ],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知:
],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知: 加热至125℃、
加热至125℃、 加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与
加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与 的分解温度接近。
的分解温度接近。
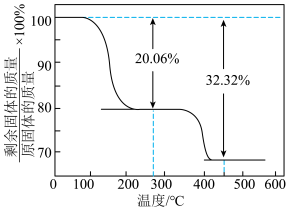
根据以上实现数据计算,确定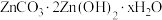 中x的值(写出计算过程)。
中x的值(写出计算过程)。______

(1)“溶解”时Cu发生反应的离子方程式为
(2)“溶解”可适当升高温度以加快反应速率,但温度不宜过高。温度不宜过高的原因是
(3)滤渣中的主要物质是
(4)“沉锌”时生成碱式碳酸锌[
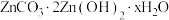 ],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知:
],碱式碳酸锌在空气中加热可转化为ZnO,过程中固体质量随温度的变化关系如下图所示。已知: 加热至125℃、
加热至125℃、 加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与
加热至350℃均分解成ZnO,该碱式碳酸锌失去结晶水的温度与 的分解温度接近。
的分解温度接近。
根据以上实现数据计算,确定
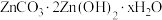 中x的值(写出计算过程)。
中x的值(写出计算过程)。
您最近一年使用:0次
2023-05-16更新
|
550次组卷
|
5卷引用:合格考汇编3氧化还原反应
解题方法
7 . 某工厂拟综合处理含NH 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
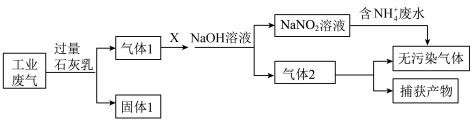
已知:2NaOH+NO+NO2=2NaNO2+H2O、2NaOH+2NO2=NaNO3+NaNO2+H2O。
下列说法不正确的是
 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
已知:2NaOH+NO+NO2=2NaNO2+H2O、2NaOH+2NO2=NaNO3+NaNO2+H2O。
下列说法不正确的是
| A.固体1中只含有CaCO3、CaSO3 | B.X可以是空气,且不能过量 |
| C.捕获剂所捕获的气体主要是CO | D.含NH 废水在该流程中作还原剂 废水在该流程中作还原剂 |
您最近一年使用:0次
名校
8 . 空气吹出法是工业规模海水提溴的常用方法,流程如下:

下列说法不正确的是

下列说法不正确的是
| A.步骤①发生的主要反应为:Cl2+2Br-=Br2+2Cl- |
| B.步骤②③的目的是富集溴元素 |
| C.物质X为HBrO |
| D.空气吹出法用到了溴易挥发的性质 |
您最近一年使用:0次
2023-04-26更新
|
635次组卷
|
6卷引用:专题11 化学与可持续发展(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)
(已下线)专题11 化学与可持续发展(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)第04讲 氧化剂和还原剂 氧化还原反应的配平及规律-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)(已下线)第11讲 氧化还原反应的配平及应用-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)第09练 化学与可持续发展-2023年【暑假分层作业】高一化学(人教版2019必修第二册)北京市中国人民大学附属中学2020届高三化学质检试题北京市中国人民大学附属中学2019-2020学年高三上学期9月质检化学试题
21-22高一·全国·假期作业
解题方法
9 . 硫酸铵是一种常见的化肥,某工厂用石膏、NH3、H2O、CO2制备硫酸铵的工艺流程如下:
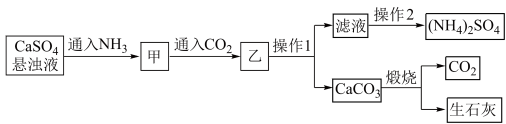
下列说法错误的是

下列说法错误的是
| A.操作1为过滤,操作2为蒸发浓缩、冷却结晶、过滤、洗涤、干燥 |
| B.滤液中的主要阳离子可通过向少量滤液中加NaOH溶液,加热,并用湿润的红色石蕊试纸来检验 |
| C.甲到乙反应的离子方程式为Ca2++2NH3+CO2+H2O = CaCO3↓+2NH4+ |
| D.工艺流程中产生的CO2可循环利用 |
您最近一年使用:0次
2022高一·全国·专题练习
解题方法
10 . 工业上用活性炭吸附海带提碘后废水中的I-制取I2,其流程如下图:

(1)向废水中加入NaNO2并调节pH<4,写出反应的离子方程式_______ 。
(2)用活性炭吸附生成的单质碘的目的是_______ ,用浓、热NaOH洗脱吸附的碘的化学方程式为_______ 。
(3)从调节pH后所得的溶液中获取碘,工业上可用热空气吹出,其原因是_______ ;若取少量该溶液在实验室中分离得到单质碘,需要进行的操作为_______ 。
(4)流程中生成的NO尾气有毒,工业上将其与O2按一定比例通入NaOH制备NaNO2,写出反应的化学方程式:_______ 。
(5)工业上虚框内流程还可用如下图操作代替,评价该图流程的优点_______ (写出一条)。


(1)向废水中加入NaNO2并调节pH<4,写出反应的离子方程式
(2)用活性炭吸附生成的单质碘的目的是
(3)从调节pH后所得的溶液中获取碘,工业上可用热空气吹出,其原因是
(4)流程中生成的NO尾气有毒,工业上将其与O2按一定比例通入NaOH制备NaNO2,写出反应的化学方程式:
(5)工业上虚框内流程还可用如下图操作代替,评价该图流程的优点

您最近一年使用:0次



