1 . 下列物质除杂过程中,选用的试剂和后续操作不能达到目的的是
| 选项 | 物质 | 试剂 | 后续操作 |
| A | NO中混有少量 | 水 | 干燥 |
| B |  中混有少量 中混有少量 | 酸性 溶液 溶液 | 干燥 |
| C |  溶液混有少量 溶液混有少量 | 铁粉 | 过滤 |
| D |  溶液混有少量 溶液混有少量 | 铜粉 | 过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O3既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
以下是一种废钒催化剂回收工艺路线:
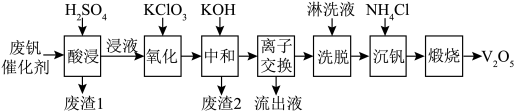
回答下列问题:
(1)“酸浸”时V2O5转化为 , 反应的离子方程式为
, 反应的离子方程式为___________ ,同时V2O4转化为 。“废渣1”的主要成分是
。“废渣1”的主要成分是______ 。
(2)“氧化”中使 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为______ 。
(3)“中和”后的溶液中,钒主要以 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
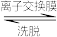
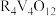 +
+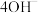 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈_____ 性(填“敢”或“碱”)。
(4)检验“流出液”中含量最多的阳离子,其实验操作称为___ 。
(5)“煅烧”中发生反应的化学方程式 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式_________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.20~2.90 | 2.8~3.32 | 22~28 | 60~65 | 1~2 | <1 |

回答下列问题:
(1)“酸浸”时V2O5转化为
 , 反应的离子方程式为
, 反应的离子方程式为 。“废渣1”的主要成分是
。“废渣1”的主要成分是(2)“氧化”中使
 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为(3)“中和”后的溶液中,钒主要以
 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
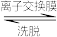
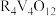 +
+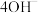 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈(4)检验“流出液”中含量最多的阳离子,其实验操作称为
(5)“煅烧”中发生反应的化学方程式
 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式
您最近一年使用:0次
名校
3 . 氯化钠既是我们日常生活中不可缺少的调味品,也是一种重要的化工原料。某化学兴趣小组进行粗盐(主要含有泥沙、Na+、Ca2+、Mg2+、SO42—、Cl—)提纯实验。
Ⅰ.甲同学的操作步骤如图所示:
依据所学知识回答下列问题:
(1)操作①所用的玻璃仪器包括烧杯、___________ ;操作(4)的名称是___________ 。
(2)从产品纯度考虑,试剂a、b、c可以分别为下列选项中的___________ (填选项);加入盐酸时发生反应生成CO2的离子方程式为___________ 。
A.BaCl2溶液、NaOH溶液、Na2SO4溶液
B.NaOH溶液、BaCl2溶液、Na2CO3溶液
C.BaCl2溶液、Na2SO4溶液、NaOH溶液
Ⅱ.乙同学对甲同学的实验进行评价,提出了一些猜想,并设计实验进行验证:
供选择的试剂:稀盐酸、Na2SO4溶液、BaCl2溶液。
(3)完成上述表格中:①___________ ;②___________ ;③___________ ;④___________ 。
(4)根据乙同学的实验,请对甲同学的实验设计进行评价:___________ 。
Ⅰ.甲同学的操作步骤如图所示:

依据所学知识回答下列问题:
(1)操作①所用的玻璃仪器包括烧杯、
(2)从产品纯度考虑,试剂a、b、c可以分别为下列选项中的
A.BaCl2溶液、NaOH溶液、Na2SO4溶液
B.NaOH溶液、BaCl2溶液、Na2CO3溶液
C.BaCl2溶液、Na2SO4溶液、NaOH溶液
Ⅱ.乙同学对甲同学的实验进行评价,提出了一些猜想,并设计实验进行验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想1:固体A中含BaCO3 | 取少量固体A于试管中,先加入足量①___________,再加入②___________ | 有气泡产生,无白色沉淀 | ③___________ |
| 猜想2:最后制得的NaCl晶体中还含有Na2SO4 | 取少量提纯后的NaCl晶体于试管中,加入适量的蒸馏水溶解,滴入稀HNO3和BaCl2溶液 | ④___________ | 猜想2成立 |
(3)完成上述表格中:①
(4)根据乙同学的实验,请对甲同学的实验设计进行评价:
您最近一年使用:0次
4 . 我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。
I.如图为联合制碱法的主要过程(部分物质已略去):
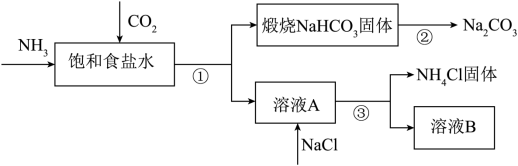
(1)①~③的涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)煅烧NaHCO3固体的化学方程式是___________ 。
(3)上述联合制碱法流程可以循环使用的中一种物质是___________ (填化学式)。
II.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。
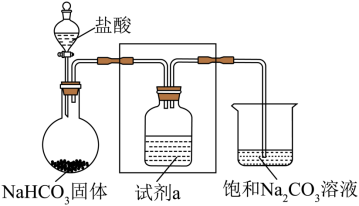
(4)方框中为洗气装置,请将该装置图补充完整___________ 。
(5)试剂a为饱和NaHCO3溶液,其作用是___________ 。
(6)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因___________ 。
(7)下列选项中哪种物质可以鉴别浓度相同的 和
和 ___________。
___________。
I.如图为联合制碱法的主要过程(部分物质已略去):

(1)①~③的涉及的操作方法中,包含过滤的是
(2)煅烧NaHCO3固体的化学方程式是
(3)上述联合制碱法流程可以循环使用的中一种物质是
II.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。

(4)方框中为洗气装置,请将该装置图补充完整
(5)试剂a为饱和NaHCO3溶液,其作用是
(6)实验持续-段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因
(7)下列选项中哪种物质可以鉴别浓度相同的
 和
和 ___________。
___________。| A.澄清石灰水 | B.氢氧化钠溶液 | C.稀盐酸 | D. 溶液 溶液 |
您最近一年使用:0次
5 . 活化二氧化锰在能源化学上有着重要作用,工业上利用精制软锰矿粉(MnO2)通过下列流程制备:
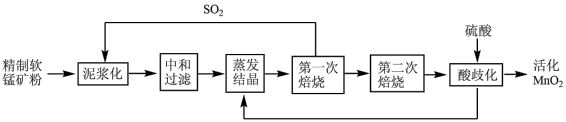
已知:蒸发结晶得到MnSO4。
(1)将软锰矿粉泥浆化的目的是________ ;反应方程式为_____________ ;
(2)“第一次焙烧”温度是1000℃,生成Mn3O4、SO2和O2,“第二次焙烧”温度为700℃,产物为Mn2O3;700℃时焙烧的氧化剂与还原剂物质的量比为_____________ 。
(3)“酸歧化”的离子方程式为________________ 。
(4)活化MnO2中不能含有铜、铅等重金属元素,在“中和过滤”前需要加入某种盐溶液除去重金属离子,该盐的化学式是___________ 。(已知CuS、PbS、PbSO4均为难溶物)
(5)“第一次焙烧”每产生3molSO2,若完全转化为硫酸,理论上需要再充入空气_____ L。(标准状况下)

已知:蒸发结晶得到MnSO4。
(1)将软锰矿粉泥浆化的目的是
(2)“第一次焙烧”温度是1000℃,生成Mn3O4、SO2和O2,“第二次焙烧”温度为700℃,产物为Mn2O3;700℃时焙烧的氧化剂与还原剂物质的量比为
(3)“酸歧化”的离子方程式为
(4)活化MnO2中不能含有铜、铅等重金属元素,在“中和过滤”前需要加入某种盐溶液除去重金属离子,该盐的化学式是
(5)“第一次焙烧”每产生3molSO2,若完全转化为硫酸,理论上需要再充入空气
您最近一年使用:0次
解题方法
6 . 尖晶石矿的主要成分为MgAl2O4(含SiO2杂质)。已知:MgAl2O4(s)+4Cl2(g)=MgCl2(s)+2A1Cl3(g)+2O2(g),该反应难以发生,但采用“加炭氯化法”可以制备MgCl2和A1Cl3(A1Cl3在180℃升华)下列说法不正确的是
| A.MgCl2和AlCl3混合固体中,可以加入过量氨水,再分离提纯 |
| B.输送气体的管道温度,至少要达到180℃ |
| C.加炭既可以增加反应的趋势,也可以提供反应需要的能量 |
| D.将MgAl2O4溶于盐酸可以得到MgCl2和AlCl3 |
您最近一年使用:0次
7 . 某废旧金属材料中主要为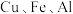 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾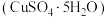 的一种流程如下:
的一种流程如下: 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。
回答下列问题:
(1)“破碎”的目的是___________ 。
(2)“碱浸”时发生反应的离子方程式为___________ 。
(3)“酸浸、氧化”的温度不宜过高,原因是___________ ;“滤渣2”的主要成分是___________ (填化学式)。
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有 的是___________。
的是___________。
(5)测定产品的纯度:准确称取胆矾样品 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为___________ (保留3位有效数字)。
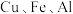 及其氧化物的混合物。利用该废旧金属材料制备胆矾
及其氧化物的混合物。利用该废旧金属材料制备胆矾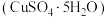 的一种流程如下:
的一种流程如下: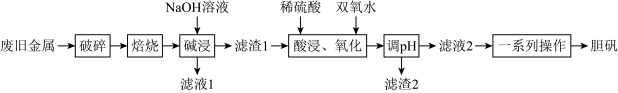
 可将
可将 与
与 分离,但不能将
分离,但不能将 与
与 分离。
分离。回答下列问题:
(1)“破碎”的目的是
(2)“碱浸”时发生反应的离子方程式为
(3)“酸浸、氧化”的温度不宜过高,原因是
(4)下列选项中可以检验酸浸、氧化后溶液里是否含有
 的是___________。
的是___________。A. 溶液,新制氯水 溶液,新制氯水 | B.酸性高锰酸钾溶液 |
C. 溶液 溶液 | D.淀粉 试纸 试纸 |
(5)测定产品的纯度:准确称取胆矾样品
 ,完全溶解于稀硫酸中,用过量的
,完全溶解于稀硫酸中,用过量的 溶液沉淀其中的铜元素,得到蓝色沉淀质量为
溶液沉淀其中的铜元素,得到蓝色沉淀质量为 。该样品纯度为
。该样品纯度为
您最近一年使用:0次
名校
解题方法
8 . 下列除去杂质(括号中的物质为杂质)的方法中,错误的是
| 选项 | 被提纯的物质 | 除杂试剂 |
| A | NaBr溶液(NaCl) | 通入适量的 |
| B | MgO固体( ) ) | 加入足量NaOH溶液,过滤、洗涤 |
| C |  气体(HCl) 气体(HCl) | 依次通过饱和 溶液和浓硫酸 溶液和浓硫酸 |
| D | NaOH溶液( ) ) | 加入适量的氢氧化钡溶液,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 某废旧金属材料中主要含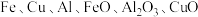 (其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收
(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收 、
、 、绿矾等。
、绿矾等。
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去___________ 。
(2)“碱浸”时发生反应的化学方程式为___________ 。
(3)操作I、II中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是___________ 。
(4)第一次酸浸完全后“加入过量试剂a”后发生的化学反应中有一个属于化合反应,其离子方程式为___________ 。
(5)①滤液II中可能含有因氧气的作用而产生少量杂质离子,该反应的离子方程式为___________ 。
②设计实验检验滤液II中是否含有上述杂质离子采用的试剂为___________ 溶液。
(6)若要定量测定所得绿矾纯度,可通过如下方法:称取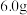 样品用稀硫酸溶解,滴加
样品用稀硫酸溶解,滴加 的酸性溶液,
的酸性溶液, 恰好完全反应时,消耗酸性
恰好完全反应时,消耗酸性 溶液的体积为
溶液的体积为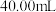 ,则
,则 的纯度为
的纯度为___________ 。(结果保留三位有效数字)已知: (未配平)
(未配平)
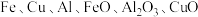 (其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收
(其余成分与酸碱都不反应)和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收 、
、 、绿矾等。
、绿矾等。
(1)“焙烧”的目的主要是将金属单质转化为氧化物,并除去
(2)“碱浸”时发生反应的化学方程式为
(3)操作I、II中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是
(4)第一次酸浸完全后“加入过量试剂a”后发生的化学反应中有一个属于化合反应,其离子方程式为
(5)①滤液II中可能含有因氧气的作用而产生少量杂质离子,该反应的离子方程式为
②设计实验检验滤液II中是否含有上述杂质离子采用的试剂为
(6)若要定量测定所得绿矾纯度,可通过如下方法:称取
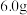 样品用稀硫酸溶解,滴加
样品用稀硫酸溶解,滴加 的酸性溶液,
的酸性溶液, 恰好完全反应时,消耗酸性
恰好完全反应时,消耗酸性 溶液的体积为
溶液的体积为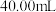 ,则
,则 的纯度为
的纯度为 (未配平)
(未配平)
您最近一年使用:0次
名校
10 . 下列混合物分离(或除杂)的方法正确的是
| A.除去Fe粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
B.除去 溶液中混有的 溶液中混有的 :加适量酸性高锰酸钾溶液 :加适量酸性高锰酸钾溶液 |
C.除去 溶液中的 溶液中的 :加适量稀盐酸 :加适量稀盐酸 |
D.除去 中的少量 中的少量 :加入过量氢氧化钠溶液,过滤、洗涤 :加入过量氢氧化钠溶液,过滤、洗涤 |
您最近一年使用:0次



