1 . 关于下列实验操作、现象和相应结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用CCl4萃取碘水后,先从下口放出下层溶液,再向另一个烧杯中从下口放出上层液体 | 下层溶液为紫色,上层为无色 | CCl4的密度比水大且碘在CCl4中溶解度比在水中的大 |
| B | 向过氧化钠样品中滴加过量的盐酸,将生成的气体通入CaCl2溶液 | 无白色沉淀产生 | 样品未变质 |
| C | 鉴别碳酸钠、碳酸氢钠溶液,向装有两溶液的两支试管中滴加氢氧化钡溶液 | 一支试管无明显现象,一支试管中产生白色沉淀 | 产生白色沉淀的溶液是碳酸钠 |
| D | 向NaBr溶液中加入少量苯,通入适量Cl2后,充分振荡、静置 | 有机层变为橙红色 | Cl2的氧化性强于Br2 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . 下列实验方案中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去 中混有的 中混有的 | 将气体通入饱和 溶液中洗气 溶液中洗气 |
| B | 检验绿矾晶体是否已变质 | 将绿矾样品溶于稀 后,滴加 后,滴加 溶液,观察溶液是否变红 溶液,观察溶液是否变红 |
| C | 检验 在 在 溶液中是否发生水解 溶液中是否发生水解 | 将 与 与 溶液共热,冷却后,取出上层水溶液,加入 溶液共热,冷却后,取出上层水溶液,加入 溶液,观察是否产生白色沉淀 溶液,观察是否产生白色沉淀 |
| D | 从碘水中提取 | 将碘水与苯混合充分振荡、静置后,下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,继续从分液漏斗下端管口放出上层液体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
3 . 下列实验方案中,可以达到实验目的的是( )
| 选项 | 实验操作与现象 | 目的或结论 |
| A | 向装有溴水的分液漏斗中加入裂化汽油,充分振荡、静置后分层 | 裂化汽油可萃取溴 |
| B | 用pH试纸分别测定相同温度和相同浓度的CH3COONa溶液和NaClO溶液的pH | 验证酸性: CH3COOH>HClO |
| C | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 | Fe(NO3)2晶体已氧化变质 |
| D | 取少量某无色弱酸性溶液,加入过量NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 溶液中一定含有NH4+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 下列说法正确的是 ( )
| A.FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 |
| B.去除粗食盐水中Ca2+、SO42-等杂质,应先加Na2CO3溶液,后加BaCl2溶液 |
| C.用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 |
| D.用BaCl2溶液和稀盐酸来检验Na2CO3样品是否含有SO42-杂质 |
您最近半年使用:0次
名校
5 . 由下列实验及现象,推出的相应结论正确的是( )
| 实验 | 现象 | 结论 |
| A.用铂丝蘸取某金属的盐溶液, 在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+,不含 K+ |
| B.①取少量绿矾样品,加水溶解, 滴加 KSCN 溶液 ②向溶液中通入空气 | ①溶液颜色无变化 ②溶液逐渐变红 | ①绿矾样品未变质 ②Fe2+易被空气氧化为 Fe3+ |
| C.①某溶液中加入 Ba(NO3)2 溶 液 ②再加入足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 SO42﹣ |
| D.向碘水中加入等体积 CCl4, 振荡后静置 | 上层接近无色,下层显紫红色 | I2 在 CCl4 中的溶解度小于在水中 的溶解度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2018-12-26更新
|
232次组卷
|
3卷引用:【全国百强校】山西省太原市第五中学2018-2019学年高一上学期12月月考化学试题
6 . 下列说法正确的是
| A.FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 |
| B.食盐水中Ca2+、SO42-等杂质的去除,应先加Na2CO3溶液,后加BaCl2溶液 |
| C.用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 |
| D.用BaCl2溶液来检验暴露在空气中的Na2SO3样品是否变质 |
您最近半年使用:0次
2016-12-09更新
|
356次组卷
|
4卷引用:2015-2016学年江苏省宿迁市高一上学期期末考试化学试卷
解题方法
7 . 某煤化工厂废水含有大量有机物、氨氮、氰化物、悬浮颗粒等有害物质。处理流程如图所示。
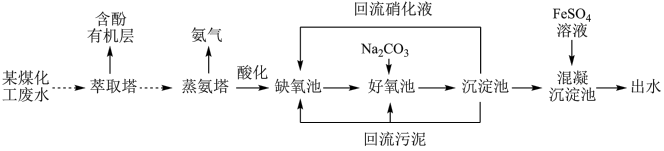
(1)萃取塔中经过_______ (填写操作名称)可将含酚有机层分离出来。
(2)蒸氨塔中需要连续加入碱液并保持较高温度。请从化学平衡角度解释回答下列问题。
①写出蒸氨塔中主要的化学平衡的离子方程式:_______ 。
②加入碱液以及保持较高温度的原因:_______ 。
(3)缺氧池中含有 及CN-,其中CN-(C为+2价)可被回流硝化液中的
及CN-,其中CN-(C为+2价)可被回流硝化液中的 氧化为无毒气体。请预测CN-反应后的产物为
氧化为无毒气体。请预测CN-反应后的产物为_______ 和_______ 。请分析由蒸氨塔到缺氧池工序酸化的目的:_______ 。
(4)好氧池中富含O2与 反应后的产物为
反应后的产物为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
(5)下列关于混凝沉淀池中的说法合理的是_______ (填写序号)。
a.混凝沉淀池溶液的pH控制在8.3左右
b.FeSO4水解产生Fe(OH)2胶体,吸附水中的悬浮颗粒
c.相同条件下,使用Fe2(SO4)3可获得相同的混凝效果
(6)出水检测
甲醛法可以测定水样中 的含量,其反应原理为
的含量,其反应原理为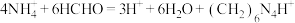 ,然后用NaOH标准溶液滴定反应生成的酸[滴定时,
,然后用NaOH标准溶液滴定反应生成的酸[滴定时,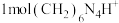 与1molH+相当]。
与1molH+相当]。
实验步骤:
i.移取VmL出水样品,以酚酞为指示剂,用cmol/LNaOH标准液滴定至终点,中和样品中的酸。消耗NaOH溶液的体积为V1mL;
ii.另取同样体积的样品,加入足量的中性甲醛溶液,摇匀,静置5min后,加入1~2滴酚酞溶液,用NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为V2mL。
①步骤ii中滴定至终点的现象为_______ 。
②该水样中残留 浓度为
浓度为_______ mol/L。

| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe2+ | 6.3 | 8.3 |
| Fe3+ | 2.7 | 3.7 |
(2)蒸氨塔中需要连续加入碱液并保持较高温度。请从化学平衡角度解释回答下列问题。
①写出蒸氨塔中主要的化学平衡的离子方程式:
②加入碱液以及保持较高温度的原因:
(3)缺氧池中含有
 及CN-,其中CN-(C为+2价)可被回流硝化液中的
及CN-,其中CN-(C为+2价)可被回流硝化液中的 氧化为无毒气体。请预测CN-反应后的产物为
氧化为无毒气体。请预测CN-反应后的产物为(4)好氧池中富含O2与
 反应后的产物为
反应后的产物为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(5)下列关于混凝沉淀池中的说法合理的是
a.混凝沉淀池溶液的pH控制在8.3左右
b.FeSO4水解产生Fe(OH)2胶体,吸附水中的悬浮颗粒
c.相同条件下,使用Fe2(SO4)3可获得相同的混凝效果
(6)出水检测
甲醛法可以测定水样中
 的含量,其反应原理为
的含量,其反应原理为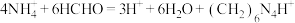 ,然后用NaOH标准溶液滴定反应生成的酸[滴定时,
,然后用NaOH标准溶液滴定反应生成的酸[滴定时,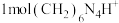 与1molH+相当]。
与1molH+相当]。实验步骤:
i.移取VmL出水样品,以酚酞为指示剂,用cmol/LNaOH标准液滴定至终点,中和样品中的酸。消耗NaOH溶液的体积为V1mL;
ii.另取同样体积的样品,加入足量的中性甲醛溶液,摇匀,静置5min后,加入1~2滴酚酞溶液,用NaOH标准溶液滴定至终点,消耗NaOH溶液的体积为V2mL。
①步骤ii中滴定至终点的现象为
②该水样中残留
 浓度为
浓度为
您最近半年使用:0次
8 . 某化学小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁(Fe2O3),并进行铁含量的测定。主要操作步骤如下:
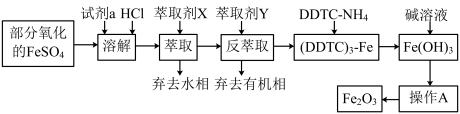
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH 。
。
请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式_________ 。
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的___ 放气;为提高萃取率和产品产量,实验时应进行的操作是__________ 。
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)____ 。
(4)操作A为_____ 、_____ 、______ 。产品处理时,温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图所示,则温度最好控制在______ ℃。

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用______ (填仪器名称)移取25.00 mL溶液于锥形瓶中,用0.l000mol/L的K2Cr2O7溶液进行滴定,消耗K2Cr2O7溶液20.60mL。产品中铁的含量为______ (假设杂质不与K2Cr2O7反应)。

已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH
 。
。请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式
(2)溶液中加入萃取剂X,转移至分液漏斗中,塞上玻璃塞振摇,振摇几次后需打开分液漏斗的
(3)可作反萃取的萃取剂Y的最佳试剂是(填试剂名称)
(4)操作A为

(5)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100mL溶液,用
您最近半年使用:0次
2020-07-28更新
|
388次组卷
|
6卷引用:山东省威海荣成市2020届高三上学期期中考试化学试题
9 . Fe2O3俗称氧化铁红,常用作油漆等着色剂。某实验小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁并进行铁含量的测定。实验过程中的主要操作步骤如图1。
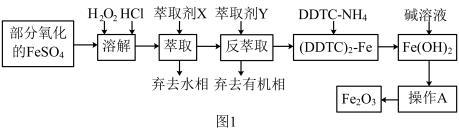
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离;
②3DDTCNH4+Fe3+===(DDTC)3Fe↓+3NH4+。
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是______________ 。
A.FeSO4原料中含有的Ca2+、Cu2+等杂质离子几乎都在水相中
B.为提高萃取率和产品产量,实验时分多次萃取并合并萃取液
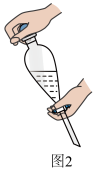
C.溶液中加入X,转移至分液漏斗中,塞上玻璃塞,如图2用力振摇
D.振摇几次后需打开分液漏斗上口的玻璃塞放气
(2)下列试剂中,可作反萃取的萃取剂Y最佳选择是________ 。
A.高纯水 B.盐酸 C.稀硫酸 D.酒精
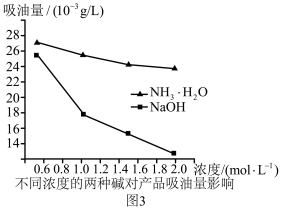
(3)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图3所示,则上述实验过程中选用的碱溶液为_______________ (填“NaOH”或“NH3·H2O”),反应的化学方程式为__________ 。
(4)操作A的步骤包括___________________________________________ 。
(5)现准确称取4.000 g样品,经酸溶、还原为Fe2+,在容量瓶中配成100 mL溶液,用移液管移取25.00 mL溶液于锥形瓶中,用0.100 0 mol/L的K2Cr2O7溶液进行滴定(还原产物是Cr3+),消耗K2Cr2O7溶液20.80 mL。
①用移液管从容量瓶中吸取25.00 mL溶液后,把溶液转移到锥形瓶中的具体操作为______________
②产品中铁的含量为___________ (假设杂质不与K2Cr2O7反应)。

已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离;
②3DDTCNH4+Fe3+===(DDTC)3Fe↓+3NH4+。
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是

A.FeSO4原料中含有的Ca2+、Cu2+等杂质离子几乎都在水相中
B.为提高萃取率和产品产量,实验时分多次萃取并合并萃取液
C.溶液中加入X,转移至分液漏斗中,塞上玻璃塞,如图2用力振摇
D.振摇几次后需打开分液漏斗上口的玻璃塞放气
(2)下列试剂中,可作反萃取的萃取剂Y最佳选择是
A.高纯水 B.盐酸 C.稀硫酸 D.酒精
(3)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图3所示,则上述实验过程中选用的碱溶液为

(4)操作A的步骤包括
(5)现准确称取4.000 g样品,经酸溶、还原为Fe2+,在容量瓶中配成100 mL溶液,用移液管移取25.00 mL溶液于锥形瓶中,用0.100 0 mol/L的K2Cr2O7溶液进行滴定(还原产物是Cr3+),消耗K2Cr2O7溶液20.80 mL。
①用移液管从容量瓶中吸取25.00 mL溶液后,把溶液转移到锥形瓶中的具体操作为
②产品中铁的含量为
您最近半年使用:0次
18-19高二下·浙江宁波·期中
名校
解题方法
10 . Fe2O3俗称氧化铁红,常用作油漆等着色剂。某实验小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁并进行铁含量的测定,实验过程中的主要操作步骤如下:
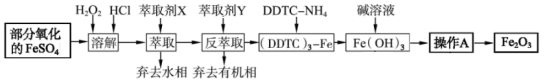
已知:①在盐酸浓度较高时,Fe3+与甲基异丁基甲酮形成可溶性的化合物,当盐酸浓度降低时,该化合物解离。
②3DDTC—NH4+Fe3+=(DDTC)3—Fe↓+3NH4+。
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是_________。
(2)下列试剂中,可作反萃取的萃取剂Y最佳选择是__________。
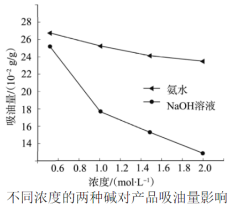
(3)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图所示,则上述实验过程中选用的碱溶液为_________ (填“NaOH”或“NH3·H2O”),反应的化学方程式为___________ 。
(4)①操作A为抽滤、______ 、____ ;
②有关抽滤,下列说法正确的是____ 。

A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 滤纸应比漏斗内径略小,且能盖住所有小孔
C. 抽滤得到的滤液应从吸滤瓶的支管口倒出
D. 右图所示的抽滤装置中,只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
E. 抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸
F. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
(5)现准确称取4.000 g,样品,经酸溶、还原为Fe2+,用容量瓶配成100 mL溶液。用移液管移取25.00 mL溶液于锥形瓶中,用0.l200 mol·L-1的KMnO4溶液进行滴定(还原产物是Mn2+,假设杂质不与KMnO4反应),记录数据如下:
①用移液管从容量瓶中吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为______ ;
②所用的指示剂为____ ;KMnO4溶液置于_____ (酸式、碱式)滴定管中。
A. 酚酞 B. 甲基橙 C. 石蕊 D. 不需要

已知:①在盐酸浓度较高时,Fe3+与甲基异丁基甲酮形成可溶性的化合物,当盐酸浓度降低时,该化合物解离。
②3DDTC—NH4+Fe3+=(DDTC)3—Fe↓+3NH4+。
请回答下列问题:
(1)用萃取剂X萃取的步骤中,以下关于萃取分液操作的叙述中,正确的是_________。

| A.FeSO4原料中含有的Ca2+、Cu2+等杂质离子几乎都在水相中 |
| B.为提高萃取率和产品产量,实验时分多次萃取并合并萃取液 |
| C.溶液中加入X,转移至分液漏斗中,塞上玻璃塞,如图用力振摇 |
| D.振摇几次后需打开分液漏斗上口的玻璃塞放气 |
| E.经几次振摇并放气后,手持分液漏斗静置待液体分层 |
| F.分液时,将分液漏斗上的玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔,打开旋塞,待下层液体完全流尽时,关闭旋塞后再从上口倒出上层液体 |
| A.高纯水 | B.盐酸 | C.稀硫酸 | D.酒精 |

(4)①操作A为抽滤、
②有关抽滤,下列说法正确的是

A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 滤纸应比漏斗内径略小,且能盖住所有小孔
C. 抽滤得到的滤液应从吸滤瓶的支管口倒出
D. 右图所示的抽滤装置中,只有一处错误,即漏斗颈口斜面没有对着吸滤瓶的支管口
E. 抽滤完毕后,应先拆下连接抽气泵和吸滤瓶的橡皮管,再关水龙头,以防倒吸
F. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
(5)现准确称取4.000 g,样品,经酸溶、还原为Fe2+,用容量瓶配成100 mL溶液。用移液管移取25.00 mL溶液于锥形瓶中,用0.l200 mol·L-1的KMnO4溶液进行滴定(还原产物是Mn2+,假设杂质不与KMnO4反应),记录数据如下:
| 滴定序号 | 待测溶液体积/mL | 消耗KMnO4标准溶液体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 1 | 25.00 | 1.15 | 21.98 |
| 2 | 25.00 | 0.50 | 21.96 |
| 3 | 25.00 | 0 | 20.77 |
①用移液管从容量瓶中吸取25.00mL溶液后,把溶液转移到锥形瓶中的具体操作为
②所用的指示剂为
A. 酚酞 B. 甲基橙 C. 石蕊 D. 不需要
您最近半年使用:0次



