名校
1 . KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。
(一)KMnO4的制备,分步骤I、II两步进行。
步骤I:先利用如图所示装置制备K2MnO4


(1)装置A应选用______ (填a、b或c)。
(2)装置B中所盛试剂的名称为______ 。
(3)装置C处反应生成K2MnO4的化学方程式为______ 。
步骤II:由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③再将滤液进行一系列处理,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为______ ;
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。某化学小组选用酸性高锰酸钾溶液和草酸溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录]
(5)为完成实验目的,H2C2O4溶液的物质的量浓度不低于______ 。
(6)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=______ 。
(一)KMnO4的制备,分步骤I、II两步进行。
步骤I:先利用如图所示装置制备K2MnO4


(1)装置A应选用
(2)装置B中所盛试剂的名称为
(3)装置C处反应生成K2MnO4的化学方程式为
步骤II:由K2MnO4制备KMnO4。已知:K2MnO4易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③再将滤液进行一系列处理,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为
(二) KMnO4的性质。已知:KMnO4具有强氧化性,可与草酸(H2C2O4)反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。某化学小组选用酸性高锰酸钾溶液和草酸溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录]
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 一定浓度mol·L-1 H2C2O4溶液 | H2O | 0.05 mol·L-1 KMnO4溶液 | 3 mol·L-1稀硫酸 | ||
| 1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
| 2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
| 3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
(6)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率为:v(KMnO4)=
您最近一年使用:0次
2 . 下列实验装置正确且能达到实验目的的是
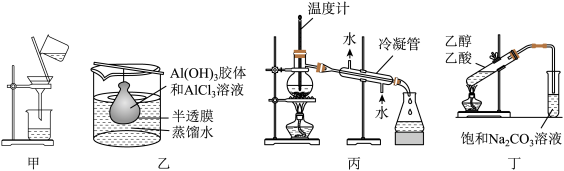

| A.用甲装置除去食盐水中混有的不溶杂质 |
| B.用乙装置提纯Al(OH)3胶体 |
| C.用丙装置分离苯和硝基苯的混合物 |
| D.用丁装置进行制备并收集乙酸乙酯 |
您最近一年使用:0次
2022-08-27更新
|
112次组卷
|
3卷引用:黑龙江省大庆铁人中学2021-2022学年高二下学期期末考试化学试题
3 . 侯德榜制碱法的反应原理为NH3+CO2+H2O+NaCl = NaHCO3↓+NH4Cl,下列装置制取碳酸钠粗品能达到实验目的的是
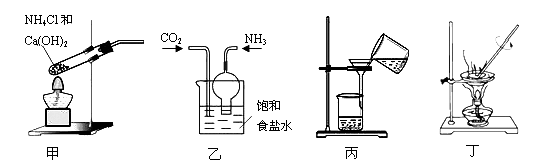

| A.用装置甲制取氨气 | B.用装置乙制取碳酸氢钠 |
| C.用装置丙分离碳酸氢钠 | D.用装置丁加热碳酸氢钠制备碳酸钠 |
您最近一年使用:0次
4 . 用下列实验装置(部分夹持装置略去)进行相应的实验,能达到实验目的的是
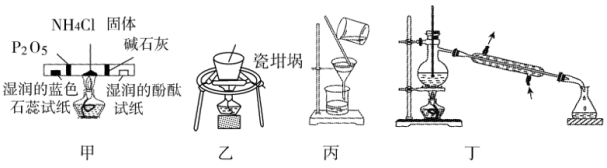

| A.用装置甲检验氯化铵受热分解生成的两种气体 |
| B.用装置乙加热熔融的纯碱固体 |
C.用装置丙提纯 胶体 胶体 |
| D.用装置丁可分离苯(沸点80.1℃)和溴苯(沸点156.2℃) |
您最近一年使用:0次
2021-01-07更新
|
705次组卷
|
5卷引用:黑龙江省大庆实验中学2021届高三上学期期末考试理科综合化学试题
5 . 用下列装置进行相应的实验,,能达到实验目的的是
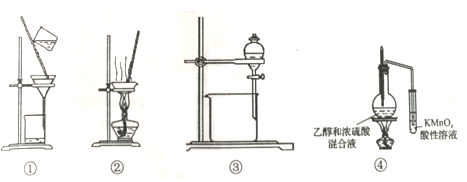

| A.图①所示装置用于粗盐提纯中除掉泥沙 |
| B.图②所示装置用于蒸干氯化镁溶液制无水MgCl2 |
| C.图③所示装置用于以己烯为萃取剂萃取溴水中的溴单质 |
| D.图④所示装置用于验证乙烯的生成 |
您最近一年使用:0次
2018-10-29更新
|
667次组卷
|
4卷引用:黑龙江省宾县第一中学2019-2020学年高二下学期期末考试化学试题
名校
解题方法
6 . 实验室由安息香制备二苯乙二酮的反应式如下:
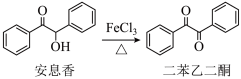
相关信息列表如下:
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0g FeCl3∙6H2O,边搅拌边加热,至固体全部溶解。②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。

回答下列问题:
(1)仪器A中应加入___________ (填“水”或“油”)作为热传导介质。
(2)仪器B的名称是___________ ;冷却水应从___________ (填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是___________ 。
(4)在本实验中,FeCl3为氧化剂且过量,其还原产物为___________ ;某同学尝试改进本实验:采用催化量的FeCl3并通入空气制备二苯乙二酮。该方案是否可行?简述判断理由___________ 。
(5)若粗品中混有少量未氧化的安息香,可用少量___________ 洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(6)本实验的产率最接近于___________ (填标号)。
a.85% b.80% c.75% d.70%

相关信息列表如下:
| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水 溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水 溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |
①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0g FeCl3∙6H2O,边搅拌边加热,至固体全部溶解。②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。

回答下列问题:
(1)仪器A中应加入
(2)仪器B的名称是
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(4)在本实验中,FeCl3为氧化剂且过量,其还原产物为
(5)若粗品中混有少量未氧化的安息香,可用少量
a.热水 b.乙酸 c.冷水 d.乙醇
(6)本实验的产率最接近于
a.85% b.80% c.75% d.70%
您最近一年使用:0次
2023-12-28更新
|
167次组卷
|
2卷引用:黑龙江省大庆市肇州县第二中学2023-2024学年高三上学期12月月考化学试题
名校
7 . 某探究活动小组根据侯德榜制碱原理,按下面设计的方案制备碳酸氢钠。实验装置如图所示(图中夹持、固定用的仪器未画出)。下列说法正确的是
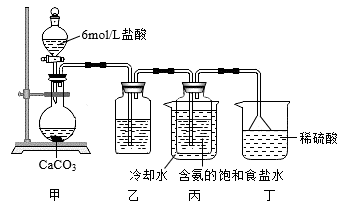

| A.乙装置中盛放的是 NaOH 溶液,以便除去 HCl 气体 |
| B.丙装置中的溶液变浑浊,因为有碳酸氢钠晶体析出 |
| C.丁装置中倒扣的漏斗主要作用是防止污染性空气逸出 |
| D.实验结束后,分离碳酸氢钠的操作是蒸发结晶 |
您最近一年使用:0次
2020-12-23更新
|
535次组卷
|
4卷引用:黑龙江省哈尔滨市德强高中2021-2022学年高一上学期期中考试化学试题
黑龙江省哈尔滨市德强高中2021-2022学年高一上学期期中考试化学试题广东实验中学2020-2021学年高一上学期期中考试化学试题(已下线)期中测试卷03-【对点变式题】2021-2022学年高一化学上学期期中期末必考题精准练(人教版2019)(已下线)易错专题14 侯氏制碱法生产纯碱-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)
8 . 苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线如下:

制备苯乙酸的装置示意图如图(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250mL三口瓶a中加入70mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是_____ 。
(2)将a中的溶液加热至100℃,缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。仪器c的名称是_____ ,其作用是_____ 。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是_____ 。下列仪器中可用于分离苯乙酸粗品的是_____ (填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是_____ ,最终得到44g纯品,则苯乙酸的产率是_____ 。
(4)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是_____ 。

制备苯乙酸的装置示意图如图(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250mL三口瓶a中加入70mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100℃,缓缓滴加40g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。仪器c的名称是
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是
(4)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
9 . 实验室将NH3通入AlCl3溶液中制备Al(OH)3,经过滤、洗涤、灼烧得Al2O3,下列图示装置和原理均能达到实验目的是( )
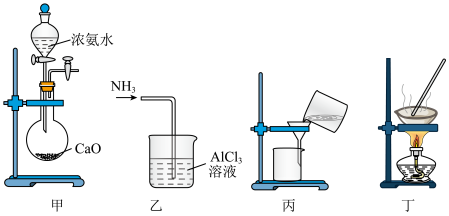

| A.用装置甲制取NH3 | B.用装置乙制备Al(OH)3 |
| C.用装置丙过滤并洗涤Al(OH)3 | D.用装置丁灼烧Al(OH)3得Al2O3 |
您最近一年使用:0次
2017-10-18更新
|
481次组卷
|
11卷引用:【全国百强校】黑龙江省大庆中学2019届高三下学期开学考试化学试题
【全国百强校】黑龙江省大庆中学2019届高三下学期开学考试化学试题江苏省宝应中学2018届高三上学期第一次月考化学试题湖南省师范大学附属中学2019届高三上学期月考(四)化学试题江苏省兴化一中2019届高三上学期12月月考化学试题湖南省永州市双牌县第二中学2019届高三上学期12月月考化学试题【全国百强校】江苏省南通市海安高级中学2019届高三上学期11月检测化学试题安徽省亳州市第二中学2020届高三上学期第三次月考化学试题江苏省扬州中学2020届高三12月月考化学试题山东省潍坊昌乐县第二中学2020届高三上学期期末化学模拟试题一(已下线)专题十 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)四川省江油中学2023-2024学年高三上期10月月考理综化学试题



