1 . 下列实验操作不正确的是
| A.提纯淀粉胶体中的NaCl:渗析 |
| B.除去NaCl溶液中的NaHCO3:加NaOH |
| C.分离CaCO3和NaCl混合物:溶解过滤 |
| D.用NaCl溶液制备NaCl固体:蒸发结晶 |
您最近一年使用:0次
2023-10-14更新
|
360次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一上学期10月月考化学试题
解题方法
2 . 早在战国时期,《周礼·考工记》就记载了我国劳动人民制取氢氧化钾以漂洗丝帛的工艺。大意是:先将干燥的木头烧成灰(含 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。

(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和________ 。
(2)反应过程中未涉及的基本反应类型是________ 。
(3)反应过程中能够循环利用的物质是________ (填化学式)。
(4)氢氧化钙与灰汁(含 )反应的化学方程式为
)反应的化学方程式为________ 。
(5)古人不提前制备大量氢氧化钾的原因是________ (用化学方程式表达)。
 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和
(2)反应过程中未涉及的基本反应类型是
(3)反应过程中能够循环利用的物质是
(4)氢氧化钙与灰汁(含
 )反应的化学方程式为
)反应的化学方程式为(5)古人不提前制备大量氢氧化钾的原因是
您最近一年使用:0次
解题方法
3 . 为达到实验目的,下列实验设计或操作不可行的是
| 选项 | 实验目的 | 实验设计或操作 |
| A | 鉴别软水和硬水 | 加入肥皂水,振荡 |
| B | 除去铜粉中少量的铁粉 | 加过量稀盐酸,充分反应后过滤、洗涤 |
| C | 分离 和 和 的固体混合物 的固体混合物 | 加水溶解、过滤、洗涤、蒸发 |
| D | 检验 溶液中是否混有 溶液中是否混有 | 取少量溶液于试管中,滴入酚酞溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 .  是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿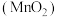 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
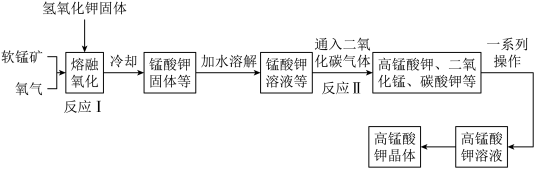
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为_______ 。
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
(3)若要除去 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作_______ (填操作名称)。
(4)由 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、_______ 、过滤、洗涤、干燥(填操作名称)。
(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成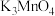 ,反应方程式为
,反应方程式为_______ 。
第二步反应方程式为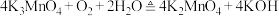
(6)写出反应Ⅱ的离子方程式_______ 。
(7)所得产品中只含有杂质 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为_______ %(保留两位小数)。
 是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿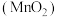 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.量筒 | D.酒精灯 |
 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作(4)由
 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成
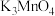 ,反应方程式为
,反应方程式为第二步反应方程式为
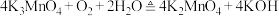
(6)写出反应Ⅱ的离子方程式
(7)所得产品中只含有杂质
 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
您最近一年使用:0次
名校
5 . 某固体混合物,可能含有CaO、 、
、 、
、 、NaCl中的几种,为检验其成分,做了如下实验:
、NaCl中的几种,为检验其成分,做了如下实验:
①取一定量固体溶于足量水,搅拌后得到无色透明溶液和白色沉淀,过滤得到滤液Ⅰ和沉淀Ⅰ,沉淀质量为10.00g。
②向滤液Ⅰ中加入过量的 溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
③向沉淀Ⅱ中加入过量的盐酸,仍有固体未溶解,过滤得到沉淀Ⅲ,沉淀质量为23.30g。
④向滤液Ⅱ中加入硝酸酸化后,再加入过量的 溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
已知:溶液中有 、
、 时,
时, 更容易和
更容易和 形成沉淀。
形成沉淀。
回答下列问题:
(1)通过实验①可知,一定不存在的是_______ (填化学式,下同)。
(2)沉淀Ⅰ、沉淀Ⅱ分别是_______ 、_______ 。
(3)本实验需要多次过滤,过滤需要用到得玻璃仪器有_______。
(4)写出实验④反应的离子方程式_______ 。
(5)该固体中一定含有_______ (填化学式),质量之比为_______ 。
 、
、 、
、 、NaCl中的几种,为检验其成分,做了如下实验:
、NaCl中的几种,为检验其成分,做了如下实验:①取一定量固体溶于足量水,搅拌后得到无色透明溶液和白色沉淀,过滤得到滤液Ⅰ和沉淀Ⅰ,沉淀质量为10.00g。
②向滤液Ⅰ中加入过量的
 溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。③向沉淀Ⅱ中加入过量的盐酸,仍有固体未溶解,过滤得到沉淀Ⅲ,沉淀质量为23.30g。
④向滤液Ⅱ中加入硝酸酸化后,再加入过量的
 溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。已知:溶液中有
 、
、 时,
时, 更容易和
更容易和 形成沉淀。
形成沉淀。回答下列问题:
(1)通过实验①可知,一定不存在的是
(2)沉淀Ⅰ、沉淀Ⅱ分别是
(3)本实验需要多次过滤,过滤需要用到得玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.漏斗 | D.酒精灯 |
(5)该固体中一定含有
您最近一年使用:0次
6 . 下列各组实验装置、所用试剂、实验现象及结论都正确的是
| A | B | C | D |
 | 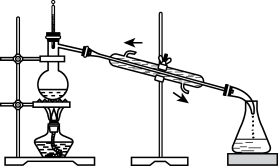 | 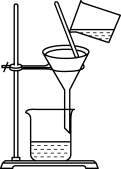 |  |
| 分离苯萃取碘水后已分层的有机层和水层 | 从三氯甲烷和四氯甲烷混合物中蒸馏出三氯甲烷 | 趁热过滤提纯苯甲酸 | 萃取时,将所需试剂加入分液漏斗,塞上玻璃塞,按如图所示方式用力振荡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-21更新
|
143次组卷
|
2卷引用:重庆市名校联盟2021-2022学年高二下学期第一次联合考试化学试题
解题方法
7 . 某工厂的废水中含有较多的 和
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
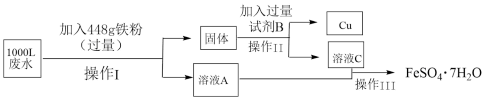
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为___________ 。
(2)操作Ⅰ和操作Ⅱ的名称是___________ ,所用到的玻璃仪器有___________ 。
(3)流程中“固体”的主要成分是___________ (填化学式);加入试剂B所发生反应的化学方程式为___________ 。
(4)操作Ⅲ包括蒸发浓缩、___________ 、过滤、___________ 、干燥。
(5)设计实验方案检验废水中是否含有 :
:___________ 。
(6)若废水中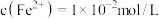 ,
,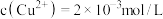 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是___________ g。
 和
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为
(2)操作Ⅰ和操作Ⅱ的名称是
(3)流程中“固体”的主要成分是
(4)操作Ⅲ包括蒸发浓缩、
(5)设计实验方案检验废水中是否含有
 :
:(6)若废水中
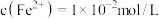 ,
,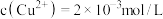 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是
您最近一年使用:0次
名校
解题方法
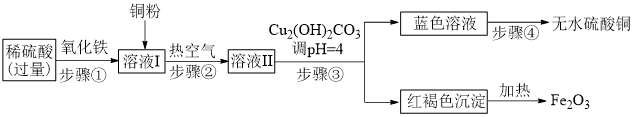
8 . 工业上以稀硫酸、氧化铁、铜粉为原料制备硫酸铜的流程如下:
已知:①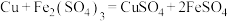 ;
;
②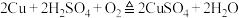 ;
;
③Fe2+易被氧化成Fe3+。
(1)步骤①发生的化学方程式是_______ 。
(2)溶液Ⅱ中溶质的成分是_______ (填化学式)。
(3)步骤③的名称是_______ ,用到的玻璃仪器有烧杯、_______ 、玻璃棒。
(4)上述流程中可以循环使用的物质是_______ (填名称)。

已知:①
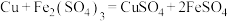 ;
;②
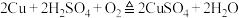 ;
;③Fe2+易被氧化成Fe3+。
(1)步骤①发生的化学方程式是
(2)溶液Ⅱ中溶质的成分是
(3)步骤③的名称是
(4)上述流程中可以循环使用的物质是
您最近一年使用:0次



