1 . 侯德榜是我国近代化学工业的奠基人之一,他将氨碱法和合成氨工艺联合起来,发明了“联合制碱法”。氨碱法中涉及的反应有:反应Ⅰ: ;反应Ⅱ:
;反应Ⅱ: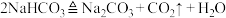 。下列装置不能达到相应实验目的的是
。下列装置不能达到相应实验目的的是
 ;反应Ⅱ:
;反应Ⅱ: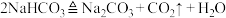 。下列装置不能达到相应实验目的的是
。下列装置不能达到相应实验目的的是| A | B | C | D |
 | 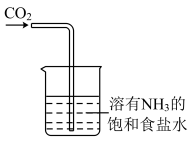 | 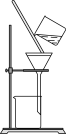 | 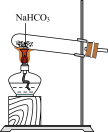 |
除去 中的 中的 | 制取 | 分离出 | 制取 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 重铬酸钾( )具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:
)具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:
(1) 中Cr的化合价为
中Cr的化合价为_______ 价,属于_______ (填“酸”、“碱”或“盐”)。
(2)当铬酸洗液变绿[溶液中 转化成
转化成 ]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入
]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入 ,粉末氧化、滤去
,粉末氧化、滤去 后可实现铬酸洗液的再生,其中加入
后可实现铬酸洗液的再生,其中加入 粉末氧化时发生反应的化学方程式为
粉末氧化时发生反应的化学方程式为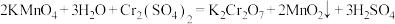 ,用单线桥法标明该反应的电子转移的方向和数目:
,用单线桥法标明该反应的电子转移的方向和数目:_______ ,滤去 时,可采用过滤操作,过滤需要用到的玻璃仪器有
时,可采用过滤操作,过滤需要用到的玻璃仪器有_______ 。
(3)当铬酸洗液变黑失效时,可在硫酸酸化条件下加入铁屑将残留的 转化成
转化成 ,铁屑自身转化成
,铁屑自身转化成 ,再用石灰石将铬元素转化成
,再用石灰石将铬元素转化成 ,沉淀,其中铁屑将
,沉淀,其中铁屑将 转化成
转化成 的化学方程式为
的化学方程式为_______ ;若黑色铬酸洗液中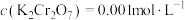 ,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为_______ g。
 )具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:
)具有强氧化性,在实验室和工业中都有很广泛的应用。其主要应用之一是配制铬酸洗液(重铬酸钾、水和浓硫酸按照一定比例配制成的溶液)。根据所学知识、回答下列问题:(1)
 中Cr的化合价为
中Cr的化合价为(2)当铬酸洗液变绿[溶液中
 转化成
转化成 ]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入
]失效时,将失效的铬酸洗液进行加热浓缩,冷却后加入 ,粉末氧化、滤去
,粉末氧化、滤去 后可实现铬酸洗液的再生,其中加入
后可实现铬酸洗液的再生,其中加入 粉末氧化时发生反应的化学方程式为
粉末氧化时发生反应的化学方程式为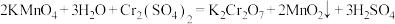 ,用单线桥法标明该反应的电子转移的方向和数目:
,用单线桥法标明该反应的电子转移的方向和数目: 时,可采用过滤操作,过滤需要用到的玻璃仪器有
时,可采用过滤操作,过滤需要用到的玻璃仪器有(3)当铬酸洗液变黑失效时,可在硫酸酸化条件下加入铁屑将残留的
 转化成
转化成 ,铁屑自身转化成
,铁屑自身转化成 ,再用石灰石将铬元素转化成
,再用石灰石将铬元素转化成 ,沉淀,其中铁屑将
,沉淀,其中铁屑将 转化成
转化成 的化学方程式为
的化学方程式为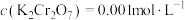 ,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
,则处理1L该黑色铬酸洗液时,所需的铁屑的质量为
您最近一年使用:0次
名校
解题方法
3 . 有一包固体,可能由硝酸铜、硫酸钾、氯化钠、碳酸钠中的一种或几种组成。为了探究该固体的组成,某化学小组设计并开展如图所示的实验:
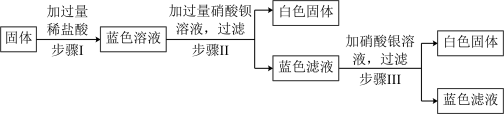
已知:①步骤I中的固体全部溶解,溶液呈蓝色,且无气泡或沉淀产生。
②步骤II、III中均可观察到有白色沉淀生成。
请回答下列问题:
(1)原固体中一定含有的物质是_______ (填化学式)。
(2)原固体中一定不含有的物质是_______ (填化学式)。
(3)写出步骤III中生成白色沉淀的离子方程式:_______ 。
(4)将步骤II中所得的白色固体经洗涤、干燥后,称量其质量为mg,则原样品中 的物质的量为
的物质的量为_______ mol。洗涤该白色固体的正确操作为:_______ 。

已知:①步骤I中的固体全部溶解,溶液呈蓝色,且无气泡或沉淀产生。
②步骤II、III中均可观察到有白色沉淀生成。
请回答下列问题:
(1)原固体中一定含有的物质是
(2)原固体中一定不含有的物质是
(3)写出步骤III中生成白色沉淀的离子方程式:
(4)将步骤II中所得的白色固体经洗涤、干燥后,称量其质量为mg,则原样品中
 的物质的量为
的物质的量为
您最近一年使用:0次
名校
解题方法
4 . 食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量 、
、 、
、 等杂质,实验室提供的试剂如下:饱和
等杂质,实验室提供的试剂如下:饱和 溶液、饱和
溶液、饱和 溶液、NaOH溶液、
溶液、NaOH溶液、 溶液。实验室提纯NaCl的流程如下图所示:
溶液。实验室提纯NaCl的流程如下图所示:

(1)欲除去溶液I中的杂质,写出A所代表的多种试剂,按滴加顺序依次为I.NaOH;II._______ ;III._______ (填化学式)
(2)请写出加入试剂I时发生反应的化学方程式:_______ 。
(3)操作a、b中均用到的玻璃仪器是_______ 、_______ (填仪器名称)。
(4)检验操作b所得到的沉淀已经洗净的操作和现象为_______ 。
(5)若上述流程中未进行操作b,即直接向溶液I中加盐酸到pH为4~5,过滤,得到沉淀X和溶液Y,则沉淀X为_______ (写化学式)。
(6)本实验中所用的盐酸是将标准状况下a L的HCl气体溶于0.1L水制得,已知该盐酸的密度为b ,则该盐酸的物质的量浓度为
,则该盐酸的物质的量浓度为_______ 。(用a和b表示)
 、
、 、
、 等杂质,实验室提供的试剂如下:饱和
等杂质,实验室提供的试剂如下:饱和 溶液、饱和
溶液、饱和 溶液、NaOH溶液、
溶液、NaOH溶液、 溶液。实验室提纯NaCl的流程如下图所示:
溶液。实验室提纯NaCl的流程如下图所示:
(1)欲除去溶液I中的杂质,写出A所代表的多种试剂,按滴加顺序依次为I.NaOH;II.
(2)请写出加入试剂I时发生反应的化学方程式:
(3)操作a、b中均用到的玻璃仪器是
(4)检验操作b所得到的沉淀已经洗净的操作和现象为
(5)若上述流程中未进行操作b,即直接向溶液I中加盐酸到pH为4~5,过滤,得到沉淀X和溶液Y,则沉淀X为
(6)本实验中所用的盐酸是将标准状况下a L的HCl气体溶于0.1L水制得,已知该盐酸的密度为b
 ,则该盐酸的物质的量浓度为
,则该盐酸的物质的量浓度为
您最近一年使用:0次
5 . 下列有关实验操作、原理和装置不能达到实验目的的是
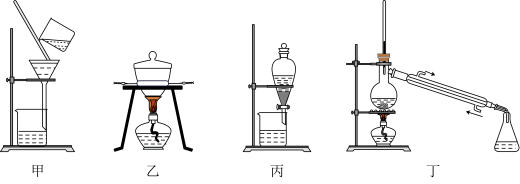
| A.用装置甲除去食盐水中的泥沙 | B.用装置乙灼烧海带 |
| C.用装置丙分离酒精和水的混合物 | D.用装置丁制取少量蒸馏水 |
您最近一年使用:0次
2022-11-10更新
|
318次组卷
|
8卷引用:江苏省苏州市2022-2023学年高一上学期期中调研化学试题
江苏省苏州市2022-2023学年高一上学期期中调研化学试题福建省福州四中2022-2023学年高一上学期第一学段检测(非美术班)化学试题江苏省常熟中学2022-2023学年高一下学期学业质量阳光指标调研化学试题江苏省昆山中学2023-2024学年高一上学期10月月考化学试题江苏省苏州中学2023-2024学年高一上学期10月月考化学试题江苏省昆山市陆家高级中学、花桥康桥学校2023-2024学年高一上学期10月阶段性测试化学试题江苏省苏州田家炳实验高级中学2023-2024学年高一上学期10月月考化学试题江苏省盐城市响水县清源高级中学2023-2024学年高一上学期第一次学情分析考试化学试卷
6 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)
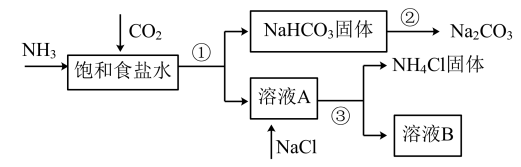
(1)①②③所涉及的操作方法中,包含过滤的是_______ (填序号)。
(2)根据如图,写出①中发生反应的化学方程式_______ 。

(1)①②③所涉及的操作方法中,包含过滤的是
(2)根据如图,写出①中发生反应的化学方程式
您最近一年使用:0次
7 . 选取下列实验方法分离物质,将分离方法的字母填在横线上:
A.萃取、分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法
(1)_______ 分离饱和食盐水与泥沙的混合物。
(2)_______ 分离水和汽油的混合物。
(3)_______ 分离四氯化碳(沸点为 )和甲苯(沸点为
)和甲苯(沸点为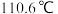 )的混合物。
)的混合物。
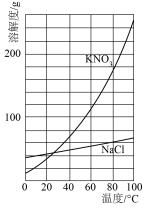
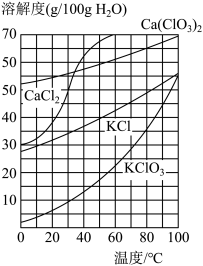
(4)_______ 从含硝酸钾和氯化钠的混合液中分离出硝酸钾。(溶解度规律如图)
A.萃取、分液法 B.结晶法 C.分液法 D.蒸馏法 E.过滤法
(1)
(2)
(3)
 )和甲苯(沸点为
)和甲苯(沸点为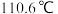 )的混合物。
)的混合物。(4)

您最近一年使用:0次
名校
解题方法
8 . “食盐的精制”实验中,离子分离或除杂的基本思路如图,下列说法错误的是
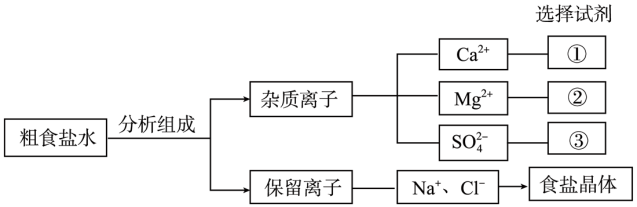

| A.①②③分别为Na2CO3溶液、NaOH溶液、BaCl2溶液 |
| B.试剂的加入顺序是①②③,逐一过滤后,滤液再加适量盐酸至中性 |
| C.整个流程实验操作中玻璃棒既有引流,又有搅拌作用 |
| D.向上层清液中继续滴加试剂②,无沉淀生成,则Mg2+沉淀完全 |
您最近一年使用:0次
9 . 下列分离方法中,和物质的溶解度无关的是
| A.升华 | B.萃取 | C.过滤 | D.结晶 |
您最近一年使用:0次
10 . 以工业废渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:

(1)氯化过程中控制废渣过量、在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①若某学生在上述流程中发现某含钙离子盐的化学式为CaO3Cl2,试根据盐的定义写出这种盐组成的表达式_______ 。
②刚开始生成Ca(ClO)2的化学方程式为_______ 。
③提高Cl2转化为Ca(ClO)2的转化率的可行措施有_______ (填序号)。
a.适当减缓通入Cl2的速率 b.充分搅拌浆料 c.加水使Ca(OH)2完全溶解
(2)氯化完成后过滤。
①滤渣的主要成分为_______ (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2]与n[CaCl2]_______ 1∶5(填“>”“<”或“=”)。
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3。你认为可能的原因是_______ 。写出可能发生的化学方程式_______ 。

(1)氯化过程中控制废渣过量、在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①若某学生在上述流程中发现某含钙离子盐的化学式为CaO3Cl2,试根据盐的定义写出这种盐组成的表达式
②刚开始生成Ca(ClO)2的化学方程式为
③提高Cl2转化为Ca(ClO)2的转化率的可行措施有
a.适当减缓通入Cl2的速率 b.充分搅拌浆料 c.加水使Ca(OH)2完全溶解
(2)氯化完成后过滤。
①滤渣的主要成分为
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2]与n[CaCl2]
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3。你认为可能的原因是

您最近一年使用:0次



