名校
解题方法
1 . 某无色溶液中可能含有以下离子中的一种或几种:Na+、Ag+、Fe3+、NH 、Al3+、CO
、Al3+、CO 、AlO
、AlO 、S2O
、S2O 、SO
、SO 。现取该溶液进行有关实验,实验结果如图所示:
。现取该溶液进行有关实验,实验结果如图所示:
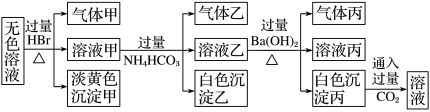
下列说法不正确的是
 、Al3+、CO
、Al3+、CO 、AlO
、AlO 、S2O
、S2O 、SO
、SO 。现取该溶液进行有关实验,实验结果如图所示:
。现取该溶液进行有关实验,实验结果如图所示:
下列说法不正确的是
| A.淡黄色沉淀甲不可能为AgBr |
| B.气体甲可能是混合气体 |
C.综合上述信息可以确定肯定存在的离子有:Na+、AlO 、S2O 、S2O |
D.由溶液甲生成气体乙的途径只有:Al3++3HCO =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
您最近一年使用:0次
解题方法
2 . 某混合物的无色溶液中,可能含有以下离子中的若干种:K+、Ca2+、Fe3+、NH 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO )=
)=___________ mol·L−1;
(2)某同学认为该溶液中一定存在K+,浓度是___________ ;
(3)根据以上实验,氯离子可能存在。检验该离子是否存在的方法是:___________ ;
(4)写出③中固体加入足量盐酸洗涤的离子方程式为___________ 。
 、Cl-、CO
、Cl-、CO 和SO
和SO 。现每次取10.00mL进行实验:
。现每次取10.00mL进行实验:①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO
 )=
)=(2)某同学认为该溶液中一定存在K+,浓度是
(3)根据以上实验,氯离子可能存在。检验该离子是否存在的方法是:
(4)写出③中固体加入足量盐酸洗涤的离子方程式为
您最近一年使用:0次
解题方法
3 . 某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子有_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ ,有关的离子方程式为_______ 。
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明液中肯定有_______ , 有关的离子方程式为_______ 。
(4)原溶液可能大量存在的阴离子是下列的_______ 。
A.Cl- B. C.
C.
(1)不做任何实验就可以肯定原溶液中不存在的离子有
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明液中肯定有
(4)原溶液可能大量存在的阴离子是下列的
A.Cl- B.
 C.
C.
您最近一年使用:0次
2022-09-17更新
|
477次组卷
|
4卷引用:广西壮族自治区玉林市五校2022-2023学年高二下学期5月联考化学试题
4 . 某学习小组拟研究FeSO4的分解实验探究,请你利用所学知识帮该小组完成以下实验方案。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
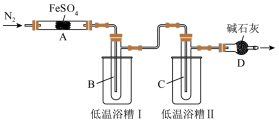
回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是_______ 。
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是_______ ,(只填操作),当A处固体完全分解后通入N2的目的是_______ 。
(3)低温浴槽I收集的物质是_______ (填化学式),低温浴槽II控制的温度范围为_______ 。
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
甲组实验中A装置得到固体产物是_______ (填化学式)。
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是_______ 。
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案_______ (填“1”或“2”)可行。
[实验目的]探究FeSO4分解产物与温度关系。
[提出假设]
假设1:Fe2O3、SO3、SO2;假设2:FeO、SO3、SO2;假设3:Fe3O4、SO3、SO2。
[查阅资料]几种物质的物理性质如表所示。
| 物质 | SO3 | SO2 | O2 | N2 |
| 熔点/℃ | 16.8 | -72.4 | -218.4 | -209.9 |
| 沸点/℃ | 44.8 | -10 | -182.9 | -195.8 |

回答下列问题:
(1)根据所学知识判断,假设2肯定不成立,理由是
(2)实验过程中,在检查装置气密性之后点燃A处酒精灯之前的操作是
(3)低温浴槽I收集的物质是
(4)甲、乙组分别进行实验,实验数据如下(不考虑损失,固体已完全分解且固体产物为纯净物):
| 实验 | A处温度/℃ | FeSO4质量/g | 低温浴槽I净增质量/g | 低温浴槽II净增质量/g |
| 甲 | T1 | 3.04 | 0.80 | 0.64 |
| 乙 | T2 | 4.56 | 1.60 | 0.64 |
(5)为进一步确认固体产物成分,取乙组实验得到的固体溶于稀硫酸,将溶液分成两份,进行如下实验:在一份溶液中滴加铁氰化钾K3[Fe(CN)6]溶液,产生蓝色沉淀。在另一份溶液中滴加NH4SCN溶液,观察到的现象是
[实验结论]通过上述实验,FeSO4分解产物与温度有关。
[交流反思]FeSO4分解反应中是否有O2生成?
(6)为验证实验猜想,他们设计两种方案检验O2:
方案1:将D管导出的气体通入酸化的淀粉-KI溶液中。
方案2:用带火星的木条放在D管口处。
假设过程中持续缓缓通入N2,对比以上两种方案,其中方案
您最近一年使用:0次
5 . 向稀硝酸酸化的某溶液中滴加氯化钠溶液,产生白色沉淀,证明原溶液中一定含有
| A.Ba | B. | C.Ag+ | D. |
您最近一年使用:0次
2022高三·全国·专题练习
6 . 下列实验能达到目的的是
| 实验目的 | 实验方法或操作 | |
| A | 测定中和反应的反应热 | 酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温度 |
| B | 探究浓度对化学反应速率的影响 | 量取同体积不同浓度的 溶液,分别加入等体积等浓度的 溶液,分别加入等体积等浓度的 溶液,对比现象 溶液,对比现象 |
| C | 判断反应后 是否沉淀完全 是否沉淀完全 | 将 溶液与 溶液与 溶液混合,反应后静置,向上层清液中再加1滴 溶液混合,反应后静置,向上层清液中再加1滴 溶液 溶液 |
| D | 检验淀粉是否发生了水解 | 向淀粉水解液中加入碘水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-06更新
|
13059次组卷
|
32卷引用:【知识图鉴】单元讲练测选择性必修3第4单元02基础练
(已下线)【知识图鉴】单元讲练测选择性必修3第4单元02基础练江西省宜春市铜鼓中学2022-2023学年高二下学期第一次段考化学试题(已下线)第09练 微型实验设计与评价 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)实验02 定性与定量研究影响化学反应速率的因素-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)实验01 中和反应反应热的测定-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)吉林省长春市第二实验中学2023-2024学年高二下学期开学考试化学试题(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编(已下线)2022年辽宁省高考真题化学试题(部分试题)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)2022年辽宁高考真题化学试题(已下线)2022年辽宁省高考真题变式题(11-15)(已下线)第28讲 定性、定量实验(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题43 常见物质的分离、提纯和鉴别-备战2023年高考化学考点微专题(全国版)福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题吉林省延边第二中学2022-2023学年高三上学期第三次阶段测试化学试题(已下线)专题11 化学实验基础(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价(已下线)专题05 突破化学实验基础(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)回归教材重难点10 再现常考化学实验基础知识-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)2022年辽宁高考真题化学试题变式题(选择题11-15)(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题11 化学实验(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)四川省内江市第六中学2023-2024学年高三上学期入学考试化学试题黑龙江省大庆市肇州县第二中学2023-2024学年高三上学期11月月考化学试题(已下线)题型07 化学实验基础(选择题)-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)北京市第一○一中学2023-2024学年高三下学期统练二化学试题
名校
解题方法
7 . 化合物X由3种元素组成。某兴趣小组按如下流程进行实验:

已知:A由两种气体组成,且两种气体组成元素相同。请回答下列问题:
(1)X的组成元素有___________ ;X的化学式为___________ 。
(2)固体B的成分是___________ (用化学式表示)
(3)X化学性质相当活泼,1mol X吸收 只生成一种二元弱酸Y和1mol气体C,请写出Y与足量NaOH溶液反应的离子方程式
只生成一种二元弱酸Y和1mol气体C,请写出Y与足量NaOH溶液反应的离子方程式___________ 。
(4)设计实验证明溶液G中的阳离子___________ 。

已知:A由两种气体组成,且两种气体组成元素相同。请回答下列问题:
(1)X的组成元素有
(2)固体B的成分是
(3)X化学性质相当活泼,1mol X吸收
 只生成一种二元弱酸Y和1mol气体C,请写出Y与足量NaOH溶液反应的离子方程式
只生成一种二元弱酸Y和1mol气体C,请写出Y与足量NaOH溶液反应的离子方程式(4)设计实验证明溶液G中的阳离子
您最近一年使用:0次
2022-06-26更新
|
635次组卷
|
6卷引用:浙江省温州浙南名校联盟2021-2022学年高二下学期期末联考化学试题
浙江省温州浙南名校联盟2021-2022学年高二下学期期末联考化学试题 浙江省宁波市余姚中学2022-2023学年高二下学期3月月考化学试题 浙江省杭州市临平区杭州二中树兰高级中学2022-2023学年高二下学期第一次调研化学试题 浙江省舟山市普陀中学2023届高三返校考试化学试题(已下线)2023年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷C(已下线)2019年高考浙江卷化学试题变式题(物质组成的测定)
名校
解题方法
8 . 棉隆用于防治棉花、花生、大豆、茶叶等枯、黄萎病,对土壤真菌、线虫、昆虫及杂草也有毒杀作用,其结构简式如图所示,其中W、X、Y、Z为短周期元素,原子序数依次增大,其中X、Y为同周期元素。下列结论错误的是
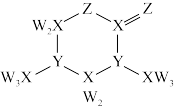

| A.棉隆的结构中除W外所有原子都满足8电子结构 |
B.X、Y、Z三种元素形成的一种阴离子能检验 |
C.原子半径大小顺序为 |
| D.X、Y、Z三种元素的氧化物的水化物有可能均为弱酸 |
您最近一年使用:0次
2022-05-29更新
|
134次组卷
|
3卷引用:河南省部分学校2021-2022学年高二下学期5月联考化学试题
9 . 下列实验“操作和现象”与“结论”对应关系正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入氯化钡溶液,生成白色沉淀 | 该溶液中一定有SO |
| B | 向某溶液中同时加入几滴KSCN溶液和少量新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 该溶液中一定无K+ |
| D | 向某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液中一定含有NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-16更新
|
129次组卷
|
3卷引用:安徽工业大学附属中学2020-2021学年高二上学期文理分科考试化学试题
名校
10 . 某钠盐溶液中可能含有SO 、SO
、SO 、NO
、NO 、NO
、NO 、CO
、CO 、Cl-、I-等阴离子。现取2份此溶液样品,分别进行如下实验:
、Cl-、I-等阴离子。现取2份此溶液样品,分别进行如下实验:
①加入足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且有气体生成;
②加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体。
根据上述实验现象,以下说法正确的是
 、SO
、SO 、NO
、NO 、NO
、NO 、CO
、CO 、Cl-、I-等阴离子。现取2份此溶液样品,分别进行如下实验:
、Cl-、I-等阴离子。现取2份此溶液样品,分别进行如下实验:①加入足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且有气体生成;
②加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体。
根据上述实验现象,以下说法正确的是
A.原溶液中CO 与SO 与SO 至少存在一种离子 至少存在一种离子 |
B.原溶液中一定存在NO 、CO 、CO ,可能存在NO ,可能存在NO 、Cl- 、Cl- |
C.原溶液中一定存在NO 、CO 、CO 、Cl-三种离子 、Cl-三种离子 |
D.原溶液中一定不存在SO 、I-,无法判断是否存在SO 、I-,无法判断是否存在SO |
您最近一年使用:0次
2022-03-03更新
|
504次组卷
|
3卷引用:浙江省杭嘉湖金四县区教研联盟2020-2021学年高二下学期6月调研测试化学试题



