1 . 已知 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: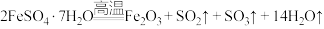 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: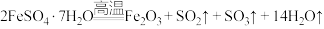 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
| A.仪器的连接顺序为a、f(或g)、g(或f)、h、i、d、e、b |
B.装置C中的X溶液为 溶液 溶液 |
| C.装置B的作用为处理尾气 |
D.反应中每生成 ,转移2mol电子 ,转移2mol电子 |
您最近一年使用:0次
名校
解题方法
2 . 区分下列物质的方法不正确的是
| 选项 | 物质 | 方法 |
| A | 金刚石和石墨 | 比较硬度 |
| B | 一氧化碳和甲烷 | 观察颜色 |
| C | 氧气和氮气 | 用带火星的木条检验 |
| D | 氢氧化钠和硝酸铵 | 溶于水测温度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列有关常见气体成分检验的结论正确的是
| 选项 | 仪器或试剂 | 实验现象 | 结论 |
| A | 湿润的红色石蕊试纸 | 试纸变蓝 | 一定含 |
| B | 灼热CuO | 黑色固体变为红色 | 一定含 |
| C | 澄清石灰水 | 溶液中出现浑浊 | 一定含 |
| D | 湿润的淀粉-KI试纸 | 试纸变蓝 | 一定含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-05更新
|
151次组卷
|
2卷引用:2022年夏季山东普通高中学业水平考试化学试题
解题方法
4 . 化合物X由四种元素组成,按如下流程进行实验。混合气体A由气体E和元素种类相同的另两种气体组成,且气体C的平均相对分子质量为8.5。混合物B中有两种固体。
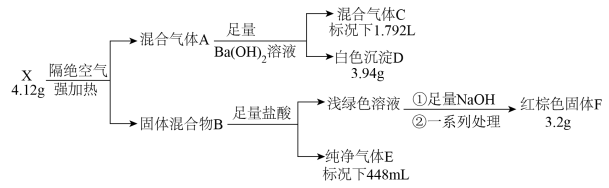
请回答:
(1)组成X的四种元素为_______ ;X的化学式为_______ 。
(2)写出由X到A的化学方程式_______ 。
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因_______ 。
(4)设计实验检验混合气体A中相对分子量较小的两种气体_______ 。

请回答:
(1)组成X的四种元素为
(2)写出由X到A的化学方程式
(3)用盐酸溶解固体F,滴加一定量KSCN溶液,得到血红色溶液Y。往溶液Y中加入一定量KCl固体,溶液Y颜色变淡,请结合离子方程式说明原因
(4)设计实验检验混合气体A中相对分子量较小的两种气体
您最近一年使用:0次
5 . 为探究某液态化合物X(仅含三种短周期元素)的组成和性质,某学习小组进行了如图实验:
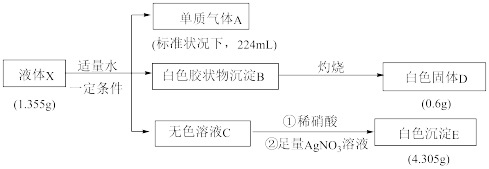
已知:白色固体D是光导纤维的主要成分。请回答:
(1)组成X的三种元素的名称是______ 。
(2)由白色固体D制备的光导纤维作通讯材料时,遇强碱性溶液易造成断路,请用离子方程式解释其原因______ 。
(3)写出液体X与适量水在一定条件下反应的化学方程式______ 。
(4)设计实验检验单质气体A______ 。

已知:白色固体D是光导纤维的主要成分。请回答:
(1)组成X的三种元素的名称是
(2)由白色固体D制备的光导纤维作通讯材料时,遇强碱性溶液易造成断路,请用离子方程式解释其原因
(3)写出液体X与适量水在一定条件下反应的化学方程式
(4)设计实验检验单质气体A
您最近一年使用:0次
6 . 利用如图所示装置制备NH3并对其性质进行检验,关闭K4、K2,打开K1、K3,使浓氨水和NaOH接触可生成NH3,待A中圆底烧瓶充满NH3时,关闭K1、K3,打开K4,下列说法错误的是
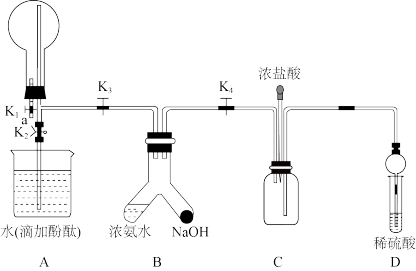

| A.可在a导管口处用干燥的蓝色石蕊试纸检验圆底烧瓶中是否充满NH3 |
| B.关闭K2,热敷圆底烧瓶可引发喷泉 |
| C.稍后挤压装浓盐酸滴管的胶头可在C中观察到白烟 |
| D.D中稀硫酸的作用为尾气吸收,其中干燥管能防止倒吸 |
您最近一年使用:0次
名校
解题方法
7 . 摩尔盐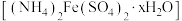 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是___________ 。
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有___________ 。取样品 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为___________ (用含a、b的代数式表示)。
(3)利用摩尔盐分解产生的 ,可制取氯化亚砜
,可制取氯化亚砜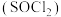 :
: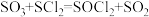 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
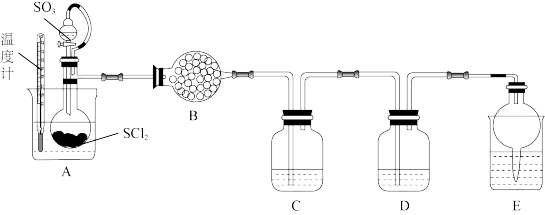
①装置B为无水 ,其作用是
,其作用是___________ 。
②装置C和装置D中的试剂分别是___________ 、___________ (填小写字母)。
a. 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液
(4)利用摩尔盐分解产生的 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
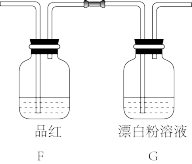
①将少量 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是___________ (用化学反应方程式表示)。
②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是___________ ,其作用是___________ ,通过___________ (填现象)即可证明亚硫酸的酸性强于次氯酸。
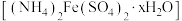 比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:
比一般的亚铁盐更稳定,是一种重要的定量分析化学试剂。回答下列问题:(1)制备摩尔盐采用的方法是先在封闭体系中利用铁和稀硫酸反应制备硫酸亚铁溶液,再用新制的硫酸亚铁溶液和硫酸按饱和溶液反应制得。配制硫酸按饱和溶液的蒸馏水,需经煮沸并迅速冷却后再使用,目的是
(2)可以采用热重分析法测定摩尔盐样品中所含结晶水的个数,加热其晶体需要使用的实验仪器除了玻璃棒、三脚架、泥三角、酒精灯外,还需要的仪器有
 加热至两次质量恒重为
加热至两次质量恒重为 (假设减少的质量仅仅是晶体失水),则x的表达式为
(假设减少的质量仅仅是晶体失水),则x的表达式为(3)利用摩尔盐分解产生的
 ,可制取氯化亚砜
,可制取氯化亚砜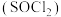 :
: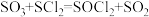 。已知
。已知 是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取
是一种液态化合物,遇水产生白雾和一种刺激性气体。利用如图装置制取 并检验生成的
并检验生成的 。
。
①装置B为无水
 ,其作用是
,其作用是②装置C和装置D中的试剂分别是
a.
 溶液 b.
溶液 b. 和
和 溶液 c.
溶液 c. 溶液 d.饱和的
溶液 d.饱和的 溶液
溶液(4)利用摩尔盐分解产生的
 ,设计实验探究亚硫酸与次氯酸的酸性强弱。
,设计实验探究亚硫酸与次氯酸的酸性强弱。
①将少量
 气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
气体直接通入装置G中,不能根据装置G中现象判断亚硫酸与次氯酸的酸性强弱,理由是②为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置F中另一种试剂是
您最近一年使用:0次
2022-07-15更新
|
303次组卷
|
2卷引用:河南省开封市五县2021-2022学年高二下学期期末考试化学试题
8 . 某兴趣小组在实验室用如图装置制备乙烯,并检验气体产物组分含有乙烯和二氧化硫。下图装置中的药品使用错误的是
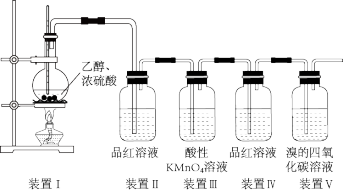

| A.装置Ⅰ | B.装置Ⅱ | C.装置Ⅲ | D.装置Ⅴ |
您最近一年使用:0次
解题方法
9 . 某化学小组制备 并验证
并验证 的部分性质,装置如图所示(部分夹持装置省略):
的部分性质,装置如图所示(部分夹持装置省略):

(1)仪器a的名称是___________ 。
(2)装置A制取 的反应中,利用了浓硫酸的
的反应中,利用了浓硫酸的___________ 性,___________ (填“能”或“不能”)用浓硝酸代替。
(3)在滴加浓硫酸之前,需先通入一段时间的 ,此操作的目的是
,此操作的目的是___________ 。
(4)装置B中的反应生成乳白色浑浊的同时生成了一种强碱,则该反应的化学方程式为___________ 。
(5)装置D验证了 的漂白性,为了进一步探究
的漂白性,为了进一步探究 与品红作用的可逆性,请写出有关实验操作及现象:
与品红作用的可逆性,请写出有关实验操作及现象:___________ 。
(6)为测定装置E中收集到的混合气体中二氧化硫的含量,进行如下操作:

当注入标准状况下10mL混合气体时,酸性 ,溶液恰好褪色,假设混合气体中
,溶液恰好褪色,假设混合气体中 能被
能被 溶液充分吸收。已知:
溶液充分吸收。已知: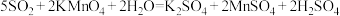 。该混合气体中二氧化硫的体积分数为
。该混合气体中二氧化硫的体积分数为___________ 。
 并验证
并验证 的部分性质,装置如图所示(部分夹持装置省略):
的部分性质,装置如图所示(部分夹持装置省略):
(1)仪器a的名称是
(2)装置A制取
 的反应中,利用了浓硫酸的
的反应中,利用了浓硫酸的(3)在滴加浓硫酸之前,需先通入一段时间的
 ,此操作的目的是
,此操作的目的是(4)装置B中的反应生成乳白色浑浊的同时生成了一种强碱,则该反应的化学方程式为
(5)装置D验证了
 的漂白性,为了进一步探究
的漂白性,为了进一步探究 与品红作用的可逆性,请写出有关实验操作及现象:
与品红作用的可逆性,请写出有关实验操作及现象:(6)为测定装置E中收集到的混合气体中二氧化硫的含量,进行如下操作:

当注入标准状况下10mL混合气体时,酸性
 ,溶液恰好褪色,假设混合气体中
,溶液恰好褪色,假设混合气体中 能被
能被 溶液充分吸收。已知:
溶液充分吸收。已知: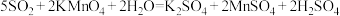 。该混合气体中二氧化硫的体积分数为
。该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
2022-07-04更新
|
280次组卷
|
2卷引用:河南省平顶山市2021-2022学年高一下学期期末调研化学试题
解题方法
10 . 将不同质量的 与
与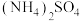 (物质的量之比均为2:1)混合样品分别加入
(物质的量之比均为2:1)混合样品分别加入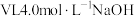 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:
下列说法错误的是
 与
与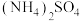 (物质的量之比均为2:1)混合样品分别加入
(物质的量之比均为2:1)混合样品分别加入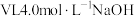 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:
溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量,部分测定结果如下:| 序号 | ① | ② |
| 铵盐的质量/g | 9.05 | 18.10 |
| 浓硫酸增加的质量/g | m | m |
| A.加热逸出的气体能使湿润的红色石蕊试纸变蓝 |
B.①中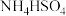 与NaOH溶液反应的离子方程式为 与NaOH溶液反应的离子方程式为 |
C.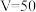 |
| D.当铵盐的质量为36.2g时,恰好与碱反应无气体产生 |
您最近一年使用:0次



