1 . 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:

(1)I、II、III、IV装置可盛放的试剂是:I___________ ;II___________ ;III___________ ;IV___________ (将下列有关试剂的序号填入空格内)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是___________ 。
(3)使用装置II的目的是___________ 。
(4)使用装置III的目的是___________ 。
(5)确定含有乙烯的现象是___________ 。

(1)I、II、III、IV装置可盛放的试剂是:I
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
(3)使用装置II的目的是
(4)使用装置III的目的是
(5)确定含有乙烯的现象是
您最近一年使用:0次
2023-06-29更新
|
60次组卷
|
18卷引用:吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题
吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题(已下线)2012年人教版高中化学选修5 2.1脂肪烃练习卷高二人教版选修5 第三章 烃的含氧衍生物 第一节 醇酚黑龙江省大兴安岭地区漠河县第一中学2018-2019学年高二上学期第一次月考化学试题福建省莆田第七中学2020-2021学年高二上学期第一次月考化学试题上海市奉城高级中学2018-2019学年高二上学期期末考试化学试题安徽省安庆桐城市第八中学2020-2021学年高二上学期第一次段考化学试题黑龙江省双鸭山市第一中学2020-2021学年高二下学期4月月考化学试题陕西省西安市蓝田县大学区联考2022-2023学年高二下学期6月期末考试化学试题2.1.1有机化学反应的主要类型(课前)-鲁科版选择性必修3陕西省西安市蓝田县大学区联考2022-2023学年高二下学期4月期中考试化学试题(已下线)2014年高一化学人教版必修2 3.2.1乙烯练习卷内蒙古北京八中乌兰察布分校2016-2017学年高一下学期第二次调考化学试题云南省绥江县一中2018-2019学年高一下学期期末考试化学试题课时1 石油的炼制 乙烯——A学习区 夯实基础(鲁科版必修2)课时1 甲烷 石油的炼制与乙烯——A学习区 夯实基础(鲁科版(2019)第二册)山东省德州市齐河县实验中学2019-2020学年高一下学期期中考试化学试题云南省元阳县一中2020-2021学年高一下学期6月份考试化学试题
名校
解题方法
2 .  的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:

已知 与
与 、
、 在溶液中存在以下平衡:
在溶液中存在以下平衡: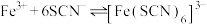 (红色);
(红色);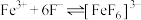 (无色)。
(无色)。
下列说法不正确的是
 的配位化合物较稳定且运用广泛。它可与
的配位化合物较稳定且运用广泛。它可与 、
、 、
、 、
、 等形成配离子使溶液显色。如:显浅紫色的
等形成配离子使溶液显色。如:显浅紫色的 、红色的
、红色的 、黄色的
、黄色的 、无色的
、无色的 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:
已知
 与
与 、
、 在溶液中存在以下平衡:
在溶液中存在以下平衡: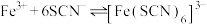 (红色);
(红色);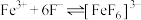 (无色)。
(无色)。下列说法不正确的是
A.Ⅰ中溶液呈黄色可能是由 水解产物的颜色引起的 水解产物的颜色引起的 |
B. 与 与 的配位能力强于 的配位能力强于 |
C.为了能观察到溶液Ⅰ中 的颜色,可向该溶液中加入稀盐酸 的颜色,可向该溶液中加入稀盐酸 |
| D.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色 |
您最近一年使用:0次
2023-03-25更新
|
590次组卷
|
8卷引用:吉林省长春外国语学校2022-2023学年高二下学期3月月考化学试题
名校
解题方法
3 . 某兴趣小组为了探究SO2气体还原Fe3+的反应,他们使用的药品和装置如下图所示,下列说法不合理的是
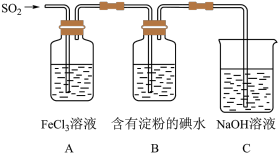
| A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色 |
| B.装置C的作用是吸收SO2尾气,防止污染空气 |
| C.为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫色褪去 |
| D.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀 |
您最近一年使用:0次
2023-02-21更新
|
923次组卷
|
55卷引用:2015-2016学年吉林省松原市油田高中高二下期末化学试卷
2015-2016学年吉林省松原市油田高中高二下期末化学试卷云南省西畴县二中2019-2020学年高二上学期开学考试化学试题湖南省常德市安乡县第一中学2021-2022 学年高二下学期期中考试化学试题上海交通大学附属中学2022-2023学年高二上学期开学摸底考试化学试题(已下线)2014年高考化学鲁科版3.3硫的转化练习卷2015-2016学年黑龙江省大庆铁人中学高一上期末化学试卷2015-2016学年河北石家庄一中高一下学情反馈一化学卷2017届广东省中山一中高三上学期第一次统测化学试卷2017届黑龙江省牡丹江高级中学高三10月月考化学卷2017届河北省衡水中学高三上期中化学卷2017届山东省莱芜一中高三上学期10月月考化学试卷2017届河南省南阳一中高三上第三次周考化学卷福建省泰宁第一中学2018届高三上学期第一阶段考试化学试题宁夏石嘴山市第三中学2018届高三上学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【押题专练】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期期中考试化学试题山东省东营市第二中学2019届高三上学期模块考试(期中)化学试题贵州省剑河县第二中学2018-2019学年高一上学期12月份考试化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一上学期期末考试化学试题甘肃省甘谷第一中学2020届高三上学期第一次检测化学试题安徽省滁州市定远县重点中学2018-2019学年高一上学期期末考试化学试题苏教版高中化学必修1专题4《硫 氮可持续发展》测试卷云南省丽江市宁蒗县第一中学2019—2020学年高一上学期期末考试化学试题云南省曲靖市罗平县第三中学2019-2020学年高一上学期期末考试化学试题云南省曲靖市沾益县炎方一中2019-2020学年高一上学期期末考试化学试题河南省商丘市第一高级中学2020届高三上学期期中考试化学试题河南省开封市第二十五中2019-2020高一下学期初分科考试化学试卷(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测河北省衡水市桃城区第十四中学2019-2020学年高一下学期第五次综合测试化学试题(已下线)第四单元 非金属及其化合物测试题-2021年高考化学一轮复习名师精讲练(已下线)第15讲 硫及其化合物(精练)-2021年高考化学一轮复习讲练测福建省福州市闽江口联盟校2021届高三上学期期中联考化学试题(已下线)练习9 硫和二氧化硫-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)浙江省温州市瑞安市上海新纪元高级中学2021-2022学年高一9月份月考(5-6班)化学试题(已下线)4.2.1 含硫物质之间的转化(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)河南省林州市第一中学2021-2022学年高一下学期开学检测化学试题课后-5.1.3 不同价态含硫物质的转化-人教2019必修第二册广东省佛山市第一中学2021-2022学年高一下学期第一次段考(3月)化学试题湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期期中考试化学试题湖北省公安县第三中学2021-2022学年高三上学期8月质量检测化学试题安徽省宿州市第二中学2022-2023学年高一上学期第一次月考化学试题安徽省阜阳市第一中学2022-2023学年高一下学期第一次月考化学试题安徽省安庆市第一中学2022-2023学年高一下学期第一次月考化学试题安徽省亳州市第一中学2022-2023学年高一下学期第一次月考化学试题河南省郑州外国语学校2022-2023学年高一下学期第一次月考化学试题安徽省阜阳市太和中学2022-2023学年高一下学期第一次质量检测化学试题四川省广安市育才学校2022-2023学年高一下学期3月月考化学试题广东省广州市培英中学2022-2023学年高一下学期期中考试化学试题湖南省衡阳县第四中学2022-2023学年高一下学期第一次(3月)月考化学试题湖南省株洲市炎陵县2022-2023学年高一下学期3月月考化学试题安徽省淮北市树人高级中学2023-2024学年高一下学期开学考试化学试题北京师范大学第二附属中学2023-2024学年高一下学期3月化学测试题安徽省芜湖市第一中学2022-2023学年高一下学期3月份教学质量诊断测试化学试卷山西省大同市第一中学校2023-2024学年高一下学期4月期中考试化学试题
4 . 某研究性学习小组利用如图装置制备 ,并对
,并对 的性质进行探究(装置的气密性已检查)。
的性质进行探究(装置的气密性已检查)。
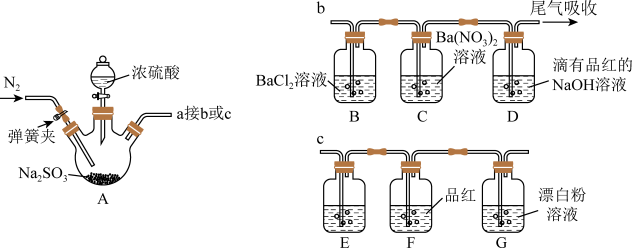
Ⅰ.探究 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)
(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是_______ 。
(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是_______ ,装置C中反应的离子方程式是_______ 。
(3)装置D中 全部转化为
全部转化为 的离子方程式为:
的离子方程式为:_______ 。
Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是_______
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是_______ ,其作用是_______ ,通过_______ 现象即可证明亚硫酸的酸性强于次氯酸。
 ,并对
,并对 的性质进行探究(装置的气密性已检查)。
的性质进行探究(装置的气密性已检查)。
Ⅰ.探究
 与可溶性钡的强酸盐是否反应(接口a接b)
与可溶性钡的强酸盐是否反应(接口a接b)(1)滴加浓硫酸之前,打开弹簧夹,通入一段时间
 ,再关闭弹簧夹,此操作的目的是
,再关闭弹簧夹,此操作的目的是(2)实验过程中装置B中没有明显变化,装置C中有白色沉淀生成,该沉淀不溶于稀盐酸。据B中现象得出的结论是
(3)装置D中
 全部转化为
全部转化为 的离子方程式为:
的离子方程式为:Ⅱ.探究亚硫酸与次氯酸的酸性强弱(接口a接c)
(4)将少量装置A中生成的气体直接通入装置G中,不能根据G中现象判断亚硫酸与次氯酸的酸性强弱,理由是
(5)为了验证亚硫酸与次氯酸的酸性强弱,需要制备一种中间酸,装置E中药品是
您最近一年使用:0次
2022-06-17更新
|
137次组卷
|
2卷引用:吉林省长春外国语学校2023-2024学年高二上学期开学考试化学试题
5 . 某化学兴趣小组探究SO2与Ca( NO3)2溶液的反应。
I.实验一:用如下装置制备SO2,然后将SO2通入Ca(NO3)2溶液中,有白色沉淀M产生。

(1)固体a是_______ (写名称) 。
(2)装置D的作用是_______ 。
(3)配制1mol·L-1Ca(NO3)2溶液时所用蒸馏水必须除去溶解的氧气,除氧方法是_______ 。
II.根据所学知识推测:白色沉淀M可能为CaSO3或CaSO4也可能是二者混合物。(查阅资料得知:CaSO4微溶于水;CaSO3难溶于水。)
实验二:探究白色沉淀M的成分。反应后将装置C中物质转移到烧杯中静置,利用倾析法倾倒出上层清液,抽滤,洗涤得到沉淀M。取沉淀M少许于试管中,加入过量的稀HCI,充分反应,发现沉淀部分溶解。由此可知白色沉淀M含有CaSO3。
(4)适合利用倾析法将下列物质与水分离的是_______
(5)取加入过量稀HCl静置后的上层溶液于试管中,加入一种试剂,可进一步证实沉淀M中含有CaSO3,则所加试剂及现象是_______ 。
实验三:探究SO 的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。
的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。
(6)有氧CaCl2溶液中通入SO2发生反应的离子方程式为_______ 。
(7)从上述实验现象可得出对SO2氧化起主要作用的是_______ (填O2或NO ),其理由是
),其理由是_______ 。
I.实验一:用如下装置制备SO2,然后将SO2通入Ca(NO3)2溶液中,有白色沉淀M产生。

(1)固体a是
(2)装置D的作用是
(3)配制1mol·L-1Ca(NO3)2溶液时所用蒸馏水必须除去溶解的氧气,除氧方法是
II.根据所学知识推测:白色沉淀M可能为CaSO3或CaSO4也可能是二者混合物。(查阅资料得知:CaSO4微溶于水;CaSO3难溶于水。)
实验二:探究白色沉淀M的成分。反应后将装置C中物质转移到烧杯中静置,利用倾析法倾倒出上层清液,抽滤,洗涤得到沉淀M。取沉淀M少许于试管中,加入过量的稀HCI,充分反应,发现沉淀部分溶解。由此可知白色沉淀M含有CaSO3。
(4)适合利用倾析法将下列物质与水分离的是_______
| A.易沉淀固体 | B.胶状物质 | C.大颗粒沉淀 | D.絮状物质 |
实验三:探究SO
 的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。
的产生途径,将SO2分别缓慢通入物质的量浓度相等的无氧CaCl2 溶液、有氧CaCl2溶液、无氧Ca( NO3)2溶液中,一段时间后,测溶液的pH ,结果表明:①无氧CaCl2溶液中无沉淀,其它两溶液中均有沉淀;②三种溶液均呈酸性,其中无氧CaCl2溶液酸性最弱,有氧CaCl2溶液酸性最强。(6)有氧CaCl2溶液中通入SO2发生反应的离子方程式为
(7)从上述实验现象可得出对SO2氧化起主要作用的是
 ),其理由是
),其理由是
您最近一年使用:0次
2022-02-17更新
|
613次组卷
|
2卷引用:吉林省长春市博硕学校(原北师大长春附属学校)2021-2022学年高二下学期期末考试化学试题
名校
解题方法
6 . 采用下图装置制备乙烯并研究乙烯与溴水的反应。实验观察到溴水褪色,得到无色透明的溶液。进一步分析发现反应产物主要为BrCH2CH2OH,含少量BrCH2CH2Br。下列说法不正确的是
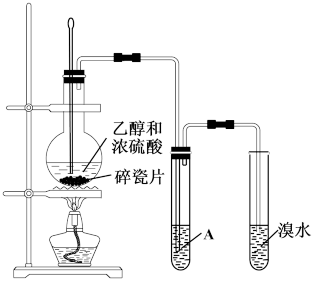

A.实验室制乙烯的方程式:CH3CH2OH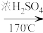 CH2=CH2↑+H2O CH2=CH2↑+H2O |
| B.除杂试剂A为NaOH溶液 |
| C.乙烯与溴水反应后的溶液近乎中性 |
| D.BrCH2CH2OH与H2O之间存在氢键 |
您最近一年使用:0次
2022-01-14更新
|
784次组卷
|
7卷引用:吉林省长春外国语学校2022-2023学年高二下学期5月期中考试化学试题
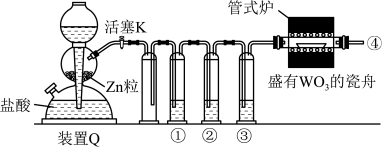
7 . 实验室用 还原
还原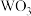 制备金属W的装置如图所示(
制备金属W的装置如图所示( 粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
 还原
还原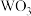 制备金属W的装置如图所示(
制备金属W的装置如图所示( 粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气),下列说法正确的是
A.①、②、③中依次盛装 溶液、浓 溶液、浓 、焦性没食子酸溶液 、焦性没食子酸溶液 |
| B.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气 |
| C.结束反应时,先关闭活塞K,再停止加热 |
| D.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度 |
您最近一年使用:0次
2021-11-01更新
|
2151次组卷
|
49卷引用:【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题
【全国百强校】吉林省延边第二中学2018-2019学年高二下学期第二次月考化学试题陕西省延安市吴起高级中学2019-2020学年高二下学期第四次质量检测(期末)化学试题江西省贵溪市实验中学2020-2021学年高二上学期第一次月考化学试题安徽省师范大学附属中学2016-2017学年高一下学期期末考试化学试题河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅰ卷精编版)甘肃省武威市第六中学2018届高三上学期第二次阶段性过关考试化学试题新疆阿克苏市农一师中学2018届高三上学期第二次月考化学试题湖南省永州市祁阳县高考补习学校2018届高三上学期第二次月考化学试题湖北省荆州中学2018届高三上学期第三次双周考(11月)化学试卷安徽省六安市第一中学2018届高三上学期第三次月考化学试题广东省揭阳市第一中学2018届高三上学期第二次阶段考试化学试题福建省莆田第一中学2018届高三上学期第一学段化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.15 物质的制备及实验方案设计与评价(已下线)《考前20天终极攻略》-5月27日 综合实验设计、探究和评价甘肃省酒泉市敦煌中学2019届高三一诊化学试题2018-2019学年人教版高中化学必修一模块综合测评题(A)【全国百强校】江苏省如东高级中学2018-2019学年高一上学期第二次月考化学试题云南省石屏县第二中学2020届高三上学期开学考试化学试题浙江省嘉兴市第一中学2020届高三上学期期中考试化学试题黑龙江省伊春市第二中学2020届高三上学期期末考试理综化学试题2020届人教版本高三化学第一轮复习第十章《化学实验热点》测试卷2020届人教版高三专题基础复习专题10《化学实验热点》测试卷江苏省苏州新草桥中学2020届高三上学期10月月考化学试题云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题河北衡水中学2020届高三下学期三月份教学质量监测理科综合化学试题(已下线)广东省深圳中学2020届高三3月份教学质量监测卷理综化学试题湖南省长沙市礼雅中学2020届高三下学期三月份网络教学质量监测理科综合化学试题河北省石家庄市第二中学2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分湖北省武汉市华中师范大学第一附属中学2020届高三下学期四月份网络教学质量监测理科综合化学试题(已下线)第27讲 物质的分离提纯和检验-2021年高考化学一轮复习名师精讲练浙江大学附属中学 2019 年选考科目阶段性教学质量检测高三化学(B 卷)试题山东省潍坊市临朐县实验中学2021届高三9月月考化学试题山东省济南市商河县第一中学2021届高三上学期阶段性考试化学试题(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(精讲)——2021年高考化学一轮复习讲练测(已下线)易错19 实验装置类选择题-备战2021年高考化学一轮复习易错题(已下线)第二章 元素与物质世界(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)(已下线)专题2.2.3 氯气的制备(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)(已下线)理综化学-2021年秋季高三开学摸底考试卷01(课标全国专用)黑龙江省哈尔滨市第三中学校2021-2022学年高三上学期期中考试化学试题(已下线)考向33 从实验到化学-备战2022年高考化学一轮复习考点微专题福建泉州市第一中学2021-2022学年高三上学期期中考化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(湖北专用)(已下线)卷12 化学综合实验选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)河北省衡水市武强中学2021-2022学年高一上学期第三次月考化学试题(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(练)-2023年高考化学一轮复习讲练测(全国通用)山东省“学情空间”区域教研共同体2022-2023学年高三上学期入学考试化学试题河南省南阳市第一中学校2022-2023学年高三上学期第一次月考化学试题河北省石家庄市第十七中学2023-2024学年高三上学期第一次月考化学试题
解题方法
8 . I.在碘化钾和硫酸的混合溶液中加入过氧化氢水溶液,迅速发生反应放出大量气体,反应过程可表示如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)H2O2在反应③中的作用是______ (填正确选项的标号)
A.氧化剂 B.还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为______ (填“对”或“不对”),其理由是______ 。
(3)上述反应说明H2O2、I2、HIO氧化性从强到弱的顺序是______ >______ >______ 。
II.硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。请回答下列问题:
(1)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,写出Fe(OH)3与NaClO在碱性介质中反应的离子方程式是______ 。
(2)硫酸亚铁制备中实验步骤①的目的是______ 。
(3)实验步骤②明显不合理,理由是______ 。
(4)实验步骤④中用少量冰水洗涤晶体,其目的是______ 。
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)H2O2在反应③中的作用是
A.氧化剂 B.还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为
(3)上述反应说明H2O2、I2、HIO氧化性从强到弱的顺序是
II.硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。请回答下列问题:
(1)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,写出Fe(OH)3与NaClO在碱性介质中反应的离子方程式是
(2)硫酸亚铁制备中实验步骤①的目的是
(3)实验步骤②明显不合理,理由是
(4)实验步骤④中用少量冰水洗涤晶体,其目的是
您最近一年使用:0次
9 . 某同学为验证酸性:醋酸>碳酸>苯酚,经仔细考虑,设计如下实验装置,请回答下列问题:
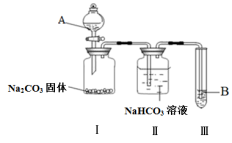
(1)A处的试剂是_______ (填序号,下同),B处的试剂是_______ 。
①醋酸溶液 ②CH3COONa溶液 ③苯酚溶液 ④苯酚钠溶液
(2)装置II中饱和NaHCO3溶液的作用_______ 。
(3)能证明三种酸的酸性强弱的现象_______ 。
(4)写出装置III中发生反应的化学方程式_______ 。

(1)A处的试剂是
①醋酸溶液 ②CH3COONa溶液 ③苯酚溶液 ④苯酚钠溶液
(2)装置II中饱和NaHCO3溶液的作用
(3)能证明三种酸的酸性强弱的现象
(4)写出装置III中发生反应的化学方程式
您最近一年使用:0次
2021-04-29更新
|
674次组卷
|
4卷引用:吉林省长春市第二十中学2020-2021学年高二下学期第二次质量测试化学试题
吉林省长春市第二十中学2020-2021学年高二下学期第二次质量测试化学试题北京市丰台区2020-2021学年高二下学期期中联考化学(B卷)试题(已下线)作业07 醇 酚-2021年高二化学暑假作业(人教版2019)(已下线)第08讲 酚(讲义)-【寒假自学课】2023年高二化学寒假精品课(人教版2019选择性必修3)
10 . 实验室通常用下图所示的装置来制取氨气。
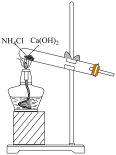
回答下列问题:
(1)写出反应的化学方程式__________ ;
(2)试管口略向下倾斜的原因是__________ ;
(3)待氨气生成后,将蘸有浓盐酸的玻璃棒靠近导管口,产生的现象是_________ ;
(4)除氨气外,还可以用该装置制取的常见气体是_________ ;
(5)氨气极易溶于水,其水溶液显弱碱性,则氨水中除H2O、H+外还存在哪些分子和离子_______ 。

回答下列问题:
(1)写出反应的化学方程式
(2)试管口略向下倾斜的原因是
(3)待氨气生成后,将蘸有浓盐酸的玻璃棒靠近导管口,产生的现象是
(4)除氨气外,还可以用该装置制取的常见气体是
(5)氨气极易溶于水,其水溶液显弱碱性,则氨水中除H2O、H+外还存在哪些分子和离子
您最近一年使用:0次



