1 . 某同学按图示装置进行实验,实验过程中观察到只有试管2中的澄清石灰水变浑浊,下列说法正确的是
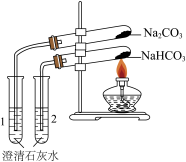
| A.该实验能证明碳酸钠的热稳定性更强 |
| B.实验结束后需要先熄灭酒精灯,再将导管移出澄清石灰水 |
| C.碳酸钠俗名纯碱,溶于水时会放出热量 |
D.可以用澄清石灰水鉴别 和 和 |
您最近一年使用:0次
2024-08-21更新
|
61次组卷
|
2卷引用:贵州省六盘水市水城区2023-2024学年高一上学期12月月考化学试题
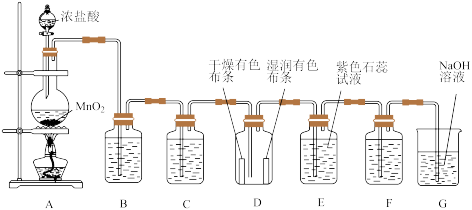
2 . 某化学兴趣小组用如图实验装置和药品制备氯气并检测氯气的相关性质,请回答问题。_______ ;该反应中氧化剂和还原剂物质的量之比为______ 。
(2)装置B中的试剂是_______ ,作用是_______ ;装置C中的试剂是_______ ,作用是_______ 。
(3)装置D中的现象是_______ ,通过这一现象能得出的结论是_______ 。
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的_______ (填序号),证明氯气有氧化性的实验现象是_______ ,发生的化学方程式是_______ 。
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是_______ 。
(2)装置B中的试剂是
(3)装置D中的现象是
(4)若要证明氯气具有氧化性,可在装置F中盛装下列试剂中的
a.酸性KMnO4溶液 b.FeCl3溶液 c.CuSO4溶液 d.淀粉碘化钾溶液
(5)装置G的作用是
您最近一年使用:0次
解题方法
3 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题。
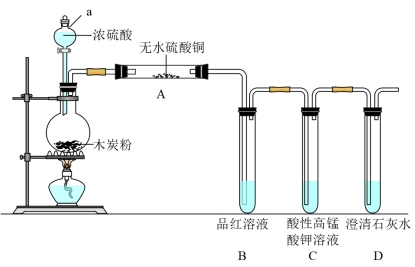
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式_______ 。
(2)仪器a的名称是_______ 。
(3)装置A中出现_______ 现象,证明气体产物中有 。
。
(4)C装置作用是_______ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式
(2)仪器a的名称是
(3)装置A中出现
 。
。(4)C装置作用是
您最近一年使用:0次
2022-04-15更新
|
999次组卷
|
4卷引用:贵州省“三新”改革联盟校2021-2022学年高一下学期联考试题(三) 化学试题
名校
解题方法
4 . 为探究SO2与Fe3+间是否发生氧化还原反应,按如图所示装置进行实验(夹持、加热仪器略),下列说法正确的是

| A.A中的反应仅体现了浓硫酸的氧化性 |
| B.试剂a为饱和NaHCO3溶液 |
| C.C中溶液pH降低,证明Fe3+氧化了SO2 |
| D.检验C中的溶液含有Fe2+,证明Fe3+氧化了SO2 |
您最近一年使用:0次
2022-02-22更新
|
678次组卷
|
11卷引用:贵州省贵阳市五校2021-2022学年高三下学期联考(五)理科综合化学试题
贵州省贵阳市五校2021-2022学年高三下学期联考(五)理科综合化学试题北京市朝阳区六校2020届高三四月联考化学(B卷)试题(已下线)北京市2019-2020学年高三各区一模化学考试分类汇编 选择题:化学与生活 氧化还原反应 阿伏加德罗常数上海市静安区2021届高三一模化学试题(已下线)重点1 仪器组合型实验方案的设计与评价-2021年高考化学【热点·重点·难点】专练(新高考)重庆市南开中学2020-2021学年高一下学期期中考试化学试题(已下线)考向35 实验的方案设计与评价-备战2022年高考化学一轮复习考点微专题上海市杨浦高级中学2021-2022学年高一上学期期末考试化学试题湖南省株洲市第二中学2022届高三下学期期中考试化学试题 上海市大同中学2021-2022学年高一下学期期中考试化学试题北京师范大学附属实验中学2024-2025学年高三上学期开学考试化学试题
5 . 某兴趣小组为丰富课本所学的SO2性质,设计了下列系列实验:
(1)用下图装置制取并收集SO2以验证其氧化性
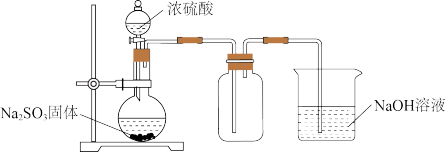
①Na2SO3久置于空气中易变质,体现了Na2SO3具有___________ 性。
②烧杯中NaOH溶液的作用是___________ 。
③若将集气瓶换成盛有Na2S溶液的广口瓶,通气一段时间后产生大量淡黄色浑浊现象,经测定,产物中还有一种相对分子质量为104的酸式盐。则该酸式盐的化学式为___________ 。
(2)用下图装置验证H2SO3比H2CO3酸性强
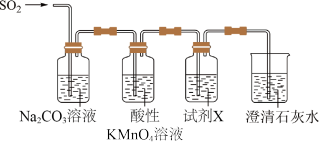
①试剂X是___________ ,其作用是___________ 。
②当观察到___________ ,即证明H2SO3比H2CO3酸性强。
(1)用下图装置制取并收集SO2以验证其氧化性

①Na2SO3久置于空气中易变质,体现了Na2SO3具有
②烧杯中NaOH溶液的作用是
③若将集气瓶换成盛有Na2S溶液的广口瓶,通气一段时间后产生大量淡黄色浑浊现象,经测定,产物中还有一种相对分子质量为104的酸式盐。则该酸式盐的化学式为
(2)用下图装置验证H2SO3比H2CO3酸性强

①试剂X是
②当观察到
您最近一年使用:0次
2020-12-17更新
|
506次组卷
|
4卷引用:贵州省六盘水市六枝特区2021-2022学年高一下学期期中教学质量检测化学试题
6 . 实验是学习化学的基础,某课外兴趣小组在学了苯与液溴的反应以后,对该反应的类型提出了猜想。
(1)甲组认为苯与液溴的反应是加成反应,乙组则认为苯与液溴的反应是___ ,对此问题你认为该怎样去证明,说出你的方法:___ 。
为了证明他们的猜想是否正确,按照如图的实验装置(夹持装置省略)进行实验。___ (装置Ⅰ或装置Ⅱ),装置Ⅱ的A中CCl4溶液的作用是___ 。
(3)装有苯和铁粉的仪器名称是___ ,B集气瓶的作用是___ ,若试管中出现___ 现象乙组猜想正确。
(4)写出铁与液溴反应的化学方程式___ ,苯和液溴反应的化学方程式___ 。
(5)简要叙述除去溴苯中溴的方法:___ 。
(1)甲组认为苯与液溴的反应是加成反应,乙组则认为苯与液溴的反应是
为了证明他们的猜想是否正确,按照如图的实验装置(夹持装置省略)进行实验。
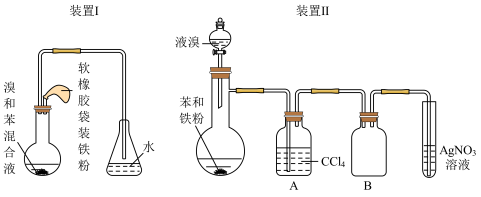
(3)装有苯和铁粉的仪器名称是
(4)写出铁与液溴反应的化学方程式
(5)简要叙述除去溴苯中溴的方法:
您最近一年使用:0次
名校
解题方法
7 . 根据下图所示装置回答以下问题。已知:①KMnO4常温下与浓盐酸反应可制得Cl2。②H2SiO3不溶于水。

(1)利用如图装置可以验证元素非金属性的变化规律。图中A装置的名称是________________ 。干燥管D的作用是____________ 。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为____________________________ 。装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_____________________ 。
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀HNO3 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2。试剂A与C分别为________ (填序号);试管中发生反应的离子方程式为__________________ 。有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为原因是_____________________ 。

(1)利用如图装置可以验证元素非金属性的变化规律。图中A装置的名称是
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性强于硫:烧瓶中发生反应的离子方程式为
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀HNO3 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2。试剂A与C分别为
您最近一年使用:0次
2020-01-13更新
|
531次组卷
|
12卷引用:贵州省榕江县第三高级中学2019-2020学年高一上学期期末考试化学试题
贵州省榕江县第三高级中学2019-2020学年高一上学期期末考试化学试题贵州省岑巩县第二中学2019-2020学年高一上学期期末考试化学试题云南省梁河县第一中学2019-2020学年高一上学期期末考试化学试题云南省文山壮族苗族自治州富宁县第二中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区河池市罗城县第二高级中学2019-2020学年高一上学期期末考试化学试题安徽省定远县育才学校2019-2020学年高一下学期4月月考化学试题甘肃省张掖市临泽县第一中学2019-2020学年高一下学期期中考试化学试题四川省泸县第二中学2019-2020学年高一下学期期末模拟考试化学试题(已下线)5.1.3 同主族元素的性质(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)云南省玉溪第三中学2021-2022学年高一上学期期末考试化学试题广西钦州市第四中学2022-2023学年高一上学期12月份考试化学试题河北省衡水市河北武强中学2023-2024学年高二上学期开学考试化学试题
8 . 草酸(乙二酸)存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,而其钙盐为沉淀。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。甲组、乙组两位同学对草酸分解产物进行探究。甲组同学认为:草酸分解产物中有CO2;乙组同学认为:草酸分解产物中还有CO。回答下列问题:
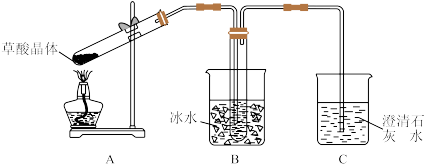
(1)甲组同学按照上图所示的装置连接,通过实验检验草酸晶体的分解产物。加热A装置前需要进行的操作是______________________ ;装置C中可观察到的现象是______________________________ ,装置C中发生的化学方程式_________________ ;由此可知草酸晶体分的产物中有___________ (填化学式)。
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验.

①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、D、G____________ (按合理顺序补全装置,填大写字母)。装置H反应管中盛有的物质是______________ ,此反应管中发生反应的化学方程式是_______________________ 。
②能证明草酸晶体分解产物中有CO的现象是_____________________________________________

(1)甲组同学按照上图所示的装置连接,通过实验检验草酸晶体的分解产物。加热A装置前需要进行的操作是
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验.

①乙组同学的实验装置中,依次连接的合理顺序为A、B、F、D、G
②能证明草酸晶体分解产物中有CO的现象是
您最近一年使用:0次
解题方法
9 . 为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)实验过程如图:
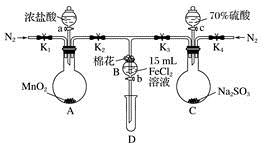
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是________________________ 。
(2)棉花中浸润的溶液为_____________ 。作用是___________________ 。
(3)A中发生反应的化学方程式:______________________________________ 。
(4)导致步骤Ⅲ中溶液变黄的离子反应是______________________________ 。用______________ (写试剂化学式)检验氧化产物,现象是____________ 。
(5)能说明氧化性Fe3+>SO2的离子方程式是__________________________ 。
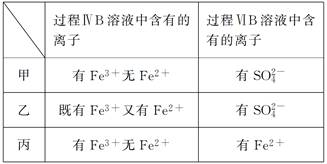
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是________________ (填“甲”“乙”或“丙”)。

Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)棉花中浸润的溶液为
(3)A中发生反应的化学方程式:
(4)导致步骤Ⅲ中溶液变黄的离子反应是
(5)能说明氧化性Fe3+>SO2的离子方程式是
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是

您最近一年使用:0次
2018-06-28更新
|
541次组卷
|
4卷引用:贵州省三都水族自治县高级中学2019-2020学年高一上学期期末考试化学试题
解题方法
10 . 下图是元素①~⑤在元素周期表中的位置。
(1)⑤在周期表中的位置是第_______ 周期第_______ 族,其最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(2)③的一种核素的中子数是9,表示该核素的符号是_______ 。
(3)非金属性:④_______ ⑤(填“>”或“<”),从原子结构角度解释其原因:_______ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程_______ 。
(5)下列关于①的说法正确的是_______ (填字母)。
a.原子结构示意图为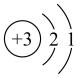
b.其单质可以和水反应生成
c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
下列说法中,正确的是_______(填字母)。
| ① | ③ | ④ | |||||
| ② | ⑤ | ||||||
(1)⑤在周期表中的位置是第
(2)③的一种核素的中子数是9,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a.原子结构示意图为

b.其单质可以和水反应生成

c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
| 实验 | ||
| 装置 | 液体a | 现象 |
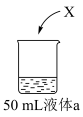 | 蒸馏水 | Ⅰ.X浮在液面上,剧烈反应,产生少量白雾 |
 盐酸 盐酸 | Ⅱ.X浮在液面上,反应比Ⅰ中剧烈,产生白雾 | |
| 浓盐酸 | Ⅲ.X浮在液面上,反应比Ⅰ中缓慢,产生大量白雾,烧杯底部有白色固体 | |
| A.Ⅰ中现象说明X与水反应放热 |
B.Ⅱ中反应的离子方程式为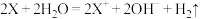 |
| C.Ⅲ中白雾比Ⅱ中多,说明Ⅲ中反应放热比Ⅱ中更多 |
D.推测Ⅲ中反应缓慢可能与 以及生成的白色固体有关 以及生成的白色固体有关 |
您最近一年使用:0次



