解题方法
1 . 某学习小组欲设计实验探究焦炭与二氧化硅反应的产物。
查阅资料:实验室可以用PdCl2溶液检验CO,二者发生反应会产生黑色金属钯,溶液变浑浊。
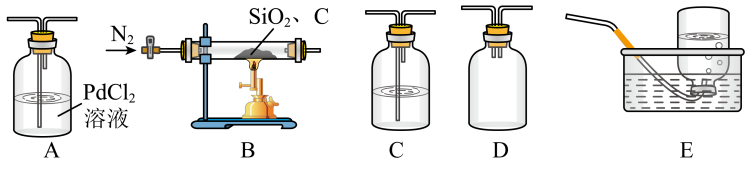
回答下列问题:
(1)上述装置连接顺序(按气流从左至右)为B→________ →E。
(2)加热前,向装置内通入一段时间氮气,其目的是________ ;D装置的作用是________ 。
(3)若A中出现浑浊,写出A中发生反应的化学方程式________ 。
(4)C装置可用来检验CO2气体,可选用的试剂是________ (填字母)。
(5)如果不用E装置,可能的后果是________ 。
(6)经测定B装置中生成的CO与CO2物质的量之比为2:1,写出B中发生反应的化学方程式________ 。
查阅资料:实验室可以用PdCl2溶液检验CO,二者发生反应会产生黑色金属钯,溶液变浑浊。
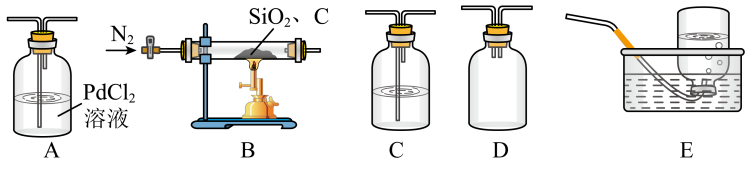
回答下列问题:
(1)上述装置连接顺序(按气流从左至右)为B→
(2)加热前,向装置内通入一段时间氮气,其目的是
(3)若A中出现浑浊,写出A中发生反应的化学方程式
(4)C装置可用来检验CO2气体,可选用的试剂是
| A.NaOH溶液 | B.Ba(OH)2溶液 |
| C.BaCl2溶液 | D.品红溶液 |
(6)经测定B装置中生成的CO与CO2物质的量之比为2:1,写出B中发生反应的化学方程式
您最近一年使用:0次
2 . 已知稀溴水和氯化铁溶液都呈黄色,现在足量的稀氯化亚铁溶液中,加入1~2滴液溴,振荡后溶液呈黄色,现对溶液呈黄色的原因进行探究。
(1)仅限选用的仪器和试剂有:烧杯、试管、玻璃棒、量筒、滴管、药匙;酸性高锰酸钾溶液、氢氧化钠溶液、四氯化碳、硫氰化钾溶液、硝酸银溶液、淀粉碘化钾溶液,完成以下实验探究过程:
【提出假设】
假设1:溶液呈黄色不是发生化学反应所致,是溶液中___________ 引起的(填微粒的化学式,下同)。
假设2:溶液呈黄色是发生化学反应所致,是溶液中___________ 引起的。
【设计实验方案】
为了验证上述假设1和假设2的推断,请用简要的文字说明你的实验方案:
假设1方案:__________________________________ 。
假设2方案:__________________________________ 。
(2)根据高中所学的知识判断,你认为__________ (填“假设1”或“假设2”)的推断是正确的;若选用淀粉碘化钾溶液验证你的假设是否可行?________ (填“行”或“否”)。
(3)写出铁离子与碘离子作用的离子方程式____________ 反应,并以该反应原理设计原电池,将电池装置示意图画在下边方框中。

____________
(1)仅限选用的仪器和试剂有:烧杯、试管、玻璃棒、量筒、滴管、药匙;酸性高锰酸钾溶液、氢氧化钠溶液、四氯化碳、硫氰化钾溶液、硝酸银溶液、淀粉碘化钾溶液,完成以下实验探究过程:
【提出假设】
假设1:溶液呈黄色不是发生化学反应所致,是溶液中
假设2:溶液呈黄色是发生化学反应所致,是溶液中
【设计实验方案】
为了验证上述假设1和假设2的推断,请用简要的文字说明你的实验方案:
假设1方案:
假设2方案:
(2)根据高中所学的知识判断,你认为
(3)写出铁离子与碘离子作用的离子方程式

您最近一年使用:0次
3 . 某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3•6H2O晶体.(图中夹持及尾气处理装置均已略去)
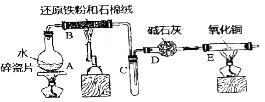
(1)装置B中发生反应的化学方程式是________ ;
(2)装置E中的现象是________ ;
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液里含有Fe3+,选用的试剂为________ ,现象是________ ;
②该实验小组同学用上述试剂没有检验到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因________ ;
③将此溶液中FeCl2完全氧化为FeCl3,最好选择下列物质中的________
④在③所得溶液浓缩结晶前需要用实验证明FeCl2已完全氧化,实验方法是________ 。

(1)装置B中发生反应的化学方程式是
(2)装置E中的现象是
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液里含有Fe3+,选用的试剂为
②该实验小组同学用上述试剂没有检验到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因
③将此溶液中FeCl2完全氧化为FeCl3,最好选择下列物质中的
| A.酸性KMnO4溶液 | B.Cl2 | C.Na2O2 | D.FeCl3 |
您最近一年使用:0次
2016-12-09更新
|
426次组卷
|
3卷引用:2015-2016学年山西省怀仁一中高一下第一次月考化学试卷
2015-2016学年山西省怀仁一中高一下第一次月考化学试卷(已下线)第三章 章末检测(1)——《高中新教材同步备课》(人教版 必修第一册)安徽省池州市第一中学2020-2021学年高一12月月考化学试题
4 . 化学小组同学依据化学反应Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与110 mL 98%的浓H2SO4充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。(F中为无水硫酸铜)
ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与110 mL 98%的浓H2SO4充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。(F中为无水硫酸铜)
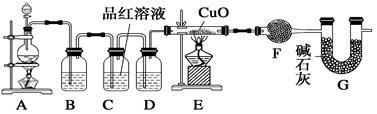
请回答下列问题:
(1)装置A中添加液体的仪器名称为_____________ ; 98%的浓H2SO4(ρ=1.84 g/cm3)的物质的量浓度是______________ ;
(2)装置B是为了吸收SO2,则不能选用下列试剂中的___________ (填序号);
A.NaOH溶液 B.浓H2SO4 C.KMnO4溶液
(3)装置D的作用是__________________________ ;
(4)可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有氢气的实验现象是______________________ 。
 ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与110 mL 98%的浓H2SO4充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。(F中为无水硫酸铜)
ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与110 mL 98%的浓H2SO4充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。(F中为无水硫酸铜)
请回答下列问题:
(1)装置A中添加液体的仪器名称为
(2)装置B是为了吸收SO2,则不能选用下列试剂中的
A.NaOH溶液 B.浓H2SO4 C.KMnO4溶液
(3)装置D的作用是
(4)可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有氢气的实验现象是
您最近一年使用:0次
5 . 某学生设计了一套验证物质化学性质的实验装置(如图):
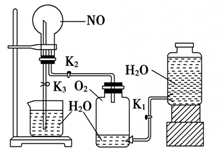
请观察该装置图,完成下列问题:
(1)该实验的目的是________________________ 。
(2)该实验的涉及的化学方程式有___________________ 。
(3)实验用品:实验仪器除铁架台(带铁夹)、储气瓶(两个)、直管活塞(K1、K2)、止水夹(K3)、橡胶管、橡胶塞以及若干玻璃管连件外,还有哪几种(写仪器名称)_________________ 。
(4)实验步骤:①按上图连接好仪器装置;②扭开活塞K1和K2,主要现象为______________ ;③关闭________ ,(填写K1或K2或K3)打开________ ,(填写K1或K2或K3), 用手或热毛巾捂住圆底烧瓶,就能使烧瓶产生喷泉。

请观察该装置图,完成下列问题:
(1)该实验的目的是
(2)该实验的涉及的化学方程式有
(3)实验用品:实验仪器除铁架台(带铁夹)、储气瓶(两个)、直管活塞(K1、K2)、止水夹(K3)、橡胶管、橡胶塞以及若干玻璃管连件外,还有哪几种(写仪器名称)
(4)实验步骤:①按上图连接好仪器装置;②扭开活塞K1和K2,主要现象为
您最近一年使用:0次
2016-12-09更新
|
429次组卷
|
3卷引用:2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷
(已下线)2014福建安溪一中、养正中学、惠安一中高一下学期期末化学试卷2014-2015学年湖北省襄阳市老河口高级中学高二下学期期末化学试卷黑龙江省青冈县一中2018-2019学年高一下学期期末考试(A+班)化学试题
解题方法
6 . 某实验小组用如图所示装置进行实验以探究Fe3+、Cl2和SO2的氧化性强弱(夹持仪器已略)。
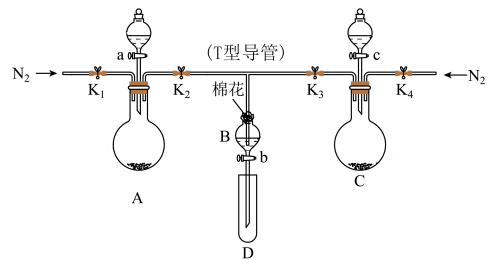
(1)按图连接好装置,检查装置的气密性后添加药品:向A装置的分液漏斗中加入浓盐酸,在圆底烧瓶中加入固体KMnO4;向B装置中加入10 mL FeCl2溶液,棉花浸润________ 溶液;在C装置的分液漏斗中加入70%的硫酸,向圆底烧瓶中加入固体Na2SO3。
(2)打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2。通入一段时间N2的目的是__________________ 。
(3)关闭K1,K3,K4,打开活塞a 和K2,逐滴加入浓盐酸,A装置中发生反应的方程式为___________ 。
(4)当B中溶液变为棕黄色时,停止滴加浓盐酸,夹紧K2,打开活塞b,使约2 mL的溶液流入D试管中,分别取1 mL溶液滴入_______ (填试剂名称)和铁氰化钾溶液可以证明其中含有Fe3+和Fe2+。此时B中发生反应的离子方程式为____________ 。
(5)打开K3和活塞c,逐滴加入70%的硫酸,当B中溶液颜色逐渐变为_____ 色,停止滴加70%的硫酸,夹紧K3,打开活塞b,使约2 mL的溶液流入D试管中,并检验其中的离子。此时B中发生反应的离子方程式为______________ 。
(6)结合实验现象判断Fe3+、Cl2、SO2氧化性由强到弱的顺序为___________ 。

(1)按图连接好装置,检查装置的气密性后添加药品:向A装置的分液漏斗中加入浓盐酸,在圆底烧瓶中加入固体KMnO4;向B装置中加入10 mL FeCl2溶液,棉花浸润
(2)打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2。通入一段时间N2的目的是
(3)关闭K1,K3,K4,打开活塞a 和K2,逐滴加入浓盐酸,A装置中发生反应的方程式为
(4)当B中溶液变为棕黄色时,停止滴加浓盐酸,夹紧K2,打开活塞b,使约2 mL的溶液流入D试管中,分别取1 mL溶液滴入
(5)打开K3和活塞c,逐滴加入70%的硫酸,当B中溶液颜色逐渐变为
(6)结合实验现象判断Fe3+、Cl2、SO2氧化性由强到弱的顺序为
您最近一年使用:0次
解题方法
7 . 某学习小组同学探究FeSO4的化学性质和用途。
(一)利用下图装置探究FeSO4的稳定性和用途。(绿矾成分为FeSO4·7H2O)
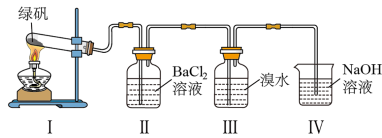
(1)II中有白色沉淀生成,说明FeSO4固体分解生成了_____________ 。
(2)III中溴水是用来检验是否有SO2气体生成,涉及的化学方程式为_________________ ,实验中,观察到溴水褪色,据此推测FeSO4分解最有可能被氧化的元素是______________ 。
(3)Ⅳ中足量NaOH溶液的作用是吸收SO2气体,防止其污染环境,请写出反应的离子方程式___________ 。
(二)探究FeSO4中Fe2+的还原性
(4)证明FeSO4有较强的还原性,完成下表步骤二及其现象。
(三)硫酸亚铁用途探究
(5)缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是_______________________ 。
(一)利用下图装置探究FeSO4的稳定性和用途。(绿矾成分为FeSO4·7H2O)

(1)II中有白色沉淀生成,说明FeSO4固体分解生成了
(2)III中溴水是用来检验是否有SO2气体生成,涉及的化学方程式为
(3)Ⅳ中足量NaOH溶液的作用是吸收SO2气体,防止其污染环境,请写出反应的离子方程式
(二)探究FeSO4中Fe2+的还原性
(4)证明FeSO4有较强的还原性,完成下表步骤二及其现象。
| 实验步骤 | 实验预期现象和结论 |
| 步骤一:取少量的FeSO4固体于试管中,加入一定量水溶解。 |  |
| 步骤二:滴加 | 当溶液中出现 |
(5)缺铁性贫血往往口服硫酸亚铁,当用硫酸亚铁制成药片时,外表包有一层特殊的糖衣,其作用是
您最近一年使用:0次
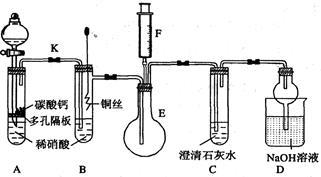
8 . 某校课外活动小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是一半空的注射器。
请回答有关问题:
(1)设计装置A的目的是________________ ;为达到此目的,应进行的操作是___________ 。
(2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是_________________________ ;B中反应的离子方程式为:_____________ 。
(3)装置E和F的作用是_______________________________________ ;为实现此作用,其操作方法是_______________________________________ 。
(4)装置D的作用是______________________________________ 。

请回答有关问题:
(1)设计装置A的目的是
(2)在完成(1)中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是
(3)装置E和F的作用是
(4)装置D的作用是
您最近一年使用:0次
2016-12-09更新
|
467次组卷
|
3卷引用:2011-2012学年安徽省马鞍山二中高一下学期期中素质测试化学试卷
(已下线)2011-2012学年安徽省马鞍山二中高一下学期期中素质测试化学试卷2014-2015四川省遂宁市射洪中学高一下学期第一次月考化学试卷河北省衡水市武强中学2020-2021学年高一下学期第一次月考化学试题
解题方法
9 . 向H2O2溶液中加入适量稀硫酸酸化的硫酸亚铁溶液,依次观察到如下现象:①反应刚开始,仅有少量气泡产生;②反应片刻后,有大量气泡产生;③试管底部最终出现红褐色沉淀。下列判断正确的是
| A.①中仅发生一个反应 | B.Fe3+能催化H2O2的分解 |
| C.反应过程中溶液pH不断减小 | D.FeSO4与等物质的量的H2O2恰好反应 |
您最近一年使用:0次
2016-12-09更新
|
375次组卷
|
2卷引用:2015届福建省龙岩市高三5月教学质量检查理综化学试卷
10 . 为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中不正确的是
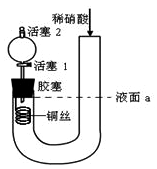

| A.关闭活塞1,加入稀硝酸至液面a处 |
| B.在装置左侧稍加热可以加快稀硝酸与铜的反应速率 |
| C.通过关闭或开启活塞1可以控制反应的进行 |
| D.反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO |
您最近一年使用:0次
2016-12-09更新
|
1695次组卷
|
19卷引用:2011届北京市丰台区高三下学期统一练习(一)(理综)化学部分
(已下线)2011届北京市丰台区高三下学期统一练习(一)(理综)化学部分2014-2015福建省福州市八县高一下学期联考化学试卷2015-2016学年黑龙江省实验中学高二下期末化学试卷上海市格致中学2016-2017学年高一下学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第4讲 氮及其化合物【押题专练】内蒙古赤峰二中2017-2018学年高一上学期期末考试化学试题(已下线)2018年12月12日 《每日一题》人教必修1-硝酸的强氧化性上海市嘉定区2016届高三第一次质量调研化学试题四川省成都龙泉第二中学2021届高三上学期九月月考化学试题浙江省浙北G2(嘉兴一中、湖州中学)2020-2021学年高二上学期期中联考化学试题辽宁省六校2021届高三上学期期中联考化学试题广东省佛山市顺德李兆基中学2020-2021学年高一3月月考化学试卷江苏省苏州市相城区黄埭中学2020-2021学年高一下学期3月月考化学试题黑龙江省哈尔滨市第六中学2020-2021学年高一4月月考化学试题湖北省部分重点高中2020-2021学年高一下学期4月联考化学试题吉林省延边第二中学2020届高三上学期第一次调研化学试题课中-5.2.3 硝酸 酸雨及防治-人教2019必修第二册江苏省盐城市东台创新高级中学2021-2022学年高一5月份月检测化学试题(已下线)3.2.2 铵盐和硝酸-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)



