名校
1 . 草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)呈淡黄色,可用于晒制蓝图。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如图装置进行实验:_______ →尾气处理装置(仪器可重复使用)。
②检查装置气密性后,先通入一段时间N2,其目的为_______ 。
③实验证明了气体产物中含有CO,依据的实验现象为_______ 。
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是_______ 。
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为_______ 。
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的实验现象为_______ 。
II.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL(已知: )。
)。
(4)步骤2中还涉及的离子方程式_______ ;步骤3中加入锌粉的目的_______ 。
(5)草酸亚铁样品的纯度为_______ (列出计算式即可);若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将_______ (填“偏高”、“偏低”或“不变”)。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如图装置进行实验:
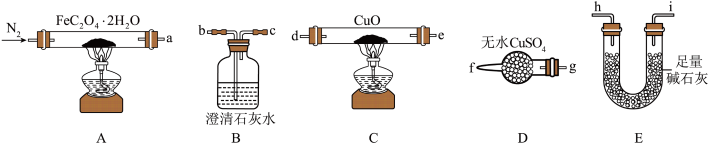
②检查装置气密性后,先通入一段时间N2,其目的为
③实验证明了气体产物中含有CO,依据的实验现象为
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的实验现象为
II.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL(已知:
 )。
)。(4)步骤2中还涉及的离子方程式
(5)草酸亚铁样品的纯度为
您最近一年使用:0次
名校
解题方法
2 . 草酸亚铁晶体(FeC2O4•2H2O,M=180g/mol)呈淡黄色,可用于晒制蓝图。南宁三中实验小组对其进行了一系列探究。采用如图装置进行实验。
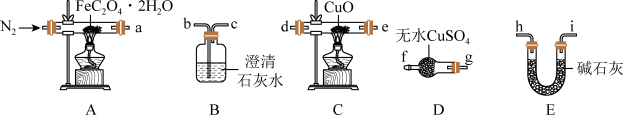
(1)为验证FeC2O4•2H2O的分解的气态产物,按照气流从左到右的方向,上述装置的连接顺序为A→_______ →尾气处理装置(仪器可重复使用)。
(2)实验证明了气体产物中含有CO,依据的实验现象为_______ 。
(3)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为_______ 。
(4)工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol/LKMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol/LKMnO4标准溶液滴定至终点,消耗标准液V2mL。
①步骤2中滴定终点的现象为_______ ;步骤3加入锌粉的目的_______ 。
②该样品中草酸亚铁晶体的质量分数的计算式为_______ 。
③若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将_______ (填“偏高”“偏低”或“不变”)。

(1)为验证FeC2O4•2H2O的分解的气态产物,按照气流从左到右的方向,上述装置的连接顺序为A→
(2)实验证明了气体产物中含有CO,依据的实验现象为
(3)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(4)工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol/LKMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol/LKMnO4标准溶液滴定至终点,消耗标准液V2mL。
①步骤2中滴定终点的现象为
②该样品中草酸亚铁晶体的质量分数的计算式为
③若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将
您最近一年使用:0次
3 . 草酸亚铁晶体( ,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。

(1)按照气流从左到右的方向,上述装置的接口顺序为A→_______ →尾气处理装置(仪器可重复使用)。
(2)实验证明了气体产物中含有 ,依据的实验现象为
,依据的实验现象为_______ 。
(3)实验证明了气体产物中含有CO,依据的实验现象为_______ 。
(4)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为_______ 。
(5)工业制得的草酸亚铁晶体中常含有 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品溶于稀 中,配成250 mL溶液;
中,配成250 mL溶液;
步骤2:取上述溶液25.00 mL,用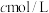
 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 ;
;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀 ,再用
,再用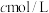
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 。
。
①步骤2中滴定终点的现象为_______ 。
②该样品中草酸亚铁晶体的质量分数的表达式为_______ 。
③若步骤1配制溶液时部分 被氧化变质,则测定结果将
被氧化变质,则测定结果将_______ (填“偏高”“偏低”或“不变”)。
 ,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
,M=180 g/mol )呈淡黄色。某学习小组采用如图装置对其进行了一系列探究其分解产物的实验。
(1)按照气流从左到右的方向,上述装置的接口顺序为A→
(2)实验证明了气体产物中含有
 ,依据的实验现象为
,依据的实验现象为(3)实验证明了气体产物中含有CO,依据的实验现象为
(4)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(5)工业制得的草酸亚铁晶体中常含有
 杂质,测定其纯度的步骤如下:
杂质,测定其纯度的步骤如下:步骤1:称取m g草酸亚铁晶体样品溶于稀
 中,配成250 mL溶液;
中,配成250 mL溶液;步骤2:取上述溶液25.00 mL,用
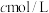
 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液 ;
;步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀
 ,再用
,再用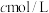
 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 。
。①步骤2中滴定终点的现象为
②该样品中草酸亚铁晶体的质量分数的表达式为
③若步骤1配制溶液时部分
 被氧化变质,则测定结果将
被氧化变质,则测定结果将
您最近一年使用:0次
2022-12-16更新
|
190次组卷
|
2卷引用:辽宁省大连市滨城联盟2022-2023学年高三上学期期中(‖)考试化学试题
名校
4 . 草酸亚铁晶体(FeC2O4·2H2O,M=180 g/mol)呈淡黄色,可用作晒制蓝图。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:
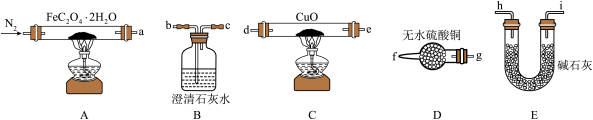
①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→_______ →尾气处理装置(仪器可重复使用)。
②检查装置气密性后,先通入一段时间N2,其目的为_______ 。
③实验证明了气体产物中含有CO,依据的实验现象为_______ 。
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是_______ 。
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为_______ 。
(3)晒制蓝图时,草酸亚铁晶体会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该反应的离子方程式为_______ 。
II.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用c mol/L KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为_______ ;
(5)若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将____ (填“偏高”、“偏低”或“不变”)。
I.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:

①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→
②检查装置气密性后,先通入一段时间N2,其目的为
③实验证明了气体产物中含有CO,依据的实验现象为
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(3)晒制蓝图时,草酸亚铁晶体会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该反应的离子方程式为
II.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用c mol/L KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为
(5)若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将
您最近一年使用:0次
5 . 草酸亚铁晶体(FeC2O4·2H2O,M=180 g/mol)呈淡黄色,可用于晒制蓝图。某实验小组对其进行了一系列探究。采用如图装置进行实验。
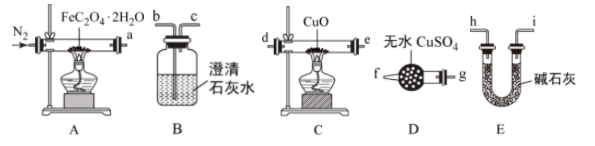
(1)按照气流从左到右的方向,上述装置的接口顺序为A→_______ →尾气处理装置(仪器可重复使用)。
(2)实验证明了气体产物中含有CO,依据的实验现象为_______ 。
(3)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为_______ 。
(4)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为_______ 。
(5)工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品溶于稀H2SO4中,配成250 mL溶液;
步骤2:取上述溶液25.00 mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用c mol/L KMnO4标准溶液滴定至终点,消耗标准液V2 mL。
①步骤2中滴定终点的现象为_______ 。
②该样品中草酸亚铁晶体的质量分数的表达式为_______ 。
③若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将_______ (填“偏高”“偏低”或“不变”)。

(1)按照气流从左到右的方向,上述装置的接口顺序为A→
(2)实验证明了气体产物中含有CO,依据的实验现象为
(3)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(4)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为
(5)工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品溶于稀H2SO4中,配成250 mL溶液;
步骤2:取上述溶液25.00 mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用c mol/L KMnO4标准溶液滴定至终点,消耗标准液V2 mL。
①步骤2中滴定终点的现象为
②该样品中草酸亚铁晶体的质量分数的表达式为
③若步骤1配制溶液时部分Fe2+被氧化变质,则测定结果将
您最近一年使用:0次
6 . 草酸亚铁晶体(FeC2O4·2H2O,M=180g/mol)呈淡黄色,可用于晒制蓝图。某实验小组对其进行了一系列探究。
Ⅰ.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如图装置进行实验:
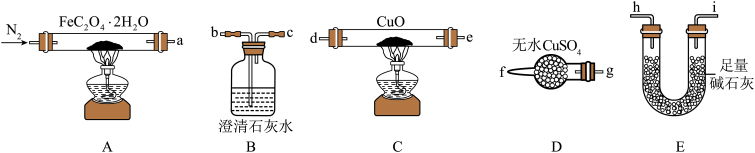
①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→___ →尾气处理装置(仪器可重复使用)。
②检查装置气密性后,先通入一段时间N2,其目的为__ 。
③实验证明了气体产物中含有CO,依据的实验现象为__ 。
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是__ 。
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为__ 。
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为__ 。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为__ ;步骤3中加入锌粉的目的为___ 。
(5)若步骤 配制溶液时部分Fe2+被氧化变质,则测定结果将
配制溶液时部分Fe2+被氧化变质,则测定结果将__ (填“偏高”、“偏低”或“不变”)
Ⅰ.纯净草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究。小组成员采用如图装置进行实验:

①按照气流从左到右的方向,上述装置的接口顺序为a→g→f→
②检查装置气密性后,先通入一段时间N2,其目的为
③实验证明了气体产物中含有CO,依据的实验现象为
④结束实验时先熄灭A、C处的酒精灯再停止通入N2,其目的是
(2)小组成员设计实验证明了A中分解后的固体成分为FeO,则草酸亚铁晶体分解的化学方程式为
(3)晒制蓝图时,草酸亚铁晶体是感光剂,会失去结晶水转化为FeC2O4,现以K3[Fe(CN)6]溶液为显色剂,该显色反应的化学方程式为
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液;
步骤2:取上述溶液25.00mL,用cmol·L-1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤2中滴定终点的现象为
(5)若步骤
 配制溶液时部分Fe2+被氧化变质,则测定结果将
配制溶液时部分Fe2+被氧化变质,则测定结果将
您最近一年使用:0次
2020-06-12更新
|
1212次组卷
|
3卷引用:吉林省延边州2020届高三4月教学质量检测理科综合化学试题
7 . 草酸亚铁晶体(FeC2O4•2H2O,M=180g/mol)呈淡黄色,可用作晒制蓝图。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究
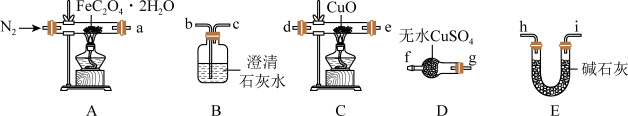
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:
①按照气流从左到右的方向,上述装置的接口顺序为 a→g→f→___________ →尾气处理装置(仪器可重复使用)。
②实验前先通入一段时间 N2,其目的为__________ 。
③实验证明了气体产物中含有 CO,依据的实验现象为__________ 。
(2)小组成员设计实验证明了 A 中分解后的固体成分为 FeO,则草酸亚铁晶体分解的化学方程式为__________ 。
(3)晒制蓝图时,以 K3[Fe(CN)6]溶液为显色剂,该反应的化学方程式为__________ 。
Ⅱ.草酸亚铁晶体样品纯度的测定:工业制得的草酸亚铁晶体中常含有 FeSO4杂质,测定其纯度的步骤如下:
步骤 1:称取 mg 草酸亚铁晶体样品并溶于稀 HSO4中,配成 250mL 溶液;
步骤 2:取上述溶液 25.00mL,用 cmol/L KMnO4标准液滴定至终点,消耗标准液 V1mL;
步骤 3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀 H2SO4,再用 cmol/L KMnO4标准溶液滴定至终点,消耗标准液 V2mL。
(4)步骤 2 中滴定终点的现象为__________ ;步骤 3 中加入锌粉的目的为__________ 。
(5)草酸亚铁晶体样品的纯度为__________ ;若步骤 1配制溶液时部分 Fe2+被氧化变质,则测定结果将__________ (填“偏高”、“偏低”或“不变”)。
I.纯净草酸亚铁晶体热分解产物的探究

(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:
①按照气流从左到右的方向,上述装置的接口顺序为 a→g→f→
②实验前先通入一段时间 N2,其目的为
③实验证明了气体产物中含有 CO,依据的实验现象为
(2)小组成员设计实验证明了 A 中分解后的固体成分为 FeO,则草酸亚铁晶体分解的化学方程式为
(3)晒制蓝图时,以 K3[Fe(CN)6]溶液为显色剂,该反应的化学方程式为
Ⅱ.草酸亚铁晶体样品纯度的测定:工业制得的草酸亚铁晶体中常含有 FeSO4杂质,测定其纯度的步骤如下:
步骤 1:称取 mg 草酸亚铁晶体样品并溶于稀 HSO4中,配成 250mL 溶液;
步骤 2:取上述溶液 25.00mL,用 cmol/L KMnO4标准液滴定至终点,消耗标准液 V1mL;
步骤 3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀 H2SO4,再用 cmol/L KMnO4标准溶液滴定至终点,消耗标准液 V2mL。
(4)步骤 2 中滴定终点的现象为
(5)草酸亚铁晶体样品的纯度为
您最近一年使用:0次
8 . 人类社会的发展离不开“求知求真”.某化学兴趣小组以 溶液与
溶液与 溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
(1)实验预测
(2)实验探究
实验一:探究 与
与 能否发生反应①,设计装置如下图,能证明反应已经发生的现象有
能否发生反应①,设计装置如下图,能证明反应已经发生的现象有_______ [已知: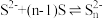 ]。
]。

实验二:探究 与
与 能否发生反应②和③,设计如下实验:
能否发生反应②和③,设计如下实验:
实验结论
 与
与 在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
 溶液与
溶液与 溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。
溶液的反应为素材,探究盐溶液之间的反应情况,体悟反应的复杂性。(1)实验预测
| 推测可能发生的反应 | 推测依据 | 预期的实验现象 |
| ①氧化还原反应 |  具有一定的氧化性, 具有一定的氧化性, 具有较强的还原性 具有较强的还原性 | 若 过量,则有淡黄色沉淀(S)生成若 过量,则有淡黄色沉淀(S)生成若 过量,则有黑色沉淀 过量,则有黑色沉淀 |
| ②复分解反应 |  为黑色难溶物, 为黑色难溶物, | 有黑色固体生成 |
| ③彻底双水解反应 |  、 、 水解能力均较强 水解能力均较强 | 有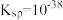 )产生,同时有臭鸡蛋气味的气体(H2S)生成 )产生,同时有臭鸡蛋气味的气体(H2S)生成 |
实验一:探究
 与
与 能否发生反应①,设计装置如下图,能证明反应已经发生的现象有
能否发生反应①,设计装置如下图,能证明反应已经发生的现象有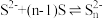 ]。
]。
实验二:探究
 与
与 能否发生反应②和③,设计如下实验:
能否发生反应②和③,设计如下实验:| 实验步骤 | 实验现象 | 实验解释或结论 |
ⅰ.向 饱和 饱和 溶液中,滴加2滴饱和 溶液中,滴加2滴饱和 溶液 溶液 | 有黑色沉淀生成,而后黑色沉淀消失,出现淡黄色沉淀 | 用离子方程式解释黑色沉淀消失的原因: |
ⅱ.将 饱和 饱和 溶液与 溶液与 饱和 饱和 溶液直接混合 溶液直接混合 | 先有黑色和另一种颜色的沉淀生成,而后都变为黑色;同时有臭鸡蛋气味的气体生成 | 试解释:沉淀最终都变为黑色的原因是 |
ⅲ.取ⅱ中最终生成的黑色沉淀样品,用无水乙醇多次洗涤后,干燥称量得 黑色固体,然后在空气中灼烧至恒重 黑色固体,然后在空气中灼烧至恒重 | 灼烧后,所得红棕色固体质量为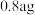 | 经计算判断,黑色固体样品的成份为 |
 与
与 在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
在溶液中相遇,会因为二者的浓度、用量等不同而反应不同,但都会先发生复分解反应。
您最近一年使用:0次
9 . 硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]又名摩尔盐,是浅绿色晶体,易溶于水,是分析化学中的重要试剂。某化学兴趣小组对摩尔盐的一些性质进行探究。回答下列问题:
(1)在试管中加入少量摩尔盐晶体,加水溶解,测得水溶液呈酸性。由此可知_______ 。
(2)摩尔盐在500℃时隔绝空气加热完全分解,气体产物可能有NH3、SO2、SO3、H2O等。兴趣小组利用下图装置证明摩尔盐分解的气体产物中有SO2和SO3。
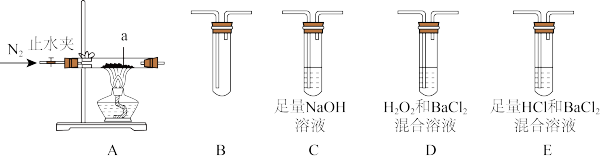
①a的名称是_______ 。装置B的作用_______ 。
②装置连接顺序为A→_______ →_______ →_______ →_______ (填字母序号)。
③能证明分解产物中有SO2的实验现象是_______ ,反应的离子方程式是_______ 。
④若装置连接顺序不变,能否将装置E中溶液换为BaCl2溶液?理由是_______ 。
(3)为判断摩尔盐是否变质,可以测定样品中Fe2+的含量。取w g样品溶于水,配制成250 mL溶液。每次取25.00 mL溶液,用c mol/L的酸性KMnO4溶液滴定,滴定三次,平均消耗KMnO4溶液体积 v mL。
①滴定时,用_______ (填“酸式”或“碱式”)滴定管盛装KMnO4溶液。
②样品中Fe2+的质量分数为_______ (用含w、c、v的式子表示)。
(1)在试管中加入少量摩尔盐晶体,加水溶解,测得水溶液呈酸性。由此可知
(2)摩尔盐在500℃时隔绝空气加热完全分解,气体产物可能有NH3、SO2、SO3、H2O等。兴趣小组利用下图装置证明摩尔盐分解的气体产物中有SO2和SO3。

①a的名称是
②装置连接顺序为A→
③能证明分解产物中有SO2的实验现象是
④若装置连接顺序不变,能否将装置E中溶液换为BaCl2溶液?理由是
(3)为判断摩尔盐是否变质,可以测定样品中Fe2+的含量。取w g样品溶于水,配制成250 mL溶液。每次取25.00 mL溶液,用c mol/L的酸性KMnO4溶液滴定,滴定三次,平均消耗KMnO4溶液体积 v mL。
①滴定时,用
②样品中Fe2+的质量分数为
您最近一年使用:0次
名校
10 . 某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了下列装置进行实验。
已知:①A中反应为 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;②石灰乳的主要成分为Ca(OH)2,其他杂质不参与反应。
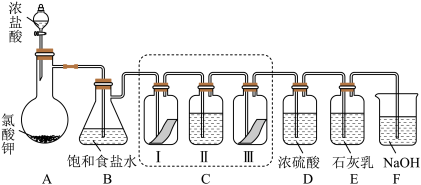
(1)用“双线桥”标出A中反应电子转移的方向和数目_______ 。
(2)B装置作用_______ 。
(3)装置C的目的是验证氯气是否有漂白性,C中I、II、III依次放入的物质正确的是_______ (填编号)。
(4)为测定所得漂白粉的有效成分含量。称取ag漂白粉样品溶解,往所得溶液中通入 CO2至产生沉淀最大值时,该过程的化学方程式为_______ ,若反应生成沉淀的物质的量为bmol,则该漂白粉中有效成份的质量分数为_______ (用含a、b的式子表示)。
已知:①A中反应为 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;②石灰乳的主要成分为Ca(OH)2,其他杂质不参与反应。

(1)用“双线桥”标出A中反应电子转移的方向和数目
(2)B装置作用
(3)装置C的目的是验证氯气是否有漂白性,C中I、II、III依次放入的物质正确的是
| 编号 | I | II | III |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 浓硫酸 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
您最近一年使用:0次



