名校
解题方法
1 . 亚硝酸钠(NaNO2)是一种工业盐,实验室可用如图装置(略去部分夹持仪器)制备。

已知:
① ;
;
② ;
;
③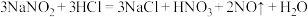 ;
;
④酸性条件下,NO和 都能与
都能与 反应生成
反应生成 和
和 ;
; 能使酸性高锰酸钾溶液褪色。
能使酸性高锰酸钾溶液褪色。
(1)加热装置A前,先通一段时间N2,目的是_______ ;
(2)装置A中发生反应的化学方程式为_______ ;
(3)实验结束后,B瓶溶液中溶质的主要成分是_______ (填化学式)。
(4)仪器C中盛放的药品为_______ (填名称)。
(5)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,_______ ,则产物是NaNO2 (注明试剂、现象)。
(6)装置F的作用是_______ ;
(7)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000molL酸性KMnO4溶液20.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数_______ 。(写出计算过程)

已知:
①
 ;
;②
 ;
;③
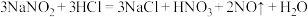 ;
;④酸性条件下,NO和
 都能与
都能与 反应生成
反应生成 和
和 ;
; 能使酸性高锰酸钾溶液褪色。
能使酸性高锰酸钾溶液褪色。(1)加热装置A前,先通一段时间N2,目的是
(2)装置A中发生反应的化学方程式为
(3)实验结束后,B瓶溶液中溶质的主要成分是
(4)仪器C中盛放的药品为
(5)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,
(6)装置F的作用是
(7)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000molL酸性KMnO4溶液20.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数
您最近一年使用:0次
2021-04-28更新
|
449次组卷
|
4卷引用:江苏省常熟市2020-2021学年高一下学期期中化学试题
名校
2 . 以黄铜矿(CuFeS2)、FeCl3和乳酸[CH3CH(OH)COOH]为原料可制备有机合成催化剂CuCl和补铁剂乳酸亚铁{[CH3CH(OH)COO]2Fe}。其主要实验流程如下:_________ 。
(2)向溶液1中加入过量铁粉的目的是_____________ 。
(3)过滤后得到的FeCO3固体应进行洗涤,检验洗涤已完全的方法是___________ 。
(4)实验室制备乳酸亚铁的装置如图1所示。________ 。
②某兴趣小组用KMnO4滴定法测定样品中Fe2+含量进而计算产品中乳酸亚铁的质量分数,结果测得产品的质量分数总是大于100%,其原因可能是______________ 。
(5)已知:①CuCl为白色晶体,难溶于水和乙醇,在空气中易氧化;可与NaCl溶液反应,生成易溶于水的NaCuCl2。
②NaCuCl2可水解生成CuCl,温度、pH对CuCl产率的影响如图2、3所示。______ 。
(实验中须使用的试剂有:饱和NaCl溶液,0.1 mol·L-1 H2SO4、乙醇;除常用仪器外须使用的仪器有:真空干燥箱)。

(2)向溶液1中加入过量铁粉的目的是
(3)过滤后得到的FeCO3固体应进行洗涤,检验洗涤已完全的方法是
(4)实验室制备乳酸亚铁的装置如图1所示。
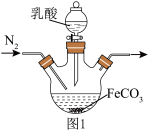
②某兴趣小组用KMnO4滴定法测定样品中Fe2+含量进而计算产品中乳酸亚铁的质量分数,结果测得产品的质量分数总是大于100%,其原因可能是
(5)已知:①CuCl为白色晶体,难溶于水和乙醇,在空气中易氧化;可与NaCl溶液反应,生成易溶于水的NaCuCl2。
②NaCuCl2可水解生成CuCl,温度、pH对CuCl产率的影响如图2、3所示。
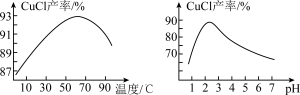
(实验中须使用的试剂有:饱和NaCl溶液,0.1 mol·L-1 H2SO4、乙醇;除常用仪器外须使用的仪器有:真空干燥箱)。
您最近一年使用:0次
2019-03-28更新
|
703次组卷
|
5卷引用:【全国百强校】江苏省启东中学2018-2019学年高二(创新班)下学期期中考试化学试题
解题方法
3 . 高品质MnO2可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料采用“两矿一步浸出法”制备高品质MnO2的某工艺流程如图所示:
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如下:
回答下列问题:
(1)“酸浸”操作中需先后分批加入H2SO4、H2O2。加入H2SO4后发生酸浸过程的主要反应离子方程式为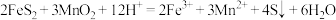 ,
,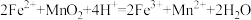 。
。
已知滤渣1的主要成分为S、SiO2、CaSO4等,其附着在矿粉颗粒表面使上述反应受阻,此时加入H2O2,利用其迅速分解产生的大量气泡可破除该不利影响。分析导致H2O2迅速分解的因素是____ 。
(2)加氨水“调pH”时调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为____ (填化学式)。
(3)加NH4F“调pH”时,溶液体系中的Ca2+和Mg2+形成氟化物沉淀。
①若沉淀后上层清液中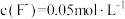 ,则
,则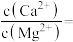
____ 。
②可以用MnF2代替NH4F,以Mg2+为例,结合反应的平衡常数解释能用MnF2除去Mg2+(和Ca2+)的原因是____ 。
(已知:Ksp(MnF2)=5×10-3,Ksp(MgF2)=5×10-11,Ksp(CaF2)=2.5×10-9)
(4)NH4HCO3“调pH”时,发生主要反应的离子方程式为____ 。
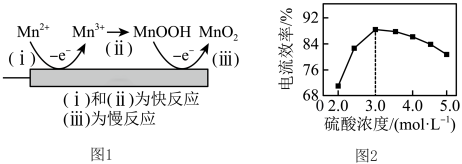
(5)利用惰性电极电解H2SO4—MnSO4—H2O体系获得MnO2的机理(部分)如图1所示,硫酸浓度与电流效率的关系如图2所示。硫酸浓度超过3.0 mol·L−1时,电流效率降低的原因是____ 。 +I2=2I-+
+I2=2I-+ ,计算粗品中MnO2的质量分数
,计算粗品中MnO2的质量分数_______ (写出计算过程)。
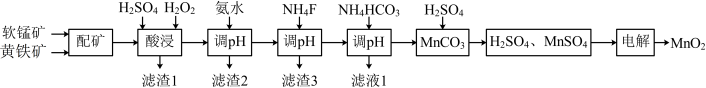
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如下:
| 金属离子 |  |  |  |  |  |
| 开始沉淀pH | 6.9 | 1.9 | 6.6 | 9.1 | 3.4 |
沉淀完全(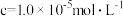 )的pH )的pH | 8.3 | 3.2 | 10.1 | 10.9 | 4.7 |
(1)“酸浸”操作中需先后分批加入H2SO4、H2O2。加入H2SO4后发生酸浸过程的主要反应离子方程式为
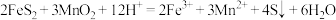 ,
,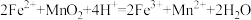 。
。已知滤渣1的主要成分为S、SiO2、CaSO4等,其附着在矿粉颗粒表面使上述反应受阻,此时加入H2O2,利用其迅速分解产生的大量气泡可破除该不利影响。分析导致H2O2迅速分解的因素是
(2)加氨水“调pH”时调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为
(3)加NH4F“调pH”时,溶液体系中的Ca2+和Mg2+形成氟化物沉淀。
①若沉淀后上层清液中
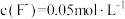 ,则
,则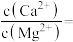
②可以用MnF2代替NH4F,以Mg2+为例,结合反应的平衡常数解释能用MnF2除去Mg2+(和Ca2+)的原因是
(已知:Ksp(MnF2)=5×10-3,Ksp(MgF2)=5×10-11,Ksp(CaF2)=2.5×10-9)
(4)NH4HCO3“调pH”时,发生主要反应的离子方程式为
(5)利用惰性电极电解H2SO4—MnSO4—H2O体系获得MnO2的机理(部分)如图1所示,硫酸浓度与电流效率的关系如图2所示。硫酸浓度超过3.0 mol·L−1时,电流效率降低的原因是
 +I2=2I-+
+I2=2I-+ ,计算粗品中MnO2的质量分数
,计算粗品中MnO2的质量分数
您最近一年使用:0次
名校
4 . 以黄铁矿(主要成分FeS2))为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如下图所示。
(1)煅烧前,黄铁矿需要研磨,目的是___________ 。
(2)煅烧黄铁矿的化学方程式是___________ 。
(3)过程①中处理尾气SO2的离子反应方程式为___________ 。
(4)已知1molSO2(g) 完全转化为1molSO3(g) 放热99kJ,写出SO2催化氧化的热化学方程式___________ 。
(5)因为Na2S2O5在保存过程中易被氧化,导致商品Na2S2O5中存在Na2SO4.欲检验Na2S2O5已变质的实验方法为___________ 。
(6)一般用K2Cr2O7滴定分析法测定还原铁粉的纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的Fe2+。反应方程式为(方程式未配平):
Cr2O72-+Fe2++H+→Cr3++Fe3++H2O。某次实验称取0.2800g样品,滴定时消耗浓度为0.0300mol/L的K2Cr2O7溶液25.00mL,则样品中铁的质量分数为___________ 。(请写出计算过程)

(1)煅烧前,黄铁矿需要研磨,目的是
(2)煅烧黄铁矿的化学方程式是
(3)过程①中处理尾气SO2的离子反应方程式为
(4)已知1molSO2(g) 完全转化为1molSO3(g) 放热99kJ,写出SO2催化氧化的热化学方程式
(5)因为Na2S2O5在保存过程中易被氧化,导致商品Na2S2O5中存在Na2SO4.欲检验Na2S2O5已变质的实验方法为
(6)一般用K2Cr2O7滴定分析法测定还原铁粉的纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准K2Cr2O7溶液滴定其中的Fe2+。反应方程式为(方程式未配平):
Cr2O72-+Fe2++H+→Cr3++Fe3++H2O。某次实验称取0.2800g样品,滴定时消耗浓度为0.0300mol/L的K2Cr2O7溶液25.00mL,则样品中铁的质量分数为
您最近一年使用:0次
5 . 碳酸亚铁(FeCO3)难溶于水,常用于制取铁盐或补血剂。一种FeCO3的制备装置如图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得FeCO3沉淀。______________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:__________________ 。
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程_________ 。
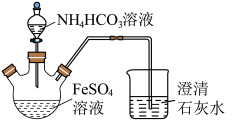
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)FeCO3在潮湿的空气中会转化为Fe(OH)3并进步转化为Fe2O3。写出FeCO3在潮湿的空气中转化为Fe(OH)3的化学方程式:
(4)某FeCO3固体被部分氧化,为测定其中Fe3+的质量分数,现进行如下实验:称取5.000g固体样品,加足量盐酸溶解,将溶液稀释至100mL,量取20.00mL该溶液,加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定,当滴定至终点时消耗Na2S2O3溶液20.00mL。已知实验过程中发生反应如下:2Fe3++2I-=2Fe2++I2,I2+2S2O
 =S4O
=S4O +2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
+2I-。计算FeCO3固体样品中Fe3+的质量分数,写出计算过程
您最近一年使用:0次
名校
解题方法
6 . 碳酸亚铁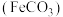 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
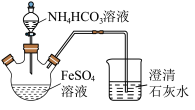
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是___________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3) 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:___________ 。
(4)某 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入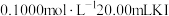 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程___________ 。
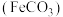 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)
 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:(4)某
 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入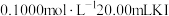 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程
您最近一年使用:0次
名校
解题方法
7 . 氯化亚铜(CuCl)微溶于水,易被氧化,广泛应用于医药等行业。以废铜渣(铜单质的质量分数为64%,CuO的质量分数为8%,其他杂质不含铜元素)为原料,可制备CuCl并获得副产品(NH4)2SO4,流程如图:
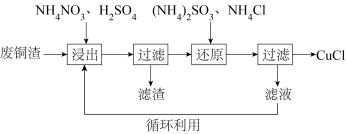
(1)“浸出”时发生的主要反应有:
反应Ⅰ:CuO与H2SO4反应的化学方程式为______ 。
反应Ⅱ:4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O。
①浸出温度为20℃时,铜元素浸出率随时间的变化如图所示。

铜元素浸出率=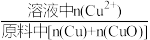 ×100%
×100%
结合图像,从反应速率的角度分析,可得出的结论是______ 。
②实际浸出温度选择65℃,可提高单位时间内铜元素浸出率。若温度过高,会产生红棕色气体,该气体的化学式为______ 。
(2)充分浸出后,“还原”时加入的(NH4)2SO3溶液需略过量,“还原”后的滤液经多次循环可提取一定量的(NH4)2SO4 (忽略转化流程中杂质参与的反应)。
①“还原”时(NH4)2SO4溶液过量的原因是______ 。
②假设铜元素完全浸出,忽略过量的(NH4)2SO4,计算100g废铜渣理论上可制得CuCl与(NH4)2SO4的物质的量(写出计算过程)。______

(1)“浸出”时发生的主要反应有:
反应Ⅰ:CuO与H2SO4反应的化学方程式为
反应Ⅱ:4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O。
①浸出温度为20℃时,铜元素浸出率随时间的变化如图所示。

铜元素浸出率=
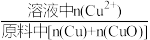 ×100%
×100%结合图像,从反应速率的角度分析,可得出的结论是
②实际浸出温度选择65℃,可提高单位时间内铜元素浸出率。若温度过高,会产生红棕色气体,该气体的化学式为
(2)充分浸出后,“还原”时加入的(NH4)2SO3溶液需略过量,“还原”后的滤液经多次循环可提取一定量的(NH4)2SO4 (忽略转化流程中杂质参与的反应)。
①“还原”时(NH4)2SO4溶液过量的原因是
②假设铜元素完全浸出,忽略过量的(NH4)2SO4,计算100g废铜渣理论上可制得CuCl与(NH4)2SO4的物质的量(写出计算过程)。
您最近一年使用:0次
名校
解题方法
8 . 氯化亚铜(CuCl)微溶于水,易被氧化,广泛应用于医药等行业。以废铜渣(铜单质的质量分数为64%,CuO的质量分数为8%,其他杂质不含铜元素)为原料,可制备CuCl并获得副产品(NH4)2SO4,流程如下:
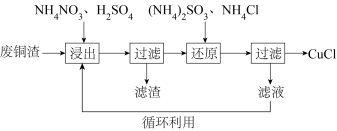
(1)“浸出”时发生的主要反应有:
反应Ⅰ. CuO + H2SO4 = CuSO4 + H2O
反应Ⅱ. 4Cu + NH4NO3 + 5H2SO4 = 4CuSO4 + (NH4)2SO4 + 3H2O
①浸出温度为20℃时,铜元素浸出率随时间的变化如图所示。铜元素浸出率 =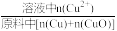 ×100%
×100%

结合图像,从反应速率的角度分析,可得出的结论是_______ 。
②实际浸出温度选择65℃,可提高单位时间内铜元素浸出率。若温度过高,会产生红棕色气体,该气体的化学式为_______ 。
(2)充分浸出后,“还原”时加入的(NH4)2SO3溶液需略过量,“还原”后的滤液经多次循环可提取一定量的(NH4)2SO4(忽略转化流程中杂质参与的反应)。
①“还原”时(NH4)2SO3溶液过量的原因是_______ (写出两点)。
②假设铜元素完全浸出,忽略过量的(NH4)2SO3,计算100 g废铜渣理论上可制得CuCl与(NH4)2SO4的物质的量______ (写出计算过程)。

(1)“浸出”时发生的主要反应有:
反应Ⅰ. CuO + H2SO4 = CuSO4 + H2O
反应Ⅱ. 4Cu + NH4NO3 + 5H2SO4 = 4CuSO4 + (NH4)2SO4 + 3H2O
①浸出温度为20℃时,铜元素浸出率随时间的变化如图所示。铜元素浸出率 =
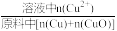 ×100%
×100%
结合图像,从反应速率的角度分析,可得出的结论是
②实际浸出温度选择65℃,可提高单位时间内铜元素浸出率。若温度过高,会产生红棕色气体,该气体的化学式为
(2)充分浸出后,“还原”时加入的(NH4)2SO3溶液需略过量,“还原”后的滤液经多次循环可提取一定量的(NH4)2SO4(忽略转化流程中杂质参与的反应)。
①“还原”时(NH4)2SO3溶液过量的原因是
②假设铜元素完全浸出,忽略过量的(NH4)2SO3,计算100 g废铜渣理论上可制得CuCl与(NH4)2SO4的物质的量
您最近一年使用:0次
2023-04-19更新
|
579次组卷
|
3卷引用:江苏省盐城市响水中学2023-2024学年高二上学期期中考试化学(必修)试题
江苏省盐城市响水中学2023-2024学年高二上学期期中考试化学(必修)试题江苏省2023年普通高中学业水平合格性考试化学试题(已下线)题型三 工艺流程中的答题规范-备战2024年高考化学答题技巧与模板构建
名校
解题方法
9 . 含氯消毒剂可有效灭活新冠病毒,为阻断疫情做出了巨大贡献。
(1)人类最初用新制氯水漂白、杀菌、消毒。氯水使用起来不方便,效果也不理想的原因是_______ 。
(2)常用的含氯漂白剂中二氧化氯( )被联合国世界卫生组织(WHO)列为AⅠ级安全消毒剂,是一种易溶于水、难溶于有机溶剂的气体,易与碱液反应生成盐和水。其性质非常不稳定,温度过高或水溶液中
)被联合国世界卫生组织(WHO)列为AⅠ级安全消毒剂,是一种易溶于水、难溶于有机溶剂的气体,易与碱液反应生成盐和水。其性质非常不稳定,温度过高或水溶液中 的质量分数高于30%等均有可能引起爆炸,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低。实验室可用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如下图所示。
的质量分数高于30%等均有可能引起爆炸,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低。实验室可用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如下图所示。
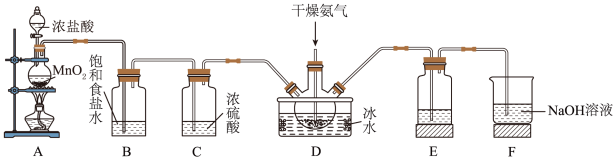
①装置A中用来存放、添加浓盐酸的仪器名称是_______ ;写出A中发生反应的化学方程式并用单线桥法标出电子转移的方向和数目:_______ 。
②装置C的作用为_______ 。
③装置D中从实验开始到结束都要持续通入干燥氮气,其可能的原因是_______ ;写出D中发生反应的化学方程式:_______ 。
④装置E将产生的二氧化氯气体进行溶解、吸收、保存,吸收液最好使用_______ (填字母序号)。
a.80℃的温水 b.冰水 c.四氯化碳 d.NaOH溶液
(1)人类最初用新制氯水漂白、杀菌、消毒。氯水使用起来不方便,效果也不理想的原因是
(2)常用的含氯漂白剂中二氧化氯(
 )被联合国世界卫生组织(WHO)列为AⅠ级安全消毒剂,是一种易溶于水、难溶于有机溶剂的气体,易与碱液反应生成盐和水。其性质非常不稳定,温度过高或水溶液中
)被联合国世界卫生组织(WHO)列为AⅠ级安全消毒剂,是一种易溶于水、难溶于有机溶剂的气体,易与碱液反应生成盐和水。其性质非常不稳定,温度过高或水溶液中 的质量分数高于30%等均有可能引起爆炸,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低。实验室可用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如下图所示。
的质量分数高于30%等均有可能引起爆炸,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低。实验室可用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如下图所示。
①装置A中用来存放、添加浓盐酸的仪器名称是
②装置C的作用为
③装置D中从实验开始到结束都要持续通入干燥氮气,其可能的原因是
④装置E将产生的二氧化氯气体进行溶解、吸收、保存,吸收液最好使用
a.80℃的温水 b.冰水 c.四氯化碳 d.NaOH溶液
您最近一年使用:0次
名校
解题方法
10 . 亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室用如下图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。

(1)装置A利用Na2SO3和硫酸制取SO2,导管b的作用是___________ 。
(2)装置B中浓HNO3与SO2在浓H2SO4作用下化合制得NOSO4H,该反应为放热反应。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以采取的操作是______ 。
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是______ 。
(3)该实验装置存在可能导致NOSO4H产量降低的缺陷是___________ 。
(4)测定亚硝酰硫酸NOSO4H的纯度。
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol/L、60.00mL的KMnO4溶液和10mL25%H2SO4溶液,摇匀。然后将0.2500mol/L草酸钠(Na2C2O4)溶液滴入碘量瓶中,消耗草酸钠溶液的体积为20.00mL。
已知:
①配平下面的方程式:___________ 。
_______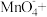 _______
_______ _______
_______ ______
______
 ______
______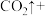 ______
______
②亚硝酰硫酸的质量分数=___________ 。(精确到0.1%)(写出计算过程)

(1)装置A利用Na2SO3和硫酸制取SO2,导管b的作用是
(2)装置B中浓HNO3与SO2在浓H2SO4作用下化合制得NOSO4H,该反应为放热反应。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以采取的操作是
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是
(3)该实验装置存在可能导致NOSO4H产量降低的缺陷是
(4)测定亚硝酰硫酸NOSO4H的纯度。
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol/L、60.00mL的KMnO4溶液和10mL25%H2SO4溶液,摇匀。然后将0.2500mol/L草酸钠(Na2C2O4)溶液滴入碘量瓶中,消耗草酸钠溶液的体积为20.00mL。
已知:

①配平下面的方程式:
_______
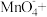 _______
_______ _______
_______ ______
______
 ______
______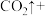 ______
______
②亚硝酰硫酸的质量分数=
您最近一年使用:0次
2023-04-10更新
|
458次组卷
|
2卷引用:江苏省苏州中学2022-2023学年高一下学期期中考试化学试题



