1 .  的转化是资源利用和环境保护的重要研究课题。
的转化是资源利用和环境保护的重要研究课题。
(1)通过电化学循环法可将 转化为
转化为 和
和 (如图所示)。其中氧化过程发生如下两步反应:
(如图所示)。其中氧化过程发生如下两步反应: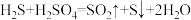 、
、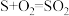 。
。
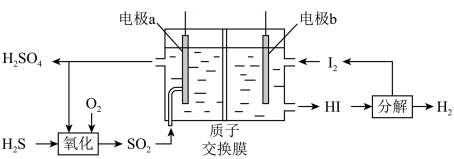
①电极a上发生反应的电极反应式为_______ 。
②理论上1mol 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为_______ 。
(2) 可用作脱除
可用作脱除 气体的脱硫剂。以赤铁矿渣(主要成分为
气体的脱硫剂。以赤铁矿渣(主要成分为 、
、 和少量
和少量 )为原料制备
)为原料制备 晶体,已知
晶体,已知 易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣,
易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣,_______ ,向滤液中加乙醇,在恒温水浴槽中冷却结晶,过滤,用丙酮洗涤,干燥。(已知该实验中pH=3.5时, 沉淀完全;pH=4.1时,
沉淀完全;pH=4.1时, 开始沉淀。实验中必须使用的试剂:1.0
开始沉淀。实验中必须使用的试剂:1.0
 、1.0
、1.0 NaOH、铁粉。)
NaOH、铁粉。)
 的转化是资源利用和环境保护的重要研究课题。
的转化是资源利用和环境保护的重要研究课题。(1)通过电化学循环法可将
 转化为
转化为 和
和 (如图所示)。其中氧化过程发生如下两步反应:
(如图所示)。其中氧化过程发生如下两步反应: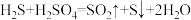 、
、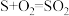 。
。
①电极a上发生反应的电极反应式为
②理论上1mol
 参加反应可产生
参加反应可产生 的物质的量为
的物质的量为(2)
 可用作脱除
可用作脱除 气体的脱硫剂。以赤铁矿渣(主要成分为
气体的脱硫剂。以赤铁矿渣(主要成分为 、
、 和少量
和少量 )为原料制备
)为原料制备 晶体,已知
晶体,已知 易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣,
易溶于水难溶于乙醇,请补充完整相应的实验方案:取一定量的赤铁矿渣, 沉淀完全;pH=4.1时,
沉淀完全;pH=4.1时, 开始沉淀。实验中必须使用的试剂:1.0
开始沉淀。实验中必须使用的试剂:1.0
 、1.0
、1.0 NaOH、铁粉。)
NaOH、铁粉。)
您最近一年使用:0次
解题方法
2 . 二氧化氯(ClO2)是一种高效的灭菌消毒剂,受热或浓度过大时易发生分解甚至爆炸。工业上常将ClO2制备成NaClO2固体以便运输和贮存,流程如下:
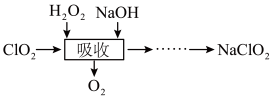
(1)“吸收”过程中发生反应的离子方程式是_______ 。
(2)“吸收”过程,温度控制在25℃的目的是_______ (填字母)。
a.保持适当的反应速率 b.促进H2O2分解 c.防止温度过高引起爆炸
(3)NaClO2的溶解度曲线如图所示,由NaClO2溶液得到无水NaClO2的操作如下:

①减压,55℃蒸发结晶;
②_______ ;
③38℃~60℃热水洗涤;
④低于60℃干燥。

(1)“吸收”过程中发生反应的离子方程式是
(2)“吸收”过程,温度控制在25℃的目的是
a.保持适当的反应速率 b.促进H2O2分解 c.防止温度过高引起爆炸
(3)NaClO2的溶解度曲线如图所示,由NaClO2溶液得到无水NaClO2的操作如下:

①减压,55℃蒸发结晶;
②
③38℃~60℃热水洗涤;
④低于60℃干燥。
您最近一年使用:0次
3 . 铁酸H2FeO4是一种多功能、高效无毒的新型绿色水处理剂,投入水中会迅速发生反应。
(1)H2FeO4中Fe的化合价为________ 。
(2)已知:常温下高铁酸为紫黑色固体,将H2FeO4投入水中,有气体生成,同时有红褐色沉淀产生,则H2FeO4与水反应的化学方程式为________ 。
(3)在工业上制备H2FeO4的方法有多种。
Ⅰ.干法制备的反应原理如下:2FeSO4+6Na2O2=aNa2FeO4+bM↑+2Na2O+2Na2SO4
①b=________ 。
②每生成1molM,该反应转移电子的物质的量为________ mol。
Ⅱ.湿法制备的工艺流程如下;
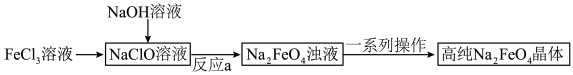
已知:H2FeO4在强碱性溶液中的溶解度较小,高温易分解。
③反应a中,生成物除了H2FeO4外,另一种盐的化学式为________ 。
④一系列操作包括过滤、________ 、________ 。
(1)H2FeO4中Fe的化合价为
(2)已知:常温下高铁酸为紫黑色固体,将H2FeO4投入水中,有气体生成,同时有红褐色沉淀产生,则H2FeO4与水反应的化学方程式为
(3)在工业上制备H2FeO4的方法有多种。
Ⅰ.干法制备的反应原理如下:2FeSO4+6Na2O2=aNa2FeO4+bM↑+2Na2O+2Na2SO4
①b=
②每生成1molM,该反应转移电子的物质的量为
Ⅱ.湿法制备的工艺流程如下;
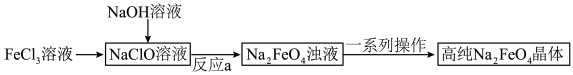
已知:H2FeO4在强碱性溶液中的溶解度较小,高温易分解。
③反应a中,生成物除了H2FeO4外,另一种盐的化学式为
④一系列操作包括过滤、
您最近一年使用:0次
11-12高二下·安徽六安·课时练习
名校
4 . 工业制备氯化铜时,将浓盐酸用蒸气加热至80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌,使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液,采用以下步骤:
参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3。
请回答以下问题:
(1)第一步除去Fe2+,能否直接调整pH=9.6,将Fe2+沉淀除去?___ ,理由是___ 。
(2)有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是____ 。(填序号)
A.一定增大 B.一定减小 C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?___ ,理由是___ 。
③现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有___ (多选)。
A.浓HNO3 B.KMnO4 C.Cl2 D.O2 E.H2O2
(3)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有___ (多选)。
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3 E.CuO F.Cu(OH)2
参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3。
请回答以下问题:
(1)第一步除去Fe2+,能否直接调整pH=9.6,将Fe2+沉淀除去?
(2)有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是
A.一定增大 B.一定减小 C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?
③现有下列几种常用的氧化剂,可用于除去混合溶液中Fe2+的有
A.浓HNO3 B.KMnO4 C.Cl2 D.O2 E.H2O2
(3)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3 E.CuO F.Cu(OH)2
您最近一年使用:0次
2019-11-06更新
|
349次组卷
|
6卷引用:江苏省南京师大苏州实验学校2019-2020学年高二9月月考化学试题
江苏省南京师大苏州实验学校2019-2020学年高二9月月考化学试题(已下线)2011-2012学年安徽省舒城晓天中学高二下学期质量测试5化学试卷(已下线)2014年高中化学苏教版选修四专题3 溶液中的离子反应练习卷福建省宁德市2017-2018学年高二上学期期末模拟质量检测化学试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题甘肃省古浪县第二中学2019-2020学年高二12月基础知识竞赛化学试题



