名校
1 . 有机合成是有机化学的重要组成部分,如图是关于气体A制备和性质的合成路线图。已知C是一种塑料,D是一种植物生长调节剂,可以催熟果实。
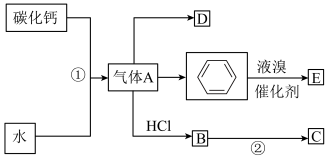
(1)①的化学方程式为______ 。
(2)②的化学方程式为______ ,该反应属于______ 反应(填反应类型)。
(3)D中的官能团为______ (填名称),写出实验室制D的化学方程式为______ ,该反应属于______ 反应(填反应类型)。
(4)与链烃相比,苯的化学性质的主要特征是 (单选)。
(5)证明苯制备E为取代反应的实验方案是______ 。已知硝基为间位定位基团,溴原子为邻、对位定位基团,写出以苯原料,制各间溴硝基苯的合成路线_____ 。
(合成路线的表示方式为:甲 乙
乙 目标产物)
目标产物)
(6)与上述物质有关的化学实验的说法中,正确的是 (单选)。

(1)①的化学方程式为
(2)②的化学方程式为
(3)D中的官能团为
(4)与链烃相比,苯的化学性质的主要特征是 (单选)。
| A.难氧化、难取代、难加成 | B.易氧化、易取代、易加成 |
| C.难氧化、能加成、易取代 | D.易氧化、易加成、难取代 |
(合成路线的表示方式为:甲
 乙
乙 目标产物)
目标产物)(6)与上述物质有关的化学实验的说法中,正确的是 (单选)。
| A.实验室制备乙烯时,产生的气体使溴水褪色,能证明有乙烯生成 |
| B.除去溴苯中的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液 |
| C.实验室制乙炔,反应物为固体和液体,且常温条件下反应,可以用启普发生器 |
| D.制取硝基苯时,试管中先加入浓H2SO4,再逐滴滴入浓HNO3和苯 |
您最近一年使用:0次
名校
2 . 某化学兴趣小组查阅文献资料了解到湿法合成高铁酸钾(K2FeO4)是目前人工成本最低、产品纯度最高的合成方法,其合成路线如图:
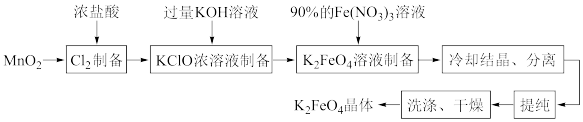
该兴趣小组根据文献资料设计了如图所示装置(部分夹持仪器已省略)制取K2FeO4。
已知:K2FeO4为紫色固体,具有强氧化性;在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。
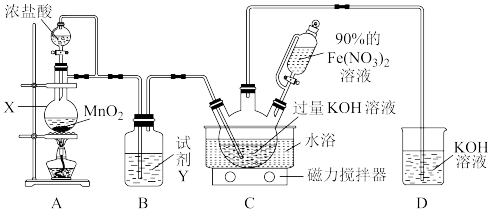
(1)仪器X的名称是_______ 。试剂Y的作用为_______ 。
(2)水浴方式是_______ (填“冷水浴”或“热水浴”)。
(3)装置C中KOH过量的原因是_______ 。
(4)上述流程中,“提纯”所用的方法是_______ 。
(5)称取1.98 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,并加入1 mL苯二胺磺酸钠作指示剂,用1.00 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,消耗(NH4)2Fe(SO4)2溶液5.76 mL。测定过程中发生反应:
a. Cr(OH) +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-
b. 2CrO +2H+=Cr2O
+2H+=Cr2O +H2O
+H2O
c. Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
则K2FeO4样品的纯度是_______ 。
(6)K2FeO4是一种新型、高效、多功能水处理剂,既能杀菌消毒,又能净化水中悬浮杂质,请解释K2FeO4作为多功能水处理剂的原理:_______ 。
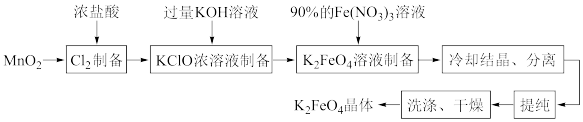
该兴趣小组根据文献资料设计了如图所示装置(部分夹持仪器已省略)制取K2FeO4。
已知:K2FeO4为紫色固体,具有强氧化性;在酸性或中性溶液中快速产生O2,在0℃~5℃、强碱性溶液中较稳定。

(1)仪器X的名称是
(2)水浴方式是
(3)装置C中KOH过量的原因是
(4)上述流程中,“提纯”所用的方法是
(5)称取1.98 g高铁酸钾样品,完全溶解于浓KOH溶液中,再加入足量亚铬酸钾{K[Cr(OH)4]}反应后配成100.00 mL溶液;取上述溶液20.00 mL于锥形瓶中,加入稀硫酸调至pH=2,并加入1 mL苯二胺磺酸钠作指示剂,用1.00 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,消耗(NH4)2Fe(SO4)2溶液5.76 mL。测定过程中发生反应:
a. Cr(OH)
 +FeO
+FeO =Fe(OH)3+CrO
=Fe(OH)3+CrO +OH-
+OH-b. 2CrO
 +2H+=Cr2O
+2H+=Cr2O +H2O
+H2Oc. Cr2O
 +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O则K2FeO4样品的纯度是
(6)K2FeO4是一种新型、高效、多功能水处理剂,既能杀菌消毒,又能净化水中悬浮杂质,请解释K2FeO4作为多功能水处理剂的原理:
您最近一年使用:0次
2022-01-12更新
|
158次组卷
|
4卷引用:福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题
福建省泉州市永春第一中学2022-2023学年高二下学期6月期末考试化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(工业流程题)(已下线)工业流程题吉林省长春吉大附中实验学校2021-2022学年高三上学期第三次摸底考试化学试题
解题方法
3 . 苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一、下面是它的一种实验室合成路线:
 +2H2O+H2SO4
+2H2O+H2SO4
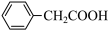 +NH4HSO4
+NH4HSO4
2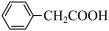 +Cu(OH)2→(
+Cu(OH)2→(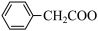 )2Cu+2H2O
)2Cu+2H2O
如图为制备苯乙酸的装置示意图(加热和夹持装置等略):已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
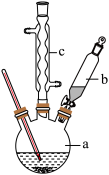
回答下列问题:
(1)在 三口瓶a中加入
三口瓶a中加入 硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是___________ 。
(2)将a中的溶液加热至 ,缓缓滴加
,缓缓滴加 苯乙腈到硫酸溶液中然后升温至
苯乙腈到硫酸溶液中然后升温至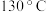 充分反应。在装置中,仪器b的作用是
充分反应。在装置中,仪器b的作用是___________ ;仪器c的名称是___________ ,其作用是___________ 。
(3)反应结束后加适量冷水,再分离出苯乙酸粗品。下列仪器中可用于分离苯乙酸粗品的是___________ (填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(4)提纯粗苯乙酸的具体操作步骤是___________ 、冷却结晶、过滤、洗涤、干燥。最终得到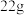 纯品,则苯乙酸的产率是
纯品,则苯乙酸的产率是___________ (保留三位有效数字)
(5)用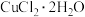 和
和 溶液制备适量
溶液制备适量 沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是___________ 。
(6)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________ 。
 +2H2O+H2SO4
+2H2O+H2SO4
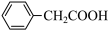 +NH4HSO4
+NH4HSO42
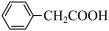 +Cu(OH)2→(
+Cu(OH)2→(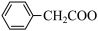 )2Cu+2H2O
)2Cu+2H2O如图为制备苯乙酸的装置示意图(加热和夹持装置等略):已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。

回答下列问题:
(1)在
 三口瓶a中加入
三口瓶a中加入 硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是(2)将a中的溶液加热至
 ,缓缓滴加
,缓缓滴加 苯乙腈到硫酸溶液中然后升温至
苯乙腈到硫酸溶液中然后升温至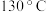 充分反应。在装置中,仪器b的作用是
充分反应。在装置中,仪器b的作用是(3)反应结束后加适量冷水,再分离出苯乙酸粗品。下列仪器中可用于分离苯乙酸粗品的是
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(4)提纯粗苯乙酸的具体操作步骤是
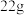 纯品,则苯乙酸的产率是
纯品,则苯乙酸的产率是(5)用
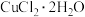 和
和 溶液制备适量
溶液制备适量 沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是(6)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入
 搅拌
搅拌 ,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
4 . 苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
 + H2O+H2SO4
+ H2O+H2SO4
 +NH4HSO4
+NH4HSO4
 +Cu(OH)2→(
+Cu(OH)2→( )2Cu+H2O
)2Cu+H2O
制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
__________________________ 。
(2)将a中的溶液加热至100℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。在装置中,仪器b的作用是_____________________ ;仪器c的名称是______________ ,其作用是___________________________________________ 。
反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是____________ 。下列仪器中可用于分离苯乙酸粗品的是________________ (填标号)。
(3)提纯粗苯乙酸的方法是_____________ ,最终得到44 g纯品,则苯乙酸的产率是________ 。
(4)用CuCl2• 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是____________________________________________ 。
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是___________________ 。
 + H2O+H2SO4
+ H2O+H2SO4
 +NH4HSO4
+NH4HSO4 +Cu(OH)2→(
+Cu(OH)2→( )2Cu+H2O
)2Cu+H2O制备苯乙酸的装置示意图如下(加热和夹持装置等略):

已知:苯乙酸的熔点为76.5℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130℃继续反应。在装置中,仪器b的作用是
反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是
| A.分液漏斗 | B.漏斗 | C.烧杯 | D.直形冷凝管E.玻璃棒 |
(3)提纯粗苯乙酸的方法是
(4)用CuCl2• 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是
(5)将苯乙酸加入到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是
您最近一年使用:0次
2019-01-30更新
|
3820次组卷
|
18卷引用:湖北省武汉中学2022-2023学年高二下学期5月月考化学试题
湖北省武汉中学2022-2023学年高二下学期5月月考化学试题2015-2016学年陕西西安铁一中学高二下开学考试化学试卷2015-2016学年山西省怀仁一中高二下第二次月考化学试卷2014-2015学年湖南省双峰一中高二下期中理科化学试卷广西南宁市第三中学2019-2020学年高二上学期期中考试化学(理)试题第三章 烃的含氧衍生物——B 拓展区 综合拓展(人教版选修5)重庆市主城区七校2019-2020学年高二下学期期末联考化学试题黑龙江省哈尔滨市哈师大附中2020-2021学年高二下学期期中考试化学试题(已下线)第一章 有机化合物的结构特点与研究方法 章末测试(A)-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修3)福建省莆田第一中学2021-2022学年高二上学期期中考试化学试题甘肃省永昌县第一高级中学2021-2022学年高二下学期期末考试化学试题2014年全国普通高等学校招生统一考试理科综合能力测试化学(全国大纲卷)(已下线)2013-2014江西省临川一中高一下学期期末考试化学试卷(已下线)2013-2014学年江西省临川一中高一(下)期末考试化学试卷2016届黑龙江省哈尔滨三中高三上第三次检测理综化学试卷会做实验2020届高三化学实验复习——过滤、蒸馏、冷凝、洗气装置的创新应用【选择15+有机工艺10题突破】(已下线)解密12 实验化学(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密13 实验化学(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)
解题方法
5 . 阿司匹林(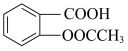 )是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:
)是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:
①取反应物:取适量水杨酸、醋酸酐、浓硫酸加入反应容器,混合摇匀;
②合成:控制温度为85°C ~90°C加热10分钟后,冷却反应液、过滤、洗涤得粗产品;
③提纯。
已知:
请根据以上信息回答下列问题:
(1)取反应物前应先向反应容器中加入_______ 。
(2)合成应在_______ (填“无水”或“有水”)条件下进行,最合适的加热方法是_______ 。
(3)冷却反应液后,发现无晶体析出,此时可采取的措施是_______ 。
(4)I.提纯时,先加入少量的NaHCO3溶液后过滤,再向固体中加盐酸酸化,冷却、过滤、洗涤、干燥后得到较纯的阿司匹林。判断洗涤干净的方法是_______ 。
II.另一种提纯方法是将粗产品与乙酸乙酯、沸石混合后加热回流,趁热过滤、冷却过滤、洗涤干燥。其中回流的装置如图所示:

①使用温度计的目的是_______ 。
②乙酸乙酯的作用是_______ ,该方法所得产品中有机杂质要比方案I少,原因是_______ 。
 )是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:
)是被广泛应用的解热镇痛和抗凝药。在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O] 为主要原料合成阿司匹林,设计如下实验步骤:①取反应物:取适量水杨酸、醋酸酐、浓硫酸加入反应容器,混合摇匀;
②合成:控制温度为85°C ~90°C加热10分钟后,冷却反应液、过滤、洗涤得粗产品;
③提纯。
已知:
| 名称 | 相对分子质量 | 相关性质 |
| 水杨酸 | 138 | 熔点15°C,微溶于水 |
| 醋酸酐 | 102 | 沸点139.4°C,与水激烈反应生成醋酸 |
| 乙酰水杨酸 | 180 | 熔点135°C,128~ 135°C分解,微溶于水 |
(1)取反应物前应先向反应容器中加入
(2)合成应在
(3)冷却反应液后,发现无晶体析出,此时可采取的措施是
(4)I.提纯时,先加入少量的NaHCO3溶液后过滤,再向固体中加盐酸酸化,冷却、过滤、洗涤、干燥后得到较纯的阿司匹林。判断洗涤干净的方法是
II.另一种提纯方法是将粗产品与乙酸乙酯、沸石混合后加热回流,趁热过滤、冷却过滤、洗涤干燥。其中回流的装置如图所示:

①使用温度计的目的是
②乙酸乙酯的作用是
您最近一年使用:0次
2023-05-03更新
|
1004次组卷
|
5卷引用:第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)
(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)云南省“3+3+3”2023届高三下学期诊断性联考二模理综化学试题(已下线)考点巩固卷13 化学实验基础(二)(3个考点30题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)第33讲认识有机化合物(已下线)考点1 认识有机化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
解题方法
6 . 乙酰苯胺是合成磺胺类药物的重要原料,也可用作止痛剂,退热剂和防腐剂。某化学兴趣小组在实验室中制备并提纯乙酰苯胺的过程如下。
已知:①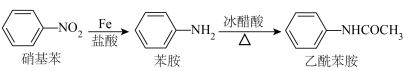
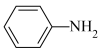 +CH3COOH
+CH3COOH
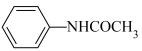 +H2O
+H2O
②有机物相关数据
I.制备并提纯苯胺
先还原硝基苯制备苯胺,所得苯胺粗产品中混有少量互溶的硝基苯杂质,提纯过程如下:

(1)苯胺与盐酸反应生成可溶于水的盐的化学方程式为___________ 。
(2)操作1与操作2相同,需要用到的主要玻璃仪器有___________ 、烧杯。
(3)无水硫酸钠固体的作用是___________ 。
Ⅱ.制备乙酰苯胺
在圆底烧瓶中加入9.3g苯胺,足量冰醋酸及少量锌粉,组装好仪器,维持圆底烧瓶中反应温度在100~110℃之间,反应一段时间后,在搅拌下趁热将圆底烧瓶中的混合物倒入冰水中,抽滤、洗涤、烘干得到乙酰苯胺粗产品。
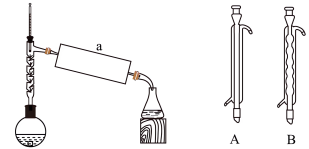
(4)a处应选择仪器___________ (填“A”或“B”),其名称为___________ 。
(5)结合反应原理,从化学平衡角度分析,使用蒸馏装置的原因是___________ 。
(6)加入少量锌粉的作用是___________ 。
Ⅲ.乙酰苯胺粗产品提纯
(7)将制得的乙酰苯胺粗产品放入烧杯中,加入适量蒸馏水,加热,搅拌,使粗产品完全溶解。加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,___________ (填操作名称)。待所得滤液完全冷却后滤出晶体,经洗涤、干燥、称量,得到产品8.7g。该实验中乙酰苯胺的产率为___________ (保留三位有效数字)。
已知:①

 +CH3COOH
+CH3COOH
 +H2O
+H2O②有机物相关数据
| 名称 | 相对分子质量 | 常温下性状 | 主要性质 |
| 硝基苯 | 123 | 无色或微黄色,具有苦杏仁味的油状液体 | 难溶于水,易溶于有机溶剂 |
| 苯胺 | 93 | 无色油状液体 | 有碱性和还原性,在空气中易被氧化,微溶于水,易溶于乙醇和乙醚 |
| 乙酰苯胺 | 135 | 白色晶体 | 微溶于冷水,溶于沸水,溶于有机溶剂 |
先还原硝基苯制备苯胺,所得苯胺粗产品中混有少量互溶的硝基苯杂质,提纯过程如下:

(1)苯胺与盐酸反应生成可溶于水的盐的化学方程式为
(2)操作1与操作2相同,需要用到的主要玻璃仪器有
(3)无水硫酸钠固体的作用是
Ⅱ.制备乙酰苯胺
在圆底烧瓶中加入9.3g苯胺,足量冰醋酸及少量锌粉,组装好仪器,维持圆底烧瓶中反应温度在100~110℃之间,反应一段时间后,在搅拌下趁热将圆底烧瓶中的混合物倒入冰水中,抽滤、洗涤、烘干得到乙酰苯胺粗产品。

(4)a处应选择仪器
(5)结合反应原理,从化学平衡角度分析,使用蒸馏装置的原因是
(6)加入少量锌粉的作用是
Ⅲ.乙酰苯胺粗产品提纯
(7)将制得的乙酰苯胺粗产品放入烧杯中,加入适量蒸馏水,加热,搅拌,使粗产品完全溶解。加入少量活性炭吸附色素等杂质,在搅拌下微沸5min,
您最近一年使用:0次
解题方法
7 . 磷酸铁 是合成锂电池正极材料磷酸铁锂的前驱体,工业上以废铁屑为原料经过如下步骤制备
是合成锂电池正极材料磷酸铁锂的前驱体,工业上以废铁屑为原料经过如下步骤制备 。
。
步骤i:洗涤——分别用X、水洗涤;
步骤ii:酸浸——用稀硫酸溶解;
步骤iii:氧化——用双氧水氧化;
步骤iv:沉铁——用 溶液沉淀
溶液沉淀 ;
;
步骤v:分离——过滤、洗涤、干燥,最后得到 。
。
(1)洗涤是为了除去废铁屑表面的油污,则X通常是热的___________ 溶液(填化学式)。
(2)酸浸时发生的反应除了 、
、 外,还可能有
外,还可能有___________ (写离子方程式)。
(3)检验 全部被氧化的实验方法是
全部被氧化的实验方法是___________ 。
(4)沉铁时有 沉淀和
沉淀和 生成,则该反应的离子方程式为
生成,则该反应的离子方程式为___________ 。
(5)研究发现,不同 对
对 沉淀的影响如表所示:
沉淀的影响如表所示:
当 时随
时随 的增加,
的增加, 的沉淀率开始下降,而
的沉淀率开始下降,而 沉淀率未下降,其原因可能为
沉淀率未下降,其原因可能为____ 。
 是合成锂电池正极材料磷酸铁锂的前驱体,工业上以废铁屑为原料经过如下步骤制备
是合成锂电池正极材料磷酸铁锂的前驱体,工业上以废铁屑为原料经过如下步骤制备 。
。步骤i:洗涤——分别用X、水洗涤;
步骤ii:酸浸——用稀硫酸溶解;
步骤iii:氧化——用双氧水氧化;
步骤iv:沉铁——用
 溶液沉淀
溶液沉淀 ;
;步骤v:分离——过滤、洗涤、干燥,最后得到
 。
。(1)洗涤是为了除去废铁屑表面的油污,则X通常是热的
(2)酸浸时发生的反应除了
 、
、 外,还可能有
外,还可能有(3)检验
 全部被氧化的实验方法是
全部被氧化的实验方法是(4)沉铁时有
 沉淀和
沉淀和 生成,则该反应的离子方程式为
生成,则该反应的离子方程式为(5)研究发现,不同
 对
对 沉淀的影响如表所示:
沉淀的影响如表所示: | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | |
| 沉降率/% |  | 90.0 | 94.6 | 97.9 | 99.2 | 95.3 |
 | 88.1 | 95.4 | 97.2 | 98.5 | 99.8 | |
当
 时随
时随 的增加,
的增加, 的沉淀率开始下降,而
的沉淀率开始下降,而 沉淀率未下降,其原因可能为
沉淀率未下降,其原因可能为
您最近一年使用:0次
名校
解题方法
8 . 甲基丙烯酸甲酯是合成有机玻璃的单体,有关物质的性质如下:
某小组拟制备甲基丙烯酸甲酯并探究其性质,装置如图所示(夹持及加热仪器略)。

向三颈瓶中依次加入20 mL甲醇、5 mL浓硫酸、30 mL甲基丙烯酸及沸石少许,充分搅拌,加热。
(1)向其中加入沸石的目的是___________ 。
(2)使用油水分离器的作用是___________ 。
(3)实验结束后,提纯产品的流程如下:
混合液 产品
产品
①水洗2的目的是___________ 。
②加入硫酸钠粉末的作用是___________ 。
③蒸馏操作中收集产品的温度约为___________ 。
(4)设计简单实验检验产品中含碳碳双键:___________ 。
(5)甲基丙烯酸甲酯另一种合成方法为 ,已知该反应的原子利用率为100%,则A的结构简式为
,已知该反应的原子利用率为100%,则A的结构简式为___________ 。
| 物质 | 沸点/℃ | 溶解性 |
| 甲醇 | 64.7 | 易溶于水和有机溶剂 |
甲基丙烯酸 | 161 | 溶于水,易溶于有机溶剂 |
| 甲基丙烯酸甲酯 | 100 | 易溶于有机溶剂,微溶于水 |

向三颈瓶中依次加入20 mL甲醇、5 mL浓硫酸、30 mL甲基丙烯酸及沸石少许,充分搅拌,加热。
(1)向其中加入沸石的目的是
(2)使用油水分离器的作用是
(3)实验结束后,提纯产品的流程如下:
混合液
 产品
产品①水洗2的目的是
②加入硫酸钠粉末的作用是
③蒸馏操作中收集产品的温度约为
(4)设计简单实验检验产品中含碳碳双键:
(5)甲基丙烯酸甲酯另一种合成方法为
 ,已知该反应的原子利用率为100%,则A的结构简式为
,已知该反应的原子利用率为100%,则A的结构简式为
您最近一年使用:0次
名校
9 . 氨基甲酸铵(NH2COONH4)是一种重要的医用氨化剂,有关该物质的信息如下表所示:
某实验小组在实验室中利用下列装置合成少量的氨基甲酸铵。回答下列问题:
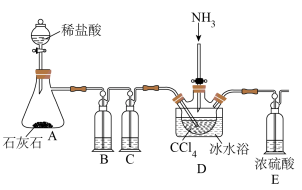
(1)盛放稀盐酸的仪器的名称是___________ 。
(2)装置B和C中试剂的名称分别是___________ 、___________ 。
(3)实验室制取氨气的化学方程式为___________ 。
(4)反应结束后,从三颈烧瓶中分离出产品,进行的实验操作是___________ 。
(5)装置E的作用有___________ (写出两点)。若观察到E中出现大量气泡(浓硫酸足量),则可能的原因是___________ 。
(6)设计实验:检验制得的产品中是否混有 ?
?___________ 。
| 制备原理 | 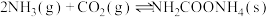 放热反应 放热反应 |
| 主要性质 | ①在潮湿的空气中转变为 ②温度较高时容易分解生成  、 、 ③不溶于  |

(1)盛放稀盐酸的仪器的名称是
(2)装置B和C中试剂的名称分别是
(3)实验室制取氨气的化学方程式为
(4)反应结束后,从三颈烧瓶中分离出产品,进行的实验操作是
(5)装置E的作用有
(6)设计实验:检验制得的产品中是否混有
 ?
?
您最近一年使用:0次
2023-07-14更新
|
78次组卷
|
2卷引用:四川省宜宾市叙州区第一中学校2023-2024学年高二上学期开学化学试题
10 . 苯酚是重要的化工原料,有关苯酚的实验如下:
(Ⅰ)苯酚的制备
工业上用异丙苯氧化法合成苯酚,其生产流程如图:
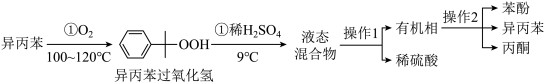
(1)异丙苯氧化过程①温度不能过高的原因是___________ 。
(2)检验有机相中是否含有水的试剂是___________ 。
(3)“操作1”的名称是___________ 。
(Ⅱ)苯酚的实验探究
探究铁盐种类和 对苯酚与
对苯酚与 显色反应的影响。
显色反应的影响。
查阅资料:ⅰ.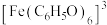 为紫色;
为紫色;
ⅱ. 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;
ⅲ.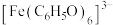 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与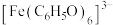 的浓度在一定范围内成正比
的浓度在一定范围内成正比
ⅳ.苯酚与 的显色原理:
的显色原理:
提出猜想:猜想1: 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响
猜想2: 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。
猜想3: 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。
进行实验:常温下,用盐酸调节配制得到 分别为a和b的
分别为a和b的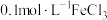 溶液(a>b),用硫酸调节配制得到
溶液(a>b),用硫酸调节配制得到 分别为a和b的
分别为a和b的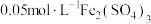 溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含
溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验
的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验 改变对
改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。
结果讨论:实验结果为 。
。
(4)①根据实验结果,小组同学认为此结果不足以证明猜想3成立的理由是___________ 。
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中相关内容。(限选试剂: 溶液、
溶液、 溶液、
溶液、 固体、
固体、 固体)
固体)
③小组同学得出实验结果为: ,
,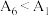 ,由此得出此结论是
,由此得出此结论是___________ 。
④根据实验1~6的结果,小组同学得出猜想3成立,且 对
对 与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是
与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是___________ 。
(Ⅰ)苯酚的制备
工业上用异丙苯氧化法合成苯酚,其生产流程如图:

(1)异丙苯氧化过程①温度不能过高的原因是
(2)检验有机相中是否含有水的试剂是
(3)“操作1”的名称是
(Ⅱ)苯酚的实验探究
探究铁盐种类和
 对苯酚与
对苯酚与 显色反应的影响。
显色反应的影响。查阅资料:ⅰ.
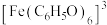 为紫色;
为紫色;ⅱ.
 对苯酚与
对苯酚与 的显色反应无影响;
的显色反应无影响;ⅲ.
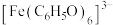 对特定波长光的吸收程度(用吸光度A表示)与
对特定波长光的吸收程度(用吸光度A表示)与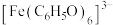 的浓度在一定范围内成正比
的浓度在一定范围内成正比ⅳ.苯酚与
 的显色原理:
的显色原理:
提出猜想:猜想1:
 对苯酚与
对苯酚与 的显色反应有影响
的显色反应有影响猜想2:
 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。猜想3:
 对苯酚与
对苯酚与 的显色反应有影响。
的显色反应有影响。进行实验:常温下,用盐酸调节配制得到
 分别为a和b的
分别为a和b的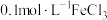 溶液(a>b),用硫酸调节配制得到
溶液(a>b),用硫酸调节配制得到 分别为a和b的
分别为a和b的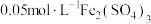 溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含
溶液。取5mL苯酚溶液于试管中,按实验1~4分别再加入0.1mL含 的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验
的试剂,显色10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验 改变对
改变对 水解程度的影响可忽略)。
水解程度的影响可忽略)。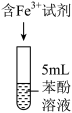 | 序号 | 含 的试剂 的试剂 | 吸光度 | |
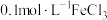 溶液 溶液 | 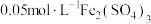 溶液 溶液 | |||
| 1 |  | / |  | |
| 2 |  | / |  | |
| 3 | / |  |  | |
| 4 | / |  |  | |
 。
。(4)①根据实验结果,小组同学认为此结果不足以证明猜想3成立的理由是
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中相关内容。(限选试剂:
 溶液、
溶液、 溶液、
溶液、 固体、
固体、 固体)
固体) | 序号 | 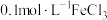 溶液 溶液 | 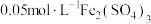 溶液 溶液 | 再加试剂 | 吸光度 |
| 5 | / |  |  固体 固体 | 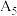 | |
| 6 |  | / | 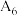 |
 ,
,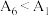 ,由此得出此结论是
,由此得出此结论是④根据实验1~6的结果,小组同学得出猜想3成立,且
 对
对 与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是
与苯酚的显色反应有抑制作用,从化学平衡角度解释其原因是
您最近一年使用:0次



