山东省泰安市宁阳一中2020-2021学年高一上学期第一次阶段性考试化学试题
山东
高一
阶段练习
2020-12-08
658次
整体难度:
容易
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
①观察法 ②实验法 ③分类法 ④比较法 ⑤假说法 ⑥模型法
| A.①② | B.①②④ | C.③⑤ | D.全部 |
①Na2O与Na2O2都能和水反应生成碱,它们的化学性质完全相同;②Na2CO3溶液和NaHCO3溶液都能与CaCl2溶液反应得到白色沉淀;③钠在常温下不易被氧化;④Na2O2可作供氧剂,而Na2O不能;⑤向紫色石蕊溶液中加入Na2O2粉末,溶液先变蓝后褪色,并有气泡冒出;⑥钠与CuSO4溶液反应,放出气体并生成蓝色沉淀。
| A.都正确 | B.②④⑤⑥ |
| C.②⑤⑥ | D.④⑤⑥ |
| A.阿伏加 德罗常数就是6.02×1023 |
| B.标准状况下,11.2L H2O所含分子数为0.5NA |
C.1.8g的 中含有的电子数为NA 中含有的电子数为NA |
| D.0.1mol·L-1的MgCl2溶液中所含Cl-的数目为0.2NA |
| A.向新制氯水中滴入几滴石蕊溶液,溶液先变红后褪色 |
| B.氯气泄漏,可用浸有NaOH溶液的毛巾捂住口鼻,逃离现场 |
| C.铜丝在氯气中燃烧,生成蓝色的氯化铜 |
| D.氯元素在自然界中既有单质又有化合物存在 |
| A.AlCl3 | B.FeCl3 | C.FeCl2 | D.CuCl2 |
【知识点】 氯气与金属单质的反应解读 铁与非金属单质反应解读 铜与非金属单质反应
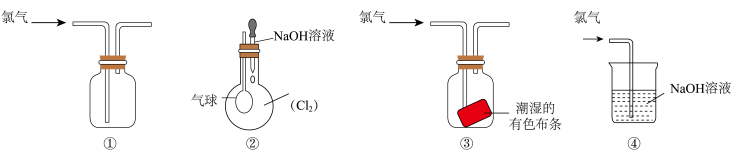
①可用于氯气的收集 ②若气球干瘪,证明Cl2可与NaOH反应 ③可证明氯气具有漂白性 ④可用于实验室中氯气的尾气吸收
| A.①② | B.①③ | C.②③ | D.①④ |
| A.漂白粉被氧化了 |
| B.有色布条被空气中的氧气氧化了 |
| C.漂白粉跟空气中的CO2反应充分,生成了较多量的 HClO |
| D.漂白粉溶液蒸发掉部分水,其浓度增大 |
【知识点】 次氯酸及其性质解读 漂白粉和漂粉精 漂白粉的变质原因及检验解读
A. mol-1 mol-1 | B.44x mol-1 |
C. mol-1 mol-1 | D.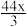 mol-1 mol-1 |
| A.过氧化钠——漂白剂 |
| B.次氯酸钠——消毒剂 |
| C.纯碱——治疗胃酸过多 |
| D.小苏打——制作馒头和面包的膨松剂 |
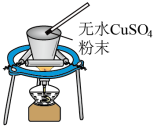
| A.上述反应是置换反应 |
| B.上述反应是放热反应 |
| C.上述反应中CuSO4表现了吸水性 |
| D.加热且无水条件下,Na可以与CuSO4反应并生成Cu |
①观察颜色 ②打开瓶盖看有无白雾 ③硝酸银溶液 ④湿润的红色石蕊试纸 ⑤湿润的蓝色石蕊试纸
| A.①②③④ | B.①②⑤ | C.①②④⑤ | D.①②④ |
【知识点】 物质的检验 物质性质实验方案的设计解读
| A.氧元素的质量比为1∶1 | B.分子数之比为1∶1 |
| C.原子总数之比为1∶1 | D.质量之比为1∶1 |
| A.1molH2O的质量为18g/mol |
| B.CH4的摩尔质量为16g |
| C.3.01×1023个SO2分子的质量为32g |
| D.0.05molSO2的体积是1.12L |
【知识点】 摩尔质量 22.4L/mol适用条件解读 物质的量有关计算
A. | B. | C. | D. |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.100mL该溶液中含有Na+ 0.01mol |
| B.1L该溶液中含有NaOH 0.4g |
| C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01mol/L |
| D.在1L水中溶解4gNaOH即可配制得0.1mol/LNaOH溶液 |
【知识点】 物质的量浓度的计算 物质的量浓度计算-溶液配制有关计算解读
| A.二者在水中的溶解度不同,Na2CO3<NaHCO3 |
| B.等物质的量的Na2CO3、NaHCO3分别与足量盐酸反应,产生的CO2质量相同 |
| C.Na2CO3俗称小苏打 |
| D.二者在一定的条件下不能相互转化 |
【知识点】 碳酸钠与碳酸氢钠性质的比较解读
|
|
|
|
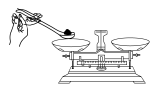
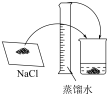
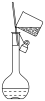
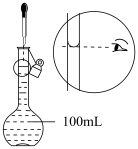
| A.接近称量质量时,轻振手腕,加够药品 | B.溶解时,用量筒控制所加蒸馏水的量 | C.移液时,玻璃棒插在刻度线以上,防止液体洒出 | D.液面接近刻度线1~2cm时,用胶头滴管滴加蒸馏水至刻度线 |
| A.A | B.B | C.C | D. D |
【知识点】 一定物质的量浓度的溶液的配制
| A.10mL 0.1mol·L-1的氯化铝溶液 | B.30mL 0.1mol·L-1的氯化钙溶液 |
| C.30mL 0.2mol·L-1的氯化钾溶液 | D.40mL 0.25mol·L-1的氯化钠溶液 |
【知识点】 某溶液与物质的量浓度相关的物理量的判断解读
二、多选题 添加题型下试题

| A.该实验说明Cl2分子具有漂白性 |
| B.该实验说明H+扩散速度比HClO分子快 |
| C.将实验后的pH试纸在酒精灯上微热,试纸又恢复为原来的颜色 |
| D.若用久置的氯水进行实验,不会产生相同的实验现象 |
A. | B.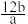 | C.bNA | D.aNA |
【知识点】 阿伏加德罗常数 结合物质结构基础知识与NA相关推算解读
三、单选题 添加题型下试题
| A.X2Y3 | B.XY | C.X3Y | D.XY3 |
【知识点】 阿伏加德罗定律 阿伏加德罗定律的应用解读
| A.250m/81V mol/L | B.500m/81V mol/L |
| C.1000m/81V mol/L | D.2000m/81V mol/L |
 NH3↑+CO2↑+H2O↑。现有2mol碳酸氢铵,加热使其完全分解,120℃下收集生成的气体于一密闭容器中,该密闭容器中混合气体的平均相对分子质量及氨气的物质的量分别是( )
NH3↑+CO2↑+H2O↑。现有2mol碳酸氢铵,加热使其完全分解,120℃下收集生成的气体于一密闭容器中,该密闭容器中混合气体的平均相对分子质量及氨气的物质的量分别是( )| A.26.33 2mol | B.30.5 2mol |
| C.26.33 1mol | D.30.5 1mol |
【知识点】 物质的量有关计算
四、计算题 添加题型下试题
(1)在标准状况下,67.2LCO2是
(2)在标准状况下,1.7g氨气所占的体积约为
(3)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为
五、解答题 添加题型下试题
①此盐酸的物质的量浓度为
②需要95mL3.00moL·L-1的盐酸,配制时需以上浓盐酸的体积为
③上述实验中所用到的玻璃仪器有
④用浓盐酸配制3.00mol·L-1稀盐酸,操作步骤的正确顺序是
a.计算需要浓盐酸的体积。
b.用量筒量取浓盐酸。
c.将烧杯中的溶液注入100mL容量瓶中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶。
d.把量好体积的浓盐酸倒入烧杯中,加适量蒸馏水稀释,冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm处,改用胶头滴管小心滴加蒸馏水至凹液面与刻度线相平。
(2)下列操作使溶液物质的量浓度偏高的是:
A.没有将洗涤液转移到容量瓶中
B.容量瓶洗净后未经干燥处理
C.转移过程中有少量溶液溅出
D.未冷却至室温就转移定容
E.摇匀后立即观察,发现溶液未达到刻度线,再用滴管加几滴蒸馏水至刻度线
F.定容时俯视刻度线
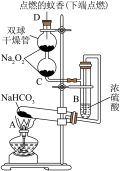
(1)在A试管内发生反应的化学方程式是
(2)B装置的作用是
(3)在双球干燥管内发生反应的化学方程式为
(4)实验时在C装置中观察到的现象是
(5)若将双球干燥管内的Na2O2换成Na2O,则实验时观察到的现象是
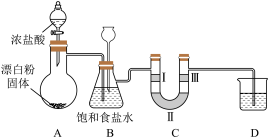
已知:装置A是氯气的发生装置,反应的化学方程式为Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑ +2H2O
据此回答下列问题:
(1)装置B中饱和食盐水的作用是
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:
(3)装置C的作用是验证氯气是否具有漂白性,则装置C中I、Ⅱ、Ⅲ处依次应放入的物质是
| 序号 | I | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| c | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)装置D作用是
六、计算题 添加题型下试题
【知识点】 化学方程式计算中物质的量的运用解读 过氧化钠的相关计算解读
试卷分析
试卷题型(共 30题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学特点 | |
| 2 | 0.85 | 化学研究基本方法 | |
| 3 | 0.65 | 钠 过氧化钠 碳酸钠 | |
| 4 | 0.65 | 阿伏加德罗常数的含义 22.4L/mol适用条件 结合物质结构基础知识与NA相关推算 依据物质的量浓度公式的基础计算 | |
| 5 | 0.94 | 卤素在自然界的存在 氯气与金属单质的反应 氯水的性质 | |
| 6 | 0.85 | 氯气与金属单质的反应 铁与非金属单质反应 铜与非金属单质反应 | |
| 7 | 0.4 | 氯气的实验室制法 化学实验探究 综合实验设计与评价 | |
| 8 | 0.65 | 次氯酸及其性质 漂白粉和漂粉精 漂白粉的变质原因及检验 | |
| 9 | 0.85 | 阿伏加德罗常数的求算 根据n=m/M进行相关计算 结合物质结构基础知识与NA相关推算 | |
| 10 | 0.85 | 漂白粉和漂粉精 过氧化钠的物理性质、组成、结构及用途 碳酸钠的俗称、物理性质及用途 碳酸氢钠的俗称、物理性质及用途 | |
| 11 | 0.85 | 钠 钠的化学性质 物质性质的探究 | |
| 12 | 0.85 | 物质的检验 物质性质实验方案的设计 | |
| 13 | 0.65 | 根据n=N/NA进行相关计算 根据n=m/M进行相关计算 以N=m·NA/M为中心的有关基本粒子的推算 | |
| 14 | 0.85 | 摩尔质量 22.4L/mol适用条件 物质的量有关计算 | |
| 15 | 0.94 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 16 | 0.94 | 物质的量浓度的计算 物质的量浓度计算-溶液配制有关计算 | |
| 17 | 0.85 | 钠与水反应原理 钠与盐溶液的反应 | |
| 18 | 0.85 | 碳酸钠与碳酸氢钠性质的比较 | |
| 19 | 0.85 | 一定物质的量浓度的溶液的配制 | |
| 20 | 0.85 | 某溶液与物质的量浓度相关的物理量的判断 | |
| 23 | 0.65 | 阿伏加德罗定律 阿伏加德罗定律的应用 | |
| 24 | 0.65 | 物质的量浓度计算-与溶质成分有关的计算 物质的量浓度计算-溶液稀释的有关计算 | |
| 25 | 0.65 | 物质的量有关计算 | |
| 二、多选题 | |||
| 21 | 0.85 | 氯水的成分及检验 氯水的性质 氯水性质实验探究 | |
| 22 | 0.65 | 阿伏加德罗常数 结合物质结构基础知识与NA相关推算 | |
| 三、计算题 | |||
| 26 | 0.65 | 气体摩尔体积 物质的量有关计算 | |
| 30 | 0.85 | 化学方程式计算中物质的量的运用 过氧化钠的相关计算 | |
| 四、解答题 | |||
| 27 | 0.65 | 配制一定物质的量浓度的溶液实验的误差分析 配制一定物质的量浓度的溶液实验的仪器 配制一定物质的量浓度溶液的综合考查 | 实验探究题 |
| 28 | 0.4 | 过氧化钠 物质性质的探究 | 实验探究题 |
| 29 | 0.65 | 氯气的化学性质 氯气的实验室制法 化学实验方案的设计与评价 物质性质的探究 | 实验探究题 |