26. 小组同学用FeSO
4·7H
2O晶体和蒸馏水配制0.5mol·L
−1FeSO
4溶液(pH为3.3)。1h后,溶液变黄。24h后,产生黄褐色沉淀,测得上层清液pH为1.4。
(1)取少量黄色溶液,
______(填操作和现象),证明黄色溶液中含有Fe
3+。
(2)取黄色溶液,加入铁粉振荡,溶液由黄色变为浅绿色,反应的离子方程式为
______。
(3)探究溶液变黄的原因。
①实验证实,溶液变黄是因为空气中的O
2将Fe
2+氧化,反应的离子方程式为
_______。
②用FeSO
4和稀硫酸配制不同溶液,进一步探究影响溶液变黄的其他因素,实验如下。
实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
c(FeSO4)/(mol·L−1) | 0.5 | 0.25 | 0.5 | 0.25 |
溶液pH | 3.3 | 3.5 | 2.9 | 2.9 |
初始颜色 | 浅绿色 | 浅绿色,比Ⅰ浅 | 浅绿色,同Ⅰ | 浅绿色,同Ⅱ |
0.5h颜色 | 浅绿色 | 黄绿色 | 浅绿色 | 浅绿色 |
5h颜色 | 黄色 | 黄色 | 浅黄色 | 浅黄色(比Ⅲ浅) |
a.实验Ⅲ和Ⅳ说明
_______对溶液变黄快慢有影响。
b.实验Ⅱ比Ⅰ更快变黄的原因是
_______。
(4)检验黄褐色沉淀的成分。
①通过下列实验证实,黄褐色沉淀中含有SO

。
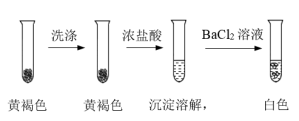
a.证实黄褐色沉淀中含有SO

的证据是
_______。
b.洗涤黄褐色沉淀的目的是
_______。
②进一步实验证实黄褐色沉淀为Fe(OH)SO
4.将反应的离子方程式补充完整:Fe
3++___+___=Fe(OH)SO
4↓+___,
_______。
(5)根据以上实验,配制FeSO
4溶液时,为使溶液较长时间保持浅绿色,还需加入铁粉和稀硫酸,其中稀硫酸的作用是
_____(答出两点)。