2015届湖北大冶一中等六校高三元月调考理综化学试卷
湖北
高三
阶段练习
2017-07-26
476次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、化学反应原理、有机化学基础、化学实验基础、物质结构与性质
2015届湖北大冶一中等六校高三元月调考理综化学试卷
湖北
高三
阶段练习
2017-07-26
476次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、化学反应原理、有机化学基础、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
适中(0.64)
1. 化学与人类生产、生活、社会可持续发展密切相关。下列说法不正确的是
| A.绿色化学的核心是应用化学原理对环境污染进行治理 |
| B.石油液化气、汽油和石蜡的主要成分都是碳氢化合物 |
| C.“天宫一号”中使用的碳纤维,是一种新型无机非金属材料 |
| D.光化学烟雾是氮氧化物受紫外线照射后产生的O3直接与空气中的一些碳氢化合物作用后生成的一种有毒烟雾 |
您最近一年使用:0次
2016-12-09更新
|
284次组卷
|
3卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
单选题
|
适中(0.64)
2. NA为阿伏加德罗常数,下列叙述正确的是
| A.6.8g熔融的KHSO4中含有0.05NA个阴离子 |
| B.1.0L 1mol/L的NaOH水溶液中含有的氧原子数目为NA |
| C.25 ℃时,pH=13的氢氧化钡溶液中含有0.1NA个氢氧根离子 |
| D.5.6g铁与一定量稀硝酸完全反应,电子转移数目一定为0.3NA |
【知识点】 化学计量
您最近一年使用:0次
单选题
|
适中(0.64)
3. 下列离子方程式书写正确的是
| A.H218O中投入Na2O2固体:2H218O+2Na2O2===4OH-+4Na++18O2↑ |
| B.Fe3O4与稀HNO3反应:Fe3O4+8H+===Fe2++2Fe3++4H2O |
C.向NaHCO3溶液中加入少量Ca(OH)2:HCO3-+Ca2++OH ===CaCO3↓+H2O ===CaCO3↓+H2O |
| D.将少量NaOH溶液加入到NH4HCO3溶液中:OH-+HCO3-===CO32-+H2O |
【知识点】 离子反应的发生及书写
您最近一年使用:0次
2016-12-09更新
|
98次组卷
|
2卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
单选题
|
适中(0.65)
解题方法
4. 下列叙述正确的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液的pH=4 |
| B.25℃时Ksp(AgCl)=1.8×10—10,向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度可能增大 |
| C.浓度均为0.1 mol·L-1的下列溶液,pH由大到小的排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4 |
| D.为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸 |
您最近一年使用:0次
2016-12-09更新
|
240次组卷
|
4卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
单选题
|
适中(0.65)
5. 下列实验中,依据实验操作及现象,得出的结论正确的是
| 操作 | 现象 | 结论 | |
| A | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
| B | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2(g) N2O4(g);ΔH<0 N2O4(g);ΔH<0 |
| C | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡 | 上层分别呈无色和紫红色 | 还原性:I->Br->Fe2+ |
| D | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或SO32- |
| A.A | B.B | C.C | D.D |
【知识点】 氧化性、还原性强弱的比较解读 化学平衡的移动及其影响因素
您最近一年使用:0次
2015-03-18更新
|
219次组卷
|
2卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
单选题
|
较易(0.85)
6. 下列说法正确的是
| A.煤经处理变为气体燃料的过程属于物理变化 |
| B.淀粉、油脂和蛋白质都是高分子化合物 |
| C.乙烯和乙醇均可使酸性KMnO4溶液褪色 |
| D.乙酸乙酯和植物油均可水解生成乙醇 |
【知识点】 油脂的基本组成与结构解读 煤的气化解读
您最近一年使用:0次
2016-12-09更新
|
573次组卷
|
5卷引用:2014届广东省十校联考高三下学期理综化学试卷
单选题
|
适中(0.64)
7. 用酸性氢氧燃料电池(乙池)为电源进行电解的实验装置(甲池,一定条件下可实现有机物的电化学储氢)如下图所示。甲池中A为含苯的物质的量分数为10%的混合气体,B为10mol混合气体其中苯的物质的量分数为24%,C为标准状况下2.8mol气体(忽略水蒸气),下列说法不正确的是


| A.乙池中溶液的pH变大 |
| B.E处通入H2,C处有O2放出 |
| C.甲池中阴极区只有苯被还原 |
| D.导线中共传导11.2mol电子 |
【知识点】 电解池
您最近一年使用:0次
2016-12-09更新
|
264次组卷
|
2卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
二、填空题 添加题型下试题
填空题
|
较难(0.4)
8. X、Y、Z、W四种常见元素,且均为短周期元素。已知:①X的最高价氧化物对应的水化物为无机酸中最强酸;②Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料;③Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料;④W被称为军事金属,可在CO2中燃烧。
(1)X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为_________ 。
(2)Z的氧化物在通信领域用来作___________ ,工业上制Z单质的化学反应方程式为_________ 。
(3)在50mLlmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积最多为_________ mL。
(4)Y、W合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某Y、W合金(设不含其他元素)中W的质量分数,设计下列实验方案进行探究。称量x g Y、W合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧。欲计算W的质量分数。该实验中还需测定的数据是__________ 。 若用空气代替O2进行实验,对测定结果是否有影响?若有影响分析其原因__________________________________ 。

(1)X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为
(2)Z的氧化物在通信领域用来作
(3)在50mLlmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积最多为
(4)Y、W合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某Y、W合金(设不含其他元素)中W的质量分数,设计下列实验方案进行探究。称量x g Y、W合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧。欲计算W的质量分数。该实验中还需测定的数据是

【知识点】 化学实验基础
您最近一年使用:0次
2016-12-08更新
|
281次组卷
|
2卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
填空题
|
较难(0.4)
9. 甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:__________________ 。
(2)甲醇脱氢可制取甲醛CH3OH(g) HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:

①600K时,Y点甲醇的υ(逆)____ (正)(填“>”或“<”)
②从Y点到X点可采取的措施是____________________________ 。
③有同学计算得到在t1K时,该反应的平衡常数为8.1mol·L-1。你认为正确吗?请说明理由_____________________________________________________ 。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分别进行催化CH3OH的脱氢实验:CH3OH(g) HCHO(g)+H2(g)
HCHO(g)+H2(g)
CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
可以判断:实验①的前20 min的平均反应速率 ν(H2)=____________ ;实验温度
T1___ T2(填“>”、“<”);催化剂的催化效率:实验①___ 实验②(填“>”、“<”)。
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程,则Co2+在阳极的电极反应式为___________ ;除去甲醇的离子方程式为____________________ 。

(1)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)甲醇脱氢可制取甲醛CH3OH(g)
 HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如下图所示。回答下列问题:
①600K时,Y点甲醇的υ(逆)
②从Y点到X点可采取的措施是
③有同学计算得到在t1K时,该反应的平衡常数为8.1mol·L-1。你认为正确吗?请说明理由
(3)纳米级Cu2O由于具有优良的催化性能而受到关注。在相同的密闭容器中,使用不同方法制得的Cu2O(Ⅰ)和(Ⅱ)分别进行催化CH3OH的脱氢实验:CH3OH(g)
 HCHO(g)+H2(g)
HCHO(g)+H2(g)CH3OH的浓度(mol·L-1)随时间t (min)变化如下表:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
T1
(4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程,则Co2+在阳极的电极反应式为

您最近一年使用:0次
2019-01-30更新
|
141次组卷
|
2卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
三、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
10. 硫代硫酸钠是一种重要的化工产品。工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq) Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成 一段液注,若________ ,则整个装置气密性良好。装置D的作用是_______ 。装置E中为__________ 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为______ 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择____ 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是___________ 。
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是______________ 。
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O3•5H2O和其他杂质)。某兴趣小组为测定该产品纯度,准确称取4.96g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L¯1碘的标准溶液滴定。反应原理为:2S2O32-+I2=S4O62-+2I¯,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为_________ 。

经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)_____________ 。[M(Na2S2O3•5H2O)=248g/mol]

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq)
 Na2S2O3(aq) (III)
Na2S2O3(aq) (III)(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成 一段液注,若
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O3•5H2O和其他杂质)。某兴趣小组为测定该产品纯度,准确称取4.96g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L¯1碘的标准溶液滴定。反应原理为:2S2O32-+I2=S4O62-+2I¯,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为

经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)
您最近一年使用:0次
2016-12-09更新
|
330次组卷
|
3卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
四、填空题 添加题型下试题
填空题
|
困难(0.15)
11. 近年,为提高能利用率,西方提出共生理念-为提高经济效益,人类生产活动尽可能多功能化.共生工程将会大大促进化学工业的发展。
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V.实际过程中,将SO2通入电池的_______ 极(填“正”或“负”),负极反应式为_______ .用这种方法处理SO2废气的优点是_______ 。
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质.合成路线如图:
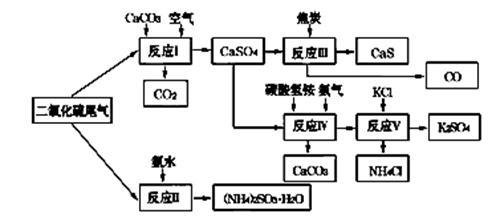
①生产中,向反应Ⅱ中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是_______ 。
②下列有关说法正确的是_______ (填序号)。
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为CaSO4+4C CaS+4CO↑
CaS+4CO↑
C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
③反应Ⅴ中选用了40%的乙二醇溶液做溶剂,温度控制在25℃,此时硫酸钾的产率超过90%,选用40%的乙二醇溶液做溶剂的原因是_______ 。
④(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统.写出二氧化氮与亚硫酸铵反应的化学方程式_______ .
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V.实际过程中,将SO2通入电池的
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质.合成路线如图:

①生产中,向反应Ⅱ中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是
②下列有关说法正确的是
A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅲ中发生反应的化学方程式为CaSO4+4C
 CaS+4CO↑
CaS+4CO↑C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
③反应Ⅴ中选用了40%的乙二醇溶液做溶剂,温度控制在25℃,此时硫酸钾的产率超过90%,选用40%的乙二醇溶液做溶剂的原因是
④(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统.写出二氧化氮与亚硫酸铵反应的化学方程式
【知识点】 原电池 化学在工农业中的应用
您最近一年使用:0次
2016-12-08更新
|
515次组卷
|
6卷引用:2013届湖北省襄阳市高三元月第一次调研考试理综化学试卷
(已下线)2013届湖北省襄阳市高三元月第一次调研考试理综化学试卷(已下线)2014届江西省重点中学协作体高三第一次联考理综化学试卷2015届湖北省部分高中高三元月调考理综化学试卷2015届辽宁省丹东五校协作体高三上学期期末考试理综化学试卷2015届湖北大冶一中等六校高三元月调考理综化学试卷2015届江西省南昌三中高三上学期第六次考试理综化学试卷
五、解答题 添加题型下试题
解答题-结构与性质
|
适中(0.65)
解题方法
12. 已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族。 E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号___ ,该能层具有的原子轨道数为____ 。
(2)E2+离子的价层电子排布图是________ ,F原子的电子排布式是________ 。
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为________ ,B元素的气态氢化物的VSEPR模型为____________________ 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为______ 。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程为______ 。
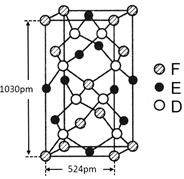
(6)某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为___________ ,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度d=______ g/cm3。(保留两位小数)
(1)基态D原子中,电子占据的最高能层符号
(2)E2+离子的价层电子排布图是
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程为
(6)某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为

您最近一年使用:0次
2016-12-08更新
|
252次组卷
|
3卷引用:2015届湖北省部分高中高三元月调考理综化学试卷
六、多选题 添加题型下试题
多选题
|
较难(0.4)
13. 【化学—选修5有机化学基础】
脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下:

(1)Ⅱ中含氧官能团的名称 。
(2)反应②的化学方程式 。
(3)Ⅰ和Ⅲ在浓硫酸催化加热时反应的化学方程式 。
(4)下列说法正确的是 。
(5)A的结构简式 。
(6)Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种。写出满足上述条件的Ⅵ的结构简式 。
(7)一定条件下,化合物Ⅶ 也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式 。
也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式 。
脱水环化是合成生物碱类天然产物的重要步骤,某生物碱V合成路线如下:

(1)Ⅱ中含氧官能团的名称 。
(2)反应②的化学方程式 。
(3)Ⅰ和Ⅲ在浓硫酸催化加热时反应的化学方程式 。
(4)下列说法正确的是 。
(5)A的结构简式 。
(6)Ⅵ与Ⅰ互为同分异构体,Ⅵ遇FeCl3发生显色反应,其苯环上的一氯代物只有2种。写出满足上述条件的Ⅵ的结构简式 。
(7)一定条件下,化合物Ⅶ
 也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式 。
也能发生类似反应④的环化反应,Ⅶ的环化产物的结构简式 。| A.Ⅰ和Ⅴ均属于芳香烃 | B.Ⅱ能发生银镜反应 |
| C.Ⅱ能与4molH2发生加成反应 | D.反应③属于酯化反应 |
【知识点】 有机物的合成与推断
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学与STSE、认识化学科学、化学反应原理、有机化学基础、化学实验基础、物质结构与性质
试卷题型(共 13题)
题型
数量
单选题
7
填空题
3
解答题
2
多选题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.64 | 化学与环境保护 化学与材料的发展 | |
| 2 | 0.64 | 化学计量 | |
| 3 | 0.64 | 离子反应的发生及书写 | |
| 4 | 0.65 | 溶液pH的计算 强电解质和弱电解质的判断 盐溶液中离子浓度大小的比较 同离子效应对难溶电解质溶解平衡的影响 | |
| 5 | 0.65 | 氧化性、还原性强弱的比较 化学平衡的移动及其影响因素 | |
| 6 | 0.85 | 油脂的基本组成与结构 煤的气化 | |
| 7 | 0.64 | 电解池 | |
| 二、填空题 | |||
| 8 | 0.4 | 化学实验基础 | |
| 9 | 0.4 | 化学平衡 电解池 | |
| 11 | 0.15 | 原电池 化学在工农业中的应用 | |
| 三、解答题 | |||
| 10 | 0.4 | 化学实验基础 仪器使用与实验安全 | 实验探究题 |
| 12 | 0.65 | 轨道表示式 等电子原理的应用 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 四、多选题 | |||
| 13 | 0.4 | 有机物的合成与推断 | |



