2015届四川省资阳市高三第三次模拟考试理综化学试卷
四川
高三
三模
2017-07-26
763次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、物质结构与性质、化学实验基础、认识化学科学、化学反应原理、常见无机物及其应用
2015届四川省资阳市高三第三次模拟考试理综化学试卷
四川
高三
三模
2017-07-26
763次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、物质结构与性质、化学实验基础、认识化学科学、化学反应原理、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
容易(0.94)
1. 化学与生活密切相关,下列说法不正确的是
| A.饮用牛奶和豆浆可以缓解重金属引起的中毒 |
| B.向煤中加入适量石灰石,可减少其燃烧产物中的SO2,降低对大气的污染 |
| C.食品包装袋、食物保鲜膜等材料的主要成分是聚氯乙烯 |
| D.混凝法、中和法和沉淀法是污水处理中常用的化学方法 |
您最近一年使用:0次
单选题
|
较易(0.85)
2. 下列判断正确的是
| A.HClO4、H2SO4、CH3COOH、H2CO3酸性依次减弱 |
| B.Cl-、Na+、Mg2+、F-的半径依次减小 |
| C.Na、Mg、Al失电子能力随最外层电子的增加而增强 |
| D.HI、HBr、HCl、HF的沸点依次降低 |
您最近一年使用:0次
2016-12-09更新
|
109次组卷
|
2卷引用:2015届四川省资阳市高三第三次模拟考试理综化学试卷
单选题
|
适中(0.65)
3. 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向FeCl3溶液中滴加NaOH溶液 | 制备Fe(OH)3胶体 |
| B | 将CO2通入水玻璃溶液中 | 证明C元素的非金属性大于Si |
| C | 向苯和苯酚的混合溶液中加入足量的浓溴水,充分反应后过滤 | 除去苯中混有的苯酚 |
| D | 淀粉与稀H2SO4共热,再加入银氨溶液水浴加热 | 验证淀粉水解产物有无还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.64)
4. 常温下,下列各组离子在给定溶液中一定能大量共存的是
| A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B.Kw=1.01×10-14的某无色溶液:NH4+、K+、AlO2-、Cl- |
| C.与铝反应产生大量氢气的溶液:Na+、Ba2+、HCO3-、NO3- |
| D.由水电离出来的c(H+)=1.0×10-13 mol·L-1的溶液:K+、Na+、NO3-、Cl- |
【知识点】 离子共存
您最近一年使用:0次
单选题
|
适中(0.65)
5. 设NA代表阿伏加德罗常数的数值,下列说法正确的是
| A.12.4 g白磷中含有共价键数为0.4NA |
| B.3Fe+4H2O(g)===Fe3O4+4H2反应中,当5.6 g Fe全部转化为Fe3O4时,则有0.3NA电子发生转移 |
| C.在1 L 0.1 mol·L-1碳酸钠溶液中阴离子总数等于0.1NA |
| D.在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为10NA |
【知识点】 阿伏加德罗常数的应用解读 物质的量有关计算
您最近一年使用:0次
2016-12-09更新
|
311次组卷
|
3卷引用:2015届四川省资阳市高三第三次模拟考试理综化学试卷
2015届四川省资阳市高三第三次模拟考试理综化学试卷(已下线)2019年7月1日 《每日一题》2020年高考一轮复习-以阿伏加德罗常数为背景的选择题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解的基础考查
单选题
|
适中(0.65)
6. 下列溶液中微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1某二元弱酸的酸式盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
| B.某酸式盐NaHY的水溶液显碱性,该酸式盐溶液中离子浓度关系为:c(Na+)>c(HY-)>c (OH-)>c(H+) |
| C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)=c(H+)+c(CH3COOH) |
| D.25 ℃,pH=12的氨水和pH=2的盐酸等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 某温度T1时,向容积为2L的恒容密闭容器中充入一定量的H2和I2(g),发生反应:H2(g)+I2(g)  2HI(g),反应过程中测定的部分数据见下表(表中t2>t1)。下列说法正确的是
2HI(g),反应过程中测定的部分数据见下表(表中t2>t1)。下列说法正确的是
 2HI(g),反应过程中测定的部分数据见下表(表中t2>t1)。下列说法正确的是
2HI(g),反应过程中测定的部分数据见下表(表中t2>t1)。下列说法正确的是| 反应时间/min | n(H2)/mol | n(I2)/mol |
| 0 | 0.9 | 0.3 |
| t1 | 0.8 | |
| t2 | 0.2 |
A.反应在tmin内的平均速率为:v(H2)=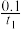 mol-1·L-1·min-l mol-1·L-1·min-l |
| B.保持其他条件不变,向平衡体系中再通0.20molH2,与原平衡相比,达到新平衡时I2(g)转化率增大,H2的体积分数不变 |
| C.保持其他条件不变,起始时向容器中充入的H2和I2(g)都为0.5mol,达到平衡时 n(HI)=0.2mol |
| D.升高温度至T2时,上述反应平衡常数为0.18,则正反应为吸热反应 |
您最近一年使用:0次
2018-07-18更新
|
185次组卷
|
3卷引用:2015届四川省资阳市高三第三次模拟考试理综化学试卷
二、填空题 添加题型下试题
填空题
|
适中(0.65)
8. 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A与B同周期、A与D同族,A原子核外有两个未成对电子,B元素的第一电离能比同周期相邻两种元素都大,C原子在同周期原子中半径最大(稀有气体除外);E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满。请根据以上信息回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)E原子核外电子排布式是_____________ 。
(2)B的最高价含氧酸根的空间构型为__________________ 。
(3)A、B、D三种元素电负性由大到小排列顺序为____________ 。
(4)D单质比化合物DA的熔点____ (填“高”或“低”),理由是_______________ 。
(5)已知A、C和地壳中含量最多的元素按1∶1∶2的原子个数比可形成某离子化合物,该化合物能使酸性高锰酸钾溶液褪色,写出发生反应的离子方程式___________________________ 。
(1)E原子核外电子排布式是
(2)B的最高价含氧酸根的空间构型为
(3)A、B、D三种元素电负性由大到小排列顺序为
(4)D单质比化合物DA的熔点
(5)已知A、C和地壳中含量最多的元素按1∶1∶2的原子个数比可形成某离子化合物,该化合物能使酸性高锰酸钾溶液褪色,写出发生反应的离子方程式
您最近一年使用:0次
2016-12-09更新
|
172次组卷
|
2卷引用:2015届四川省资阳市高三第三次模拟考试理综化学试卷
三、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
9. 学习小组设计了如下图实验(部分装置),将氯气依次通过下列装置以验证氯气的性质:

(1)通入氯气后,A中的现象是 。C装置中发生反应的离子方程式为: 。
(2)通入氯气一段时间后,B瓶的溶液中有一部分SO32-氧化成SO42-。该试验方案,检验B瓶溶液中Cl-和SO42-的存在。
实验步骤2的目的是: 。
(3)为准确测定通入氯气一段时间后C瓶中剩余FeCl2的物质的量。实验如下:
①配制250 mL 溶液:将C瓶中全部溶液取出盛于250 mL容量瓶中,并准确配制成250 mL溶液。确保C瓶中的溶液全部取出(溶质无损失),需进行的操作是 。
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,将0.20 mol/L KMnO4溶液装入 滴定至终点,记录数据。重复滴定2次。平均消耗KMnO4溶液V mL。
(反应方程式: Fe2++MnO4-+H+ — Fe3++Mn2++H2O,未配平)
③计算:C瓶中剩余FeCl2的物质的量,n(FeCl2)= mol。

(1)通入氯气后,A中的现象是 。C装置中发生反应的离子方程式为: 。
(2)通入氯气一段时间后,B瓶的溶液中有一部分SO32-氧化成SO42-。该试验方案,检验B瓶溶液中Cl-和SO42-的存在。
| 实 验 步 骤 | 预期现象和结论 |
| 步骤1:取适量B瓶中溶液于一干净试管中,滴加 。 | 若产生白色沉淀,则B瓶溶液中存在SO42-。 |
| 步骤2:另取适量B瓶中溶液于试管一干净试管中,滴加过量的2 mol/L HNO3和l mol/L Ba(NO3)2溶液,振荡,静置。 | 产生白色沉淀。 |
| 步骤3:取步骤2后试管中的上层清液于一干净试管中,滴加0. 1 mol/L AgNO3溶液,振荡。 | 。 |
(3)为准确测定通入氯气一段时间后C瓶中剩余FeCl2的物质的量。实验如下:
①配制250 mL 溶液:将C瓶中全部溶液取出盛于250 mL容量瓶中,并准确配制成250 mL溶液。确保C瓶中的溶液全部取出(溶质无损失),需进行的操作是 。
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,将0.20 mol/L KMnO4溶液装入 滴定至终点,记录数据。重复滴定2次。平均消耗KMnO4溶液V mL。
(反应方程式: Fe2++MnO4-+H+ — Fe3++Mn2++H2O,未配平)
③计算:C瓶中剩余FeCl2的物质的量,n(FeCl2)= mol。
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
10. 聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域具有广泛应用。下图是利用乙酰丙酸(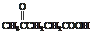 )合成聚芳酯E的路线:
)合成聚芳酯E的路线:
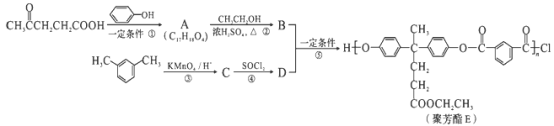
已知:①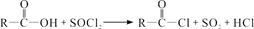
② (R、R′表示烃基)
(R、R′表示烃基)
(1)乙酰丙酸中含有的官能团是羰基和_______ (填官能团名称)。
(2)D的结构简式为_______ 。
(3)下列关于有机物B的说法正确的是_________ (填字母代号)。
a.能发生取代反应 b.能与浓溴水反应
c.能发生消去反应 d.能与H2发生加成反应
(4)A→B的化学方程式为_________ 。
(5)C的分子式为_________ ,符合下列条件的C的同分异构体有_________ 种。
①能发生银镜反应
②能与NaHCO3溶液反应
③分子中有苯环,分子中无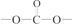 结构
结构
在上述同分异构体中,有一种苯环上有两个取代基且核磁共振氢谱图有4种峰的物质,写出该物质与足量NaOH溶液共热反应的化学方程式:_______________________________ 。
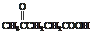 )合成聚芳酯E的路线:
)合成聚芳酯E的路线:
已知:①
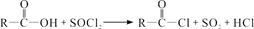
②
 (R、R′表示烃基)
(R、R′表示烃基)(1)乙酰丙酸中含有的官能团是羰基和
(2)D的结构简式为
(3)下列关于有机物B的说法正确的是
a.能发生取代反应 b.能与浓溴水反应
c.能发生消去反应 d.能与H2发生加成反应
(4)A→B的化学方程式为
(5)C的分子式为
①能发生银镜反应
②能与NaHCO3溶液反应
③分子中有苯环,分子中无
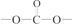 结构
结构在上述同分异构体中,有一种苯环上有两个取代基且核磁共振氢谱图有4种峰的物质,写出该物质与足量NaOH溶液共热反应的化学方程式:
您最近一年使用:0次
2016-12-09更新
|
743次组卷
|
5卷引用:2015届四川省资阳市高三第三次模拟考试理综化学试卷
解答题-工业流程题
|
适中(0.65)
11. 锌钡白是一种白色颜料。工业上是由ZnSO4与BaS溶液混合而成:BaS+ZnSO4=ZnS↓+BaSO4↓。请根据以下工业生产流程回答有关问题。
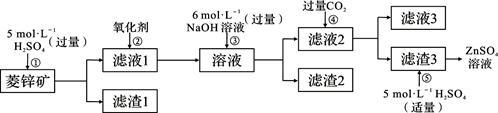
Ⅰ、ZnSO4溶液的制备与提纯:
有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;
b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2。
(1)②中使用的氧化剂最好是下列的___ (选填字母代号)。
A.Cl2 B.浓HNO3 C.KMnO4 D.H2O2
(2)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤_____ (选填①、②、③、⑤)。
(3)写出步骤④后产生滤渣3的化学式______ 。
(4)与Al相似,Zn也能溶于NaOH溶液。写出将Zn片和Cu片放入NaOH溶液中形成原电池的负极电极反应式:______________________ 。
Ⅱ、BaS溶液的制备:
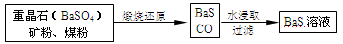
有关数据:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH1=-1473.2 kJ·mol-1
C(s)+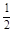 O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
Ba(s)+S(s)=BaS(s) ΔH3=-460 kJ·mol-1
(5)若煅烧还原的产物仅为BaS和CO,则其反应的热化学方程式为:______ 。
Ⅲ、制取锌钡白:
(6)如果生产流程步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌钡白产生的后果是___ 。

Ⅰ、ZnSO4溶液的制备与提纯:
有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;
b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2。
(1)②中使用的氧化剂最好是下列的
A.Cl2 B.浓HNO3 C.KMnO4 D.H2O2
(2)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤
(3)写出步骤④后产生滤渣3的化学式
(4)与Al相似,Zn也能溶于NaOH溶液。写出将Zn片和Cu片放入NaOH溶液中形成原电池的负极电极反应式:
Ⅱ、BaS溶液的制备:

有关数据:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH1=-1473.2 kJ·mol-1
C(s)+
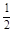 O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1Ba(s)+S(s)=BaS(s) ΔH3=-460 kJ·mol-1
(5)若煅烧还原的产物仅为BaS和CO,则其反应的热化学方程式为:
Ⅲ、制取锌钡白:
(6)如果生产流程步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌钡白产生的后果是
您最近一年使用:0次
2016-12-09更新
|
572次组卷
|
2卷引用:2015届四川省资阳市高三第三次模拟考试理综化学试卷
试卷分析
整体难度:适中
考查范围:有机化学基础、化学与STSE、物质结构与性质、化学实验基础、认识化学科学、化学反应原理、常见无机物及其应用
试卷题型(共 11题)
题型
数量
单选题
7
填空题
1
解答题
3
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 聚乙烯结构及应用 蛋白质 水污染 大气污染的治理原理及方法 | |
| 2 | 0.85 | 同周期元素性质递变规律 同主族元素性质递变规律 元素周期律的应用 元素非金属性强弱的比较方法 | |
| 3 | 0.65 | 物质的分离、提纯 常见物质的制备 物质的检验 | |
| 4 | 0.64 | 离子共存 | |
| 5 | 0.65 | 阿伏加德罗常数的应用 物质的量有关计算 | |
| 6 | 0.65 | 弱电解质的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 7 | 0.65 | 化学平衡的移动及其影响因素 化学平衡常数的影响因素及应用 | |
| 二、填空题 | |||
| 8 | 0.65 | 物质结构与性质综合考查 元素性质与电负性的关系 利用杂化轨道理论判断化学键杂化类型 原子晶体(旧教材) | |
| 三、解答题 | |||
| 9 | 0.65 | 离子反应的发生及书写 氧化还原反应有关计算 一定物质的量浓度的溶液的配制 物质的检验 | 实验探究题 |
| 10 | 0.4 | 有机官能团的性质及结构 同分异构体的数目的确定 含酯基有机物水解消耗NaOH的量的计算 高分子材料的有机推断 | 有机推断题 |
| 11 | 0.65 | 氢氧化铝 盖斯定律与热化学方程式 原电池电极反应式书写 物质制备的探究 | 工业流程题 |



